名校
1 . 下列有关物质性质与用途具有对应关系的是
| A.SiO2具有导电性,可用于制作光导纤维 |
| B.氨气具有弱碱性,可用作食品工业制冷剂 |
| C.AlCl3是电解质,可电解熔融AlCl3制铝 |
| D.FeCl3具有氧化性,可用作铜制线路板的蚀刻剂 |
您最近一年使用:0次
名校
解题方法
2 . 离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构如图所示。X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,X原子中电子只有一种自旋方向,Y、Z、Q为同一周期元素,W的原子核外有3个未成对电子。下列说法错误的是
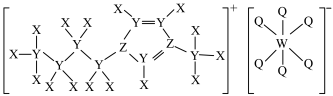
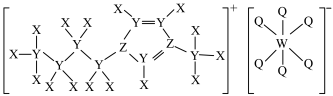
| A.简单离子半径:W>Z>Q |
| B.Z 和 W 的简单氢化物的沸点:Z>W |
| C.X 分别与 Y、Z 均能形成既含极性键又含非极性键的化合物 |
| D.Q、Z、W 的最高价氧化物对应的水化物的酸性:Q>Z>W |
您最近一年使用:0次
2024-02-15更新
|
141次组卷
|
2卷引用:湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题
解题方法
3 . A、B、C、D、E是原子序数依次增大的五种常见短周期主族元素,其中A、B、C、D四种元素的原子序数之和为E元素原子序数的2倍。E是短周期中原子半径最大的元素。A、B、C、D四种元素形成的化合物[CA4]+[BD4]-有多种用途,可用来合成纳米管,还可作杀虫剂、催化剂、阻燃剂等,其结构如图所示。下列说法正确的是
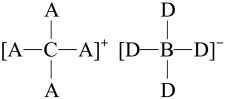
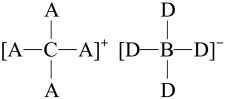
| A.元素A、C能形成含有非极性键的18电子化合物 |
| B.最简单氢化物的稳定性:C>D |
| C.元素D、E形成的化合物为共价化合物 |
| D.化合物[CA4]+[BD4]-中各原子均满足8电子稳定结构 |
您最近一年使用:0次
22-23高二下·江西·阶段练习
名校
4 . 第ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。下列说法错误的是
A. 分子内的共价键类型为非极性共价键 分子内的共价键类型为非极性共价键 |
B. 和 和 的键角大小: 的键角大小: |
C. 中心原子S的轨道杂化类型为 中心原子S的轨道杂化类型为 |
D. 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近一年使用:0次
5 . 硫酸钙用途广泛,下列说法不正确的是
A.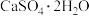 俗名:熟石膏 俗名:熟石膏 | B. 属于强电解质 属于强电解质 |
C. 中即含离子键又含共价键 中即含离子键又含共价键 | D.石膏可用来调节水泥硬化速度 |
您最近一年使用:0次
6 . 回答下列问题:
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用______(填序号,下同)。
(2)下列变化过程中放出热的是______ 。
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(3)下列变化:①碘的升华 ②烧碱熔化 ③氯化钠溶于水④氯化氢溶于水 ⑤氯气溶于水 ⑥氯化铵受热分解
未发生化学键破坏的是___________ ;仅发生离子键破坏的是___________ 。上述涉及的主要物质为纯净物时,属于共价化合物的是___________ ;属于离子化合物的是___________ 。
(1)冷敷袋俗称冰袋,在日常生活中有降温、保鲜和镇痛等多种用途。制作冷敷袋可以利用______(填序号,下同)。
| A.放热的化学变化 | B.吸热的化学变化 |
| C.放热的物理变化 | D.吸热的物理变化 |
①液态水汽化 ②稀释浓硫酸
③高温下碳酸钙分解 ④镁条与盐酸反应
⑤硝酸铵固体溶于水 ⑥铁丝在纯氧中燃烧
⑦氢氧化钾溶液与硝酸反应 ⑧八水合氢氧化钡固体与氯化铵固体混合搅拌
(3)下列变化:①碘的升华 ②烧碱熔化 ③氯化钠溶于水④氯化氢溶于水 ⑤氯气溶于水 ⑥氯化铵受热分解
未发生化学键破坏的是
您最近一年使用:0次
名校
7 . A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与C同主族,可形成CA型离子化合物,D是同周期元素中简单离子半径最小的元素,B与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。回答下列问题:
(1)C在元素周期表中的位置是___________ 。
(2)A分别与B、E形成的最简单化合物中沸点较高的是______ (填化学式),原因是___________ 。
(3)A、B、C三种元素形成的物质中含有的化学键类型是______ 。
(4)D单质与C的最高价氧化物对应水化物的溶液反应,反应的化学方程式为___________ 。
(5)向盛有A2B2溶液的试管中加入几滴酸化的WEB4溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(1)C在元素周期表中的位置是
(2)A分别与B、E形成的最简单化合物中沸点较高的是
(3)A、B、C三种元素形成的物质中含有的化学键类型是
(4)D单质与C的最高价氧化物对应水化物的溶液反应,反应的化学方程式为
(5)向盛有A2B2溶液的试管中加入几滴酸化的WEB4溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
解题方法
8 . 下表是元素周期表的一部分,根据表中给出10种元素,按要求作答。
(1)光导纤维的主要成分是_______ (填化学式)。
(2)形成化合物种类最多的元素_______ (填元素符号)。
(3)③、⑧、⑨的氢化物稳定性最强的是_______ (填化学式)。
(4)元素④、⑥的最高价氧化物对应的水化物之间可以相互反应,写出该反应的离子方程式___ 。
(5)元素②和⑤形成的化合物中含有_______ (填“离子键”或“共价键”)
(6)画出⑩的原子结构示意图_______ 。
(7)高温下,⑥单质与氧化铁反应的化学方程式为_______ ,该反应可用于_______ (填用途)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)形成化合物种类最多的元素
(3)③、⑧、⑨的氢化物稳定性最强的是
(4)元素④、⑥的最高价氧化物对应的水化物之间可以相互反应,写出该反应的离子方程式
(5)元素②和⑤形成的化合物中含有
(6)画出⑩的原子结构示意图
(7)高温下,⑥单质与氧化铁反应的化学方程式为
您最近一年使用:0次
2022-05-20更新
|
77次组卷
|
2卷引用:福建省三明市四地四校2021-2022学年高一下学期期中联考化学试题
解题方法
9 . 铜单质及其化合物在很多领域都有着重要用途,如金属铜可用来制造各项体育赛事的奖牌、电线、电缆,胆矾可用作杀菌剂等。试回答下列问题。
(1)已知Cu位于元素周期表第四周期第ⅠB族,则Cu原子的价电子排布式为___________ 。
(2)下列关于[Cu(NH3)4]SO4的说法中,正确的有___________
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4中含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的配体空间构型为正四面体形
D.[Cu(NH3)4]SO4的外界离子的空间构型为三角锥形
(3)向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续加入氨水,难溶物溶解并得到深蓝色的透明溶液。下列对此现象叙述正确的是___________
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后生成深蓝色的[Cu(NH3)4]2+
C.若硫酸铜溶液中混有少量硫酸,则可用氨水除去硫酸铜溶液中的硫酸
D.在[Cu(NH3)4]2+中,Cu2+提供孤电子对,NH3提供空轨道
(1)已知Cu位于元素周期表第四周期第ⅠB族,则Cu原子的价电子排布式为
(2)下列关于[Cu(NH3)4]SO4的说法中,正确的有
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]SO4中含有NH3分子,其水溶液中也含有NH3分子
C.[Cu(NH3)4]SO4的配体空间构型为正四面体形
D.[Cu(NH3)4]SO4的外界离子的空间构型为三角锥形
(3)向盛有硫酸铜溶液的试管中加入氨水,首先形成难溶物,继续加入氨水,难溶物溶解并得到深蓝色的透明溶液。下列对此现象叙述正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后生成深蓝色的[Cu(NH3)4]2+
C.若硫酸铜溶液中混有少量硫酸,则可用氨水除去硫酸铜溶液中的硫酸
D.在[Cu(NH3)4]2+中,Cu2+提供孤电子对,NH3提供空轨道
您最近一年使用:0次
名校
解题方法
10 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:____ 。
(2)D单质与C单质在加热条件下反应产物的电子式____ ,该物质与A的氧化物反应产生氧气,离子方程式为_____ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为____ 。
(4)G单质在一定条件下可以和A2C反应,方程式为_______ 。
(5)用电子式写出A2C的形成过程_______ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)G单质在一定条件下可以和A2C反应,方程式为
(5)用电子式写出A2C的形成过程
您最近一年使用:0次



