名校
1 . 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,双氧水、75%乙醇、含氯消毒剂、氯仿等均可有效灭活病毒。下列说法错误的是
| A.双氧水的消毒原理是利用其氧化性 |
| B.CH3CH2OH是共价化合物 |
| C.NaClO是含有共价键的离子化合物 |
| D.氯仿分子中的所有原子均满足8e- 稳定结构 |
您最近一年使用:0次
2022-05-06更新
|
208次组卷
|
3卷引用:四川省成都外国语学校2021-2022学年高一下学期期中考试化学试题
2 . 下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 酸性 | 非金属性 |
B |  溶于水能导电 溶于水能导电 |  是离子化合物 是离子化合物 |
C | Na在 中燃烧的生成物含离子键 中燃烧的生成物含离子键 | NaCl固体可导电 |
D | 向NaI溶液中滴入少量氯水,振荡、静置,溶液由无色变为棕黄色 |  的还原性强于 的还原性强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置为________ 。
(2)元素Y与氢元素形成离子YH 的电子式为
的电子式为______ 。
(3)下列表述中能证明元素X、元素Y非金属性强弱的是_____ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是_______ 。
(5)写出实验室制取Y的最简单氢化物的化学方程式:________ 。
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_______ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)元素Y与氢元素形成离子YH
 的电子式为
的电子式为(3)下列表述中能证明元素X、元素Y非金属性强弱的是
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是
(5)写出实验室制取Y的最简单氢化物的化学方程式:
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
您最近一年使用:0次
解题方法
4 . 硅是重要的半导体材料。近日,我国宣布突破了碳基半导体材料制备的瓶颈,有望替代目前的硅材料,支持高端芯片的国产化。

(1)Si在元素周期表中的位置是___ 。
(2)制作芯片需要高纯度的硅,高纯硅中Si原子之间的相互作用是___ (填“离子键”或“共价键”)。
(3)非金属性Si弱于P,用原子结构解释原因:___ ,得电子能力Si小于P。
(4)下列关于C和Si及其化合物的推断中,正确的是___ (填序号)。
①C的最高正化合价与Si的最高正化合价相同
②SiO2具有还原性
③最高价氧化物对应水化物的酸性:H2CO3>H2SiO3

(1)Si在元素周期表中的位置是
(2)制作芯片需要高纯度的硅,高纯硅中Si原子之间的相互作用是
(3)非金属性Si弱于P,用原子结构解释原因:
(4)下列关于C和Si及其化合物的推断中,正确的是
①C的最高正化合价与Si的最高正化合价相同
②SiO2具有还原性
③最高价氧化物对应水化物的酸性:H2CO3>H2SiO3
您最近一年使用:0次
名校
解题方法
5 . X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)X和W的元素符号分别为___ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式___ ,工业合成Y的氢化物的化学方程式为___ 。
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是___ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
6 . 在抗击新冠病毒中“84消毒液(有效成分是NaClO)”发挥了重要作用。工业上,制备“84消毒液”的原理为:NaCl+H2O NaClO+H2↑。下列说法正确的是
NaClO+H2↑。下列说法正确的是
 NaClO+H2↑。下列说法正确的是
NaClO+H2↑。下列说法正确的是| A.NaClO的消毒原理是利用了其强氧化性 |
B.NaClO的电子式为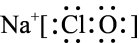 |
| C.该反应每转移1mol电子生成74.5g的NaClO |
| D.上述反应过程中有离子键、非极性共价键的断裂和形成 |
您最近一年使用:0次
7 . 随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。
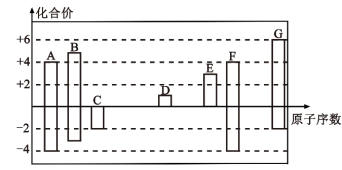
(1)G元素在周期表中的位置为___________ 。
(2)元素A与C形成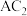 分子的电子式为
分子的电子式为____ ,B元素的单质的结构式为___________ 。
(3)A、B、F三种元素的原子半径由大到小的顺序是____ 。(填元素符号)
(4)D元素最高价氧化物的水化物所含的化学键有___________ (填化学键类型),D元素最高价氧化物的水化物与E元素的最高价氧化物的水化物反应的离子方程式是___________ 。
(5)元素C、G形成的简单气态氢化物中, 与
与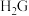 的稳定性较强的是
的稳定性较强的是___________ (填化学式)。
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷( )是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。
)是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。

(1)G元素在周期表中的位置为
(2)元素A与C形成
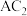 分子的电子式为
分子的电子式为(3)A、B、F三种元素的原子半径由大到小的顺序是
(4)D元素最高价氧化物的水化物所含的化学键有
(5)元素C、G形成的简单气态氢化物中,
 与
与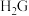 的稳定性较强的是
的稳定性较强的是(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷(
 )是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。
)是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。| A.与水反应比钠更剧烈 | B.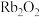 与水能剧烈反应并释放出 与水能剧烈反应并释放出 |
C.单质 具有很强的氧化性 具有很强的氧化性 | D.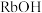 的碱性比同浓度的 的碱性比同浓度的 弱 弱 |
您最近一年使用:0次
解题方法
8 . 苯分子不能使酸性 溶液褪色的原因是
溶液褪色的原因是
 溶液褪色的原因是
溶液褪色的原因是| A.分子是平面结构 | B.分子中只存在 键 键 |
| C.苯不具有还原性 | D.分子中存在6电子大 键,结构稳定 键,结构稳定 |
您最近一年使用:0次
9 . 地康法制氯气是在催化剂作用下,通过氧气直接氧化氯化氢制备氯气:4HCl(g)+O2(g) 2Cl2(g)+H2O(g)。下列说法错误的是
2Cl2(g)+H2O(g)。下列说法错误的是
 2Cl2(g)+H2O(g)。下列说法错误的是
2Cl2(g)+H2O(g)。下列说法错误的是| A.反应中有极性键和非极性键的断裂和形成 | B.HCl水溶液显酸性,可用于除铁锈 |
| C.Cl2具有漂白性,能使品红溶液褪色 | D.Cl2具有氧化性,可与S反应制备S2Cl2 |
您最近一年使用:0次
20-21高一上·全国·课时练习
10 . 工业上最早在19世纪中叶便已生产的过氧化氢,目前成为社会需求量迅速增长的化学品,因为它有较强的氧化性,通常用于污水处理中,氧化除去水中的杂质。在过氧化氢分子中,有1个过氧键:-O-O-,每个氧原子再连接一个氢原子。纯的过氧化氢为蓝色的粘稠状液体,沸点是152.1℃,冰点是-0.89℃。
(1)过氧化氢的电子式为___________ ;
(2)过氧化氢是___________ 化合物(离子或共价);
(3)在低于-0.89℃时,过氧化氢是一种蓝色___________ 态物质,组成它的基本微粒是___________ 。
A.H2O2 B.H和O C.H2和O2 D.H和O2
(1)过氧化氢的电子式为
(2)过氧化氢是
(3)在低于-0.89℃时,过氧化氢是一种蓝色
A.H2O2 B.H和O C.H2和O2 D.H和O2
您最近一年使用:0次



