1 . 下列说法正确的是( )
| A.离子键是阴、阳离子之间的相互吸引力 |
| B.HF、HCl、HBr、HI还原性依次减弱 |
| C.第3周期非金属元素含氧酸的酸性从左到右依次减弱 |
| D.离子化合物中可能存在共价键 |
您最近一年使用:0次
2 . 2020年抗击新冠肺炎中“84消毒液(有效成分是NaClO)”发挥了重要作用。工业上,制备84消毒液的原理为NaCl + H2O NaClO +H2↑。下列说法正确的是
NaClO +H2↑。下列说法正确的是
 NaClO +H2↑。下列说法正确的是
NaClO +H2↑。下列说法正确的是| A.NaCl在通电条件下发生电离 |
| B.利用NaClO的强氧化性消毒 |
C.NaClO的电子式为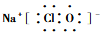 |
| D.上述反应中有两种共价化合物 |
您最近一年使用:0次
名校
3 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外电子总数与Y原子次外层的电子数相同,Y是短周期中金属性最强的元素,Z所在周期数与族序数相同,W与X属于同一主族。下列说法正确的是
| A.由X、Y组成的化合物中一定不含共价键 |
| B.X单质的氧化性比W单质的氧化性强 |
| C.Z的氧化物的水化物是强碱 |
| D.原子半径:r(W)>r(Z)>r(Y)>r(X) |
您最近一年使用:0次
2020-09-05更新
|
58次组卷
|
2卷引用:山西省大同市2021届高三上学期学情调研测试化学试题
名校
解题方法
4 . W、X、Y、Z、R是原子序数依次增大的短周期元素。a、b、c、d、e是由这些元素组成的化合物,气体a的水溶液呈碱性,c为红棕色气体,d与R的单质能发生剧烈反应,e是由W、Z、R元素形成的化合物。m为元素Z形成的单质,W与X能形成化合物XW4。上述物质的转化关系如图所示,下列说法正确的是
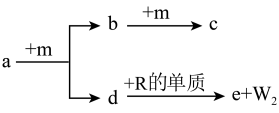

| A.简单离子半径:R>Z |
| B.最高价氧化物对应水化物的酸性:X>Y |
| C.e为离子化合物,含有离子键和共价键 |
| D.符合通式XnWn的化合物均能使溴的CCl4溶液因发生化学反应而褪色 |
您最近一年使用:0次
2021-02-19更新
|
374次组卷
|
3卷引用:(人教版2019)选择性必修2 第一章 原子结构与性质 C高考挑战区
名校
5 . 主族元素W、X、Y、Z的原子序数依次增加,且均不超过20。W、X、Y最外层电子数之和为15,Z+[Y-W≡X]-是实验室常用的化学检验试剂。下列说法中错误的是
| A.Z2Y的为共价化合物 |
| B.最简单氢化物沸点高低为:X>W |
| C.常见单质的氧化性强弱为:W<Y |
| D.[Y-W≡X]-中各原子最外层均满足8电子稳定结构 |
您最近一年使用:0次
2020-07-19更新
|
63次组卷
|
2卷引用:吉林省长春市实验中学2019-2020学年高一下学期期末考试化学试题
6 . 下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:

(1)在这些元素中,化学性质最不活泼的是______ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的化学式是______ 。
(3)最高价氧化物是两性氧化物的元素是______ ;写出它的氧化物与氢氧化钠反应的离子方程式______ 。
(4)用电子式表示元素④与⑥形成的化合物:______ ,该化合物属于______ (填“共价”或“离子”)化合物。

(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥形成的化合物:
您最近一年使用:0次
2021-04-01更新
|
179次组卷
|
4卷引用:甘肃省天水市田家炳中学2019-2020学年高一下学期期中考试化学试题
名校
7 . 下列叙述Ⅰ和Ⅱ均正确并有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 酸性HCl>H2S | 非金属性Cl>S |
| B | NH4Cl仅由非金属元素组成 | NH4Cl是共价化合物 |
| C | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| D | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙色 | Br−还原性强于Cl− |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下表是元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题.
(1)可作半导体材料的元素是 ______ (填元素符号);气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐的元素是 _____ (填名称);
(2)第三周期中离子半径最小的是___________ (填离子符号);
(3)①~⑨的最高价氧化物的水化物中:酸性最强的是__________ (填化学式);碱性最强的是________ (填化学式)。
(4)比较③、⑧最简单氢化物的稳定性:____________________ (用化学式表示)。
(5)写出②形成单质电子式________ 。
(6)⑤和⑨形成的化合物中所含化学键类型为________ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期中离子半径最小的是
(3)①~⑨的最高价氧化物的水化物中:酸性最强的是
(4)比较③、⑧最简单氢化物的稳定性:
(5)写出②形成单质电子式
(6)⑤和⑨形成的化合物中所含化学键类型为
您最近一年使用:0次
名校
9 . 为实现“双碳”目标,某科研小组设计捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
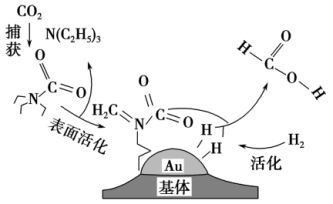

| A.标准状况下,22.4 L CO2中所含的电子数目为16NA |
| B.10.1 g N(C2H5)3中所含的非极性共价键数目为1.8NA |
| C.22 g CO2与N2O混合物中所含氧原子的数目为NA |
| D.100 g 46%的甲酸水溶液中所含的氧原子数目为5NA |
您最近一年使用:0次
2021-12-04更新
|
783次组卷
|
4卷引用:山西大学附属中学校2021-2022学年高三上学期期中考试化学试题
名校
10 . 下表是元素周期表的一部分,针对表中的①~号元素,填写下列空白:
(1)在①~0号元素中,化学性质最不活泼的是___________ (填元素符号),原子结构示意图为___________ 。元素⑩名称为___________ 。
(2)在①~⑩号元素最高价氧化物对应的水化物中,酸性最强的化合物的分子式是___________ ,碱性最强的化合物的电子式是___________ 。
(3)元素④与⑥形成的化合物属于___________ (填“共价”或“离子”)化合物。
(4)①与⑦形成的化合物的电子式为___________ ,该化合物中含有___________ (填“极性”或“非极性”)键。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是___________ (用离子符号表示)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
四 | ⑨ | ⑩ |
(1)在①~0号元素中,化学性质最不活泼的是
(2)在①~⑩号元素最高价氧化物对应的水化物中,酸性最强的化合物的分子式是
(3)元素④与⑥形成的化合物属于
(4)①与⑦形成的化合物的电子式为
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
您最近一年使用:0次
2020-09-02更新
|
323次组卷
|
4卷引用:苏教版(2020)高一必修第一册专题5第二单元 综合训练



