1 . 元素周期表体现了元素的“位一构—性”的关系,揭示了元素间的内在联系。下表列出部分元素在周期表中的位置。请回答下列问题。
(1)元素①④⑨形成的化合物中含有的化学键有 ___________ 。
(2)元素②③最高价氧化物对应水化物的酸性较强的是___________ (填化学式, 下同)。
(3)元素⑤⑧氢化物的稳定性较大的是___________ 。
(4)元素⑥⑦最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。
(5)如果发现119号元素,它应该位于周期表的位置为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ |
(2)元素②③最高价氧化物对应水化物的酸性较强的是
(3)元素⑤⑧氢化物的稳定性较大的是
(4)元素⑥⑦最高价氧化物对应的水化物之间发生反应的离子方程式为
(5)如果发现119号元素,它应该位于周期表的位置为
您最近半年使用:0次
名校
解题方法
2 . 随着原子序数的递增,7种短周期元素A~G的最高正价或最低负价与原子序数的关系如图。
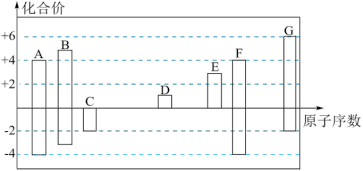
回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号_______ 。
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为_______ 。
(4)元素A与G形成的电子总数为38的分子的结构式为_______ 。
(5)元素C与D按原子个数比1:1形成的化合物的电子式为_______ ,所含有化学键类型有_______ 。
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______ 。
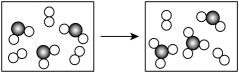

回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为
(4)元素A与G形成的电子总数为38的分子的结构式为
(5)元素C与D按原子个数比1:1形成的化合物的电子式为
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近半年使用:0次
名校
3 . 已知A、B、C、D是短周期元素的气态单质,其中A是黄绿色的气体单质,C在空气中含量最高,D是最轻的气体;E是一种最常用的金属;Y是一种常见的液态物质,Z是唯一显碱性的气体; M是一种红棕色的有毒气体;I为红褐色难溶于水的固体。有关的转化关系如下图所示(反应条件均已略去)。
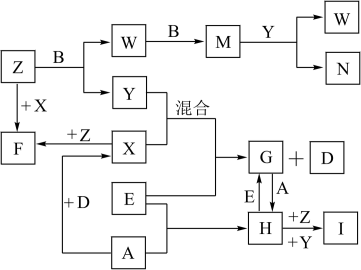
回答下列问题:
(1)A的组成元素在元素周期表的位置为____ ;
(2)F中化学键的类型是___ 、____ ;
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为_ ;
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为____ g。

回答下列问题:
(1)A的组成元素在元素周期表的位置为
(2)F中化学键的类型是
(3)Z和W在催化剂作用下反应生成C和Y,这是很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为
(4)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为
您最近半年使用:0次
名校
解题方法
4 . A、B、C、X是中学化学常见的物质,A、B、C均由短周期元素组成,转化关系如图。
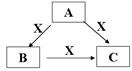
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,向C的水溶液中通入过量的CO2可得B的白色胶状沉淀。
①A中含有的金属元素为_________ (写元素名称),它在周期表中的位置为_____________ 。
②写出B → C反应的离子方程式为___________________________________ 。
(2)若A为稀HNO3,X为常见黑色金属单质,写出A→B反应的离子方程式__________ 。
(3)若A、B、C三种化合物的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是________________
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成一定物质的量浓度的溶液100mL,所用到的玻璃仪器有玻璃棒、烧杯、________ 、_________ 。
③若测得上述溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为____________ g 。

请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,向C的水溶液中通入过量的CO2可得B的白色胶状沉淀。
①A中含有的金属元素为
②写出B → C反应的离子方程式为
(2)若A为稀HNO3,X为常见黑色金属单质,写出A→B反应的离子方程式
(3)若A、B、C三种化合物的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。
①A中所含有的化学键是
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成一定物质的量浓度的溶液100mL,所用到的玻璃仪器有玻璃棒、烧杯、
③若测得上述溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为
您最近半年使用:0次
名校
解题方法
5 . 已知物质A~K之间有如下图所示转化关系。其中A是一种易溶于水的离子化合物,在空气中易潮解和变质,在水中可以电离出电子总数相等的两种离子;E为生活中常用消毒剂的有效成分,F是生活中不可缺少的调味剂,G为无色液体,B、C、D、K都是单质;反应②~⑤都是重要的工业反应。(部分反应需要在溶液中进行)
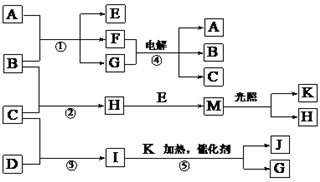
(1)物质D中所含元素在周期表中的位置为____________________________ ,
E中所含化学键类型有___________________________________________ ,
M的结构式为___________________________________________________ 。
(2)反应④的离子方程式为___________________________________________ 。
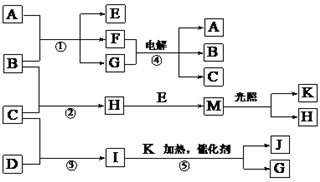
(1)物质D中所含元素在周期表中的位置为
E中所含化学键类型有
M的结构式为
(2)反应④的离子方程式为
您最近半年使用:0次
2017-10-16更新
|
196次组卷
|
2卷引用:河北省“名校联盟”(五校联考)2018届高三上学期教学质量监测(一)化学试题



