解题方法
1 . 人体必需的一些元素在周期表中的分布情况如下:
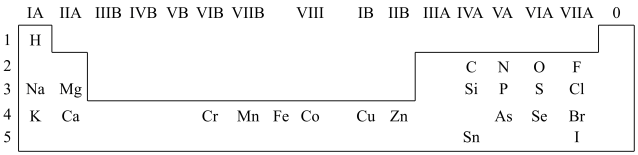
(1)请在上图中画出金属与非金属的分界线______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是______ (填字母)。
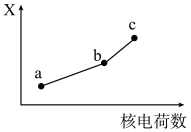
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。
(6)某小组为探究 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验②观察到的现象是______ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是______ 。试从原子结构的角度解释卤素单质的氧化性递变规律:同一主族元素从上到下,______ ,因此,元素的非金属性逐渐减弱,对应的单质的氧化性逐渐减弱。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是
| A | B | C | D |
| HCl | H₂O | CO₂ | CH₄ |
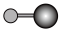 | 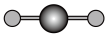 | 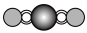 | 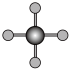 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是______(填字母)。

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)某小组为探究
 、
、 、
、 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 |  |  |
| 现象 | 溶液变为黄色 |
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,其理由是
,其理由是
您最近半年使用:0次
2 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一、元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分,列出了①~⑩10种元素在周期表中的位置。
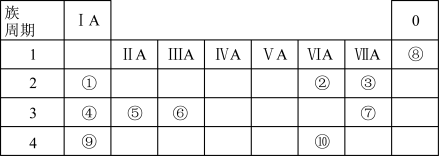
回答下列问题:
(1)①~⑩元素性质最不活泼的元素是___________ (填元素符号)。
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是___________ (填化学式),该水化物所含的化学键类型有___________ 。
(3)元素③⑥⑦的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)元素②的简单氢化物的电子式为___________ ,该氢化物常温下和元素④的单质反应的离子方程式是___________ 。
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。

回答下列问题:
(1)①~⑩元素性质最不活泼的元素是
(2)①④⑤⑥中最高价氧化物的水化物碱性最强的是
(3)元素③⑥⑦的简单离子半径由大到小的顺序是
(4)元素②的简单氢化物的电子式为
(5)元素⑩[硒(Se)]被誉为“生命元素”,科学补硒可以减少疾病的发生。铜仁市“富硒”耕地丰富,产出的“富硒”农产品受市场青睐,为“黔货出山”和“乡村振兴”作出了重要贡献。下列推断正确的是___________(填字母)。
A. 既有氧化性又有还原性 既有氧化性又有还原性 |
B. 的稳定性比 的稳定性比 强 强 |
C. 的酸性强于 的酸性强于 |
D. 在一定条件下可与NaOH溶液反应 在一定条件下可与NaOH溶液反应 |
您最近半年使用:0次
解题方法
3 . 下图为元素周期表的一部分,用化学用语回答下列问题:
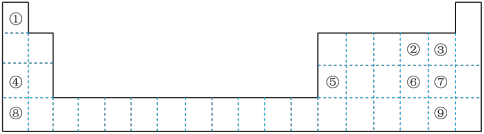
(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图___________ 。
(2)④⑤⑧的阳离子中氧化性最强的是___________ (填离子符号)。
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为___________ 。
(4)用电子式表示⑥和④形成化合物的过程___________ 。
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为___________ 。
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为___________ ,其与水反应放出气体的化学方程式为___________ 。

(1)请画出上述九种元素中非金属性最强的元素的原子结构示意图
(2)④⑤⑧的阳离子中氧化性最强的是
(3)上述元素中最高价氧化物对应的水化物中酸性最强的酸与氢氧化钠反应的化学方程式为
(4)用电子式表示⑥和④形成化合物的过程
(5)②和④形成原子个数比为1 :1的化合物中所含化学键类型为
(6)现在含有元素硒(Se)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多2个电子层,则下列叙述中正确的是___________。
| A.原子序数为34 |
| B.气态氢化物的还原性H2Se>H2S |
| C.SeO2不能与氢氧化钠反应 |
| D.SeO2既有氧化性又有还原性 |
(7)①和④可形成AB型离子化合物,该离子化合物的电子式为
您最近半年使用:0次
名校
4 . 卤族元素在性质上具有相似性与递变性。为了验证卤族部分元素递变规律,设计如图装置进行实验。请回答下列问题。
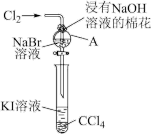
(1)A中发生反应的化学方程式是_______ 。
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是_______ 。
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应_______  填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为_______ 。
(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱_______ 。
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为_______ 。
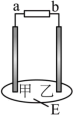
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是
(8)下图是用强光照射广口瓶中新制氯水时传感器所获得数据的图像,下列各项代表纵坐标的物理量,其中与图像不相符的是

(9)下列变化不需要破坏化学键的是

(1)A中发生反应的化学方程式是
(2)根据上述实验操作步骤,为确保“非金属性:氯>溴>碘”的实验结论可靠,你认为做好本实验最关键因素是
(3)下列性质的递变规律正确,且能作为卤族元素非金属性递变规律判断依据的是
| A.Cl-、Br-、I-的还原性逐渐增强 | B.Cl2、Br2、I2的熔点逐渐升高 |
| C.HCl、HBr、HI的酸性逐渐减弱 | D.HCl、HBr、HI的稳定性逐渐减弱 |
IBr、 ICl等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(4)氯化碘 ( ICl)能与水发生反应:ICl+H2O= HIO+ HCl,该反应
 填“是”或“不是”
填“是”或“不是” 氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为
氧化还原反应; (CN)2与NaOH水溶液反应的化学方程式为(5)从原子结构角度解释分子(CN)2中两种元素非金属性的强弱
(6)已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。在NaBr和KSCN的混合溶液中通入(CN)2,反应的离子方程式为
(7)如图所示,E是用饱和NaCl溶液和淀粉-KI溶液的混合液湿润的滤纸,用石墨做电极,通电后发现乙周围滤纸褪为蓝色,则下列判断正确的是

| A.b是阳极,a是阴极 | B.a是正极,b是负极 |
| C.乙是正极,甲是负极 | D.乙是阳极,甲是阴极 |

| A.溶液中氯离子的浓度 | B.溶液的 pH |
| C.瓶中氧气的体积分数 | D.溶液的导电能力 |
| A.液态水变为水蒸气 | B.HCl 气体溶于水 |
| C.NaHCO3 受热分解 | D.NaCl 熔化 |
您最近半年使用:0次
5 . 如图所示为元素周期表的一部分,表中每个字母分别代表一种元素。
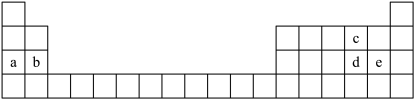
回答下列问题:
(1)d的阴离子的结构示意图为_______ 。
(2)a和c形成的原子个数比为1:1的化合物中所含化学键类型为_______ 。
(3)d和e的最高价氧化物对应水化物的酸性由强到弱的顺序_______ (用化学式表示)。
(4)为验证卤素单质氧化性的相对强弱,某同学设计了如下实验(夹持装置略)
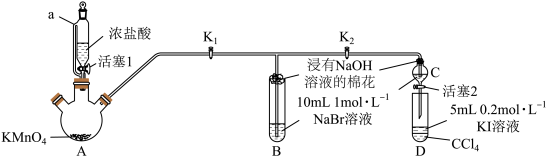
实验过程:
I.打开 、
、 ,打开活塞1,当B和C中的溶液都变为黄色时,关闭
,打开活塞1,当B和C中的溶液都变为黄色时,关闭 。
。
II.继续通气体,当B中溶液变为棕红色时,关闭活塞1。
III. ……
①装置a的名称为_______ 。
②过程I,B、C中的溶液都变黄色的原因_______ (用离子方程式表示)。
③过程II的目的是_______ 。
④过程III的目的是验证溴的氧化性强于碘。简述操作过程_______ 。

回答下列问题:
(1)d的阴离子的结构示意图为
(2)a和c形成的原子个数比为1:1的化合物中所含化学键类型为
(3)d和e的最高价氧化物对应水化物的酸性由强到弱的顺序
(4)为验证卤素单质氧化性的相对强弱,某同学设计了如下实验(夹持装置略)

实验过程:
I.打开
 、
、 ,打开活塞1,当B和C中的溶液都变为黄色时,关闭
,打开活塞1,当B和C中的溶液都变为黄色时,关闭 。
。II.继续通气体,当B中溶液变为棕红色时,关闭活塞1。
III. ……
①装置a的名称为
②过程I,B、C中的溶液都变黄色的原因
③过程II的目的是
④过程III的目的是验证溴的氧化性强于碘。简述操作过程
您最近半年使用:0次
解题方法
6 . 下表列出了①~⑩十种元素在周期表中的位置。
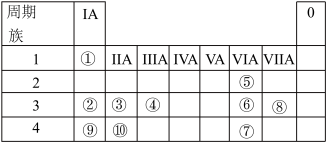
请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号___ ;元素③和⑧形成的化合物中的化学键类型为___ ,用电子式表示其形成过程___ ;元素①、⑤和⑧形成的三原子化合物的电子式为___ 。
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是___ (填化学式),碱性最强的是___ (填化学式),呈两性的氧化物与强碱反应的离子方程式为___ 。
(3)元素⑤、⑥、⑦的单质氧化性依次___ (填“增强”或“减弱”),其气态氢化物中稳定性最弱的是___ 。(均填化学式)
(4)②③④⑥⑧元素原子半径由大到小的顺序为___ ;①~⑥元素能形成10电子简单离子中半径最大的是___ 。(均用化学符号表示)

请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是
(3)元素⑤、⑥、⑦的单质氧化性依次
(4)②③④⑥⑧元素原子半径由大到小的顺序为
您最近半年使用:0次
2023高三·全国·专题练习
7 . 科学家最近研制出有望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N−N−N键角都是108.1°,下列有关N(NO2)3的说法正确的是
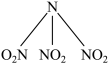

| A.分子中N、O原子间形成的共价键是非极性键 | B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 | D.分子中四个氮原子围成一个空间正四面体 |
您最近半年使用:0次
8 . 过氧化氢( )溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。
)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。 与
与 反应生成
反应生成 ,
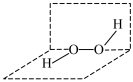
, 的分子结构如图所示。下列说法正确的是
的分子结构如图所示。下列说法正确的是
 )溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。
)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。 与
与 反应生成
反应生成 ,
, 的分子结构如图所示。下列说法正确的是
的分子结构如图所示。下列说法正确的是
A.过氧化氢的电子式为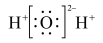 |
B. 为含有极性键和非极性键的共价化合物 为含有极性键和非极性键的共价化合物 |
C. 既有氧化性又有还原性 既有氧化性又有还原性 |
D. 与 与 反应过程中有共价键断裂,同时有共价键和离子键形成 反应过程中有共价键断裂,同时有共价键和离子键形成 |
您最近半年使用:0次
2023-07-12更新
|
124次组卷
|
2卷引用:云南省玉溪市2022-2023学年高一下学期期末考试化学试题
解题方法
9 . 科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如图。下列说法错误的是
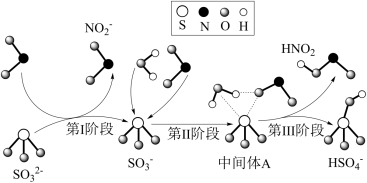

A.氧化性:NO2>SO ,还原性:SO ,还原性:SO >HNO2 >HNO2 |
B.第II、III阶段总的化学方程式为:SO +H2O+NO2=HNO2+HSO +H2O+NO2=HNO2+HSO |
| C.NO2在所有过程中都是被还原 |
| D.上述反应过程中,S的成键数目保持不变 |
您最近半年使用:0次
2022-11-20更新
|
1277次组卷
|
3卷引用:山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题
山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题(已下线)专题04 氧化还原反应及其应用 (测)-2023年高考化学二轮复习讲练测(新高考专用)山东日照市莒县一中2022-2023学年高一下学期3月月考化学试题
名校
10 . 食品添加剂可以改善食品的色香、味等品质,能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
I.磷酸氢钙CaHPO4是一种常用的营养强化剂和膨松剂,可以用于糕点、代乳品、婴幼儿配方食品等。
(1)Ca的结构示意图为_______ 。中子数为23的P,其核素符号为_______ 。
(2)下列说法中不正确的是_______。
II.短周期主族元素A、B、C、D、E、F都可能存在于某些食品添加剂中,且它们的原子序数依次增大,A的一种核素原子核内没有中子,B是地壳中含量最多的元素,C元素的原子在同周期主族元素中原子半径最大,D元素原子的最外层电子数与电子层数相等,B、E元素的原子最外层电子数相同。请回答下列问题:
(3)E元素在元素周期表中的位置为_______ 。
(4)由A、B、F三种元素组成的简单化合物的电子式为_______ 。
(5)B单质与C单质在加热条件下反应,所得产物中存在的化学键类型为_______ 。
(6)B、C、D对应简单离子的半径由小到大的顺序为_______ (用具体微粒符号表示)。
(7)D元素最高价氧化物与C元素最高价氧化物对应水化物的溶液反应的离子方程式为_______ 。
I.磷酸氢钙CaHPO4是一种常用的营养强化剂和膨松剂,可以用于糕点、代乳品、婴幼儿配方食品等。
(1)Ca的结构示意图为
(2)下列说法中不正确的是_______。
| A.热稳定性; H2O> NH3> PH3 | B.碱性: KOH >Ca(OH)2>Al(OH)3 |
| C.酸性: H3PO4>H2SiO3> H2CO3 | D.还原性: O2-<S2-<P3- |
II.短周期主族元素A、B、C、D、E、F都可能存在于某些食品添加剂中,且它们的原子序数依次增大,A的一种核素原子核内没有中子,B是地壳中含量最多的元素,C元素的原子在同周期主族元素中原子半径最大,D元素原子的最外层电子数与电子层数相等,B、E元素的原子最外层电子数相同。请回答下列问题:
(3)E元素在元素周期表中的位置为
(4)由A、B、F三种元素组成的简单化合物的电子式为
(5)B单质与C单质在加热条件下反应,所得产物中存在的化学键类型为
(6)B、C、D对应简单离子的半径由小到大的顺序为
(7)D元素最高价氧化物与C元素最高价氧化物对应水化物的溶液反应的离子方程式为
您最近半年使用:0次



