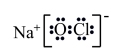名校
1 . W、X、Y、Z、Q为原子半径依次增大的短周期主族元素,X的原子序数等于W与Y的原子序数之和,Z的原子半径是第三周期中最小的,W与X形成的物质可用来杀菌消毒且该物质的分子中含18e-,Q原子最外层电子数为X原子最外层电子数的一半。下列说法不正确的是
| A.X元素与Q元素组成的化合物可做耐火材料 |
| B.由W、X、Y三种元素所组成化合物的水溶液可能显酸性也可能显碱性 |
| C.简单氢化物的沸点:X>Y>Z |
| D.由Z和Q形成的化合物中存在离子键 |
您最近一年使用:0次
2022-04-02更新
|
820次组卷
|
6卷引用:四川省成都市第七中学2021-2022学年高三下学期第七次测试理综化学试题
四川省成都市第七中学2021-2022学年高三下学期第七次测试理综化学试题(已下线)专项08 物质结构 元素周期律-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)四川省南充市白塔中学2021-2022学年高一下学期第四次月考化学试题四川省乐山沫若中学2022-2023学年高二上学期第二次月考(期中考试)化学试题(已下线)第一部分 二轮专题突破 专题9 “位—构—性”综合推断四川省内江市第六中学2023-2024学年高三上学期入学考试化学试题
解题方法
2 . 如图是元素周期表的一部分,表中的每个序号代表一种短周期元素,用相应的元素符号或化学式填空回答下列问题:
(1)元素①和③可以组成最简单的有机物,其化学式为____ 。
(2)元素⑤组成的两种常见的同素异形体是____ 。
(3)在这些元素中,化学性质最不活泼的元素是____ 。
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是____ ,碱性最强的是____ ,呈两性的氢氧化物是____ 。
(5)元素⑦和⑩可组成阴、阳离子个数比为1:1的化合物,化学式为____ 。
(6)上述元素中,非金属性最强的是____ ,金属性最强的是____ 。
(7)元素④和⑦分别形成的最高价氧化物水化物之间发生反应生成的盐的化学键类型为____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | ② | ||||||
| 二 | ③ | ④ | ⑤ | ⑥ | ||||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑤组成的两种常见的同素异形体是
(3)在这些元素中,化学性质最不活泼的元素是
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(5)元素⑦和⑩可组成阴、阳离子个数比为1:1的化合物,化学式为
(6)上述元素中,非金属性最强的是
(7)元素④和⑦分别形成的最高价氧化物水化物之间发生反应生成的盐的化学键类型为
您最近一年使用:0次
2021·全国·模拟预测
3 . 下表中相关物质的信息都正确的一项是
选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
A | NaClO |
| 强氧化性 | 消毒液 |
B | H2O2 |
| 不稳定,易分解 | 医用消毒剂 |
C | NH3 | 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
D | KAl(SO4)2 | 离子键 | 易水解 | 净水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . A、B、C、D、E是五种短周期主族元素,它们的原子序数依次增大。已知:A的一种原子不含中子;B原子最外层电子数是次外层的3倍;C与A处于同一主族;D的原子序数是B的2倍。下列叙述正确的是
| A.在B、D、E形成的简单离子中,E离子的还原性最强 |
| B.1 mol E的单质与C最高价氧化物对应水化物的溶液完全反应时,转移2 mol电子 |
| C.最高价氧化物对应水化物的酸性:D > E |
| D.B与C形成的化合物中一定含有离子键,也可能含有共价键 |
您最近一年使用:0次
2021-05-23更新
|
72次组卷
|
2卷引用:河南省宏力学校2018-2019学年高二下学期期中考试化学试题
名校
5 . 已知由一种阳离子与两种酸根阴离子组成的盐称为混盐。向混盐 中加入足量浓硫酸,发生反应:
中加入足量浓硫酸,发生反应: 。下列说法错误的是
。下列说法错误的是
 中加入足量浓硫酸,发生反应:
中加入足量浓硫酸,发生反应: 。下列说法错误的是
。下列说法错误的是A. 中的两种酸根阴离子分别为 中的两种酸根阴离子分别为 和 和 |
B. 中不含非极性共价键 中不含非极性共价键 |
| C.在上述反应中,浓硫酸不体现氧化性 |
D.每产生0.1mol ,转移电子的数目约为 ,转移电子的数目约为 |
您最近一年使用:0次
2021-10-11更新
|
288次组卷
|
4卷引用:山东省潍坊市2022届高三10月份阶段性检测化学试题
名校
解题方法
6 . 利用如下实验研究浓硫酸的性质。
实验1:表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,观察到胆矾变成白色。
实验2:取2 g蔗糖放入大管中,加2~3滴水,再加入3 mL浓硫酸,搅拌。将产生的气体导入品红溶液中,观察到品红溶液褪色。
实验3:将一小片铜放入试管中,再加入3 mL浓硫酸,加热,观察到铜片上有黑色物质产生。
下列说法不正确的是
实验1:表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,观察到胆矾变成白色。
实验2:取2 g蔗糖放入大管中,加2~3滴水,再加入3 mL浓硫酸,搅拌。将产生的气体导入品红溶液中,观察到品红溶液褪色。
实验3:将一小片铜放入试管中,再加入3 mL浓硫酸,加热,观察到铜片上有黑色物质产生。
下列说法不正确的是
| A.胆矾化学式可表示为Cu(H2O)4SO4·H2O,说明胆矾晶体中存在离子键、共价键、配位键和氢键等作用力 |
| B.“实验2”可以说明浓硫酸具有脱水性和强氧化性 |
| C.“实验3”中黑色物质可能是氧化铜 |
| D.在“实验3”中的残留物中直接加入适量水,观察溶液是否变蓝色 |
您最近一年使用:0次
2021-05-31更新
|
1444次组卷
|
5卷引用:江苏省南京师范大学附属中学2021届高三5月模拟考试化学试题
江苏省南京师范大学附属中学2021届高三5月模拟考试化学试题(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省南通市通州区金沙中学2021-2022学年高一下学期6月质量调研测试化学试题江苏省淮安市二校楚州中学新马中学2023-2024学年高三上学期10月化学试卷
7 . 下列能用键能大小解释的是
| A.液态水的密度大于冰的密度 | B.碘单质和干冰容易升华 |
| C.氧气的氧化性不如氯气的氧化性 | D.溴容易溶于四氯化碳 |
您最近一年使用:0次
名校
8 . 短周期主族元素X、Y、Z、W的原子序数依次增加,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法不正确的是( )

| A.Y、Z、W三种元素电负性:W>Z>Y |
| B.Y、Z、W三种元素的第一电离能:W>Z>Y |
| C.Y、Z、W与氢元素均可形成含非极性键的二元化合物 |
| D.由X、Y、Z、W构成的化合物中可能含有离子键 |
您最近一年使用:0次
2020-11-25更新
|
488次组卷
|
5卷引用:山东省济南市第一中学2021届高三上学期期中考试化学试题
解题方法
9 . 为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。几种主族元素在周期表中的位置如图:

根据上表回答下列问题:
(1)⑥元素的氢化物是______ (填化学式)。
(2)③④⑦三种元素简单离子半径由大到小的顺序是______ (用离子符号表示)。
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是______ ,用电子式表示该化合物的形成过程______ 。
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是______ ,最高价氧化物对应水化物酸性最强的化合物的化学式是______ 。
(5)写出②与水反应的离子方程式为______ 。
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是______ (填字母,下同)。
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是______ 。


根据上表回答下列问题:
(1)⑥元素的氢化物是
(2)③④⑦三种元素简单离子半径由大到小的顺序是
(3)③⑦两种元素形成的离子化合物中含有的化学键类型是
(4)表中元素,最高价氧化物对应水化物碱性最强的化合物的化学式是
(5)写出②与水反应的离子方程式为
(6)下列表述中能证明⑦的非金属性强于⑧这一事实的是
a.氢化物稳定性:⑦>⑧
b.最高价氧化物对应的水化物的酸性:⑦>⑧
c.⑦的单质能将⑧从其钠盐溶液中置换出来
(7)①与⑤元素形成的分子可能是

您最近一年使用:0次
10 . 下表列出了①~⑦种元素在周期表中的位置:
请回答下列问题。
(1)①~⑦中非金属性最强的是______ (填元素符号)。
(2)③⑤⑥形成的简单离子,其离子半径由大到小的顺序为______ (填离子符号)。
(3)④的最高价氧化物属于______ (填“酸性”、“碱性”或“两性”)氧化物;写出该氧化物与稀硫酸反应的离子方程式______ 。
(4)②的最低价氢化物的结构式为______ 。
(5)①和⑥的单质加热生成的化合物中,含有的化学键类型为______ 。
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ⑤ | ⑥ | ⑦ | |||
| 3 | ① | ③ | ④ | ||||
(1)①~⑦中非金属性最强的是
(2)③⑤⑥形成的简单离子,其离子半径由大到小的顺序为
(3)④的最高价氧化物属于
(4)②的最低价氢化物的结构式为
(5)①和⑥的单质加热生成的化合物中,含有的化学键类型为
您最近一年使用:0次