解题方法
1 . 科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如图。下列说法错误的是
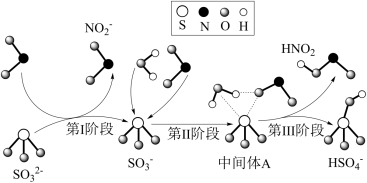

A.氧化性:NO2>SO ,还原性:SO ,还原性:SO >HNO2 >HNO2 |
B.第II、III阶段总的化学方程式为:SO +H2O+NO2=HNO2+HSO +H2O+NO2=HNO2+HSO |
| C.NO2在所有过程中都是被还原 |
| D.上述反应过程中,S的成键数目保持不变 |
您最近一年使用:0次
2022-11-20更新
|
1296次组卷
|
3卷引用:山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题
山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题山东日照市莒县一中2022-2023学年高一下学期3月月考化学试题(已下线)专题04 氧化还原反应及其应用 (测)-2023年高考化学二轮复习讲练测(新高考专用)
名校
2 . 下列叙述正确的是
| A.由分子构成的物质内部都存在范德华力,但可能不存在共价键 |
| B.阳离子只有氧化性,阴离子只有还原性 |
| C.金属与盐溶液之间只能发生置换反应 |
| D.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
您最近一年使用:0次
解题方法
3 . 元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是5种短周期主族元素的相关信息。
回答下列问题:
(1)X在元素周期表中的位置为______ 。
(2)由Y与Z形成的一种化合物可作供氧剂,该化合物中所含化学键的类型为______ 。
(3)Y、Z、Q的简单离子半径由大到小的顺序为______ (用离子符号表示)。
(4)常温下,将W的单质通入Z的最高价氧化物的水化物的溶液中,可以得到消毒液,该反应的化学方程式为______ 。
(5)研究W、Q非金属性强弱的方案中不可行的是______ (填序号)。
a.比较其简单氢化物的沸点 b.比较其单质与氢气反应的难易程度
c.比较其简单阴离子的还原性 d.比较其氧化物的水化物的酸性
| 元素 | 信息 |
| X | 其中一种核素在考古时常用来测定文物的年代 |
| Y | 最外层电子数是次外层电子数的3倍 |
| Z | 短周期主族元素中,其原子半径最大 |
| W | 常温下,其单质是一种黄绿色的气体 |
| Q | 最高化合价与最低化合价的代数和为4 |
(1)X在元素周期表中的位置为
(2)由Y与Z形成的一种化合物可作供氧剂,该化合物中所含化学键的类型为
(3)Y、Z、Q的简单离子半径由大到小的顺序为
(4)常温下,将W的单质通入Z的最高价氧化物的水化物的溶液中,可以得到消毒液,该反应的化学方程式为
(5)研究W、Q非金属性强弱的方案中不可行的是
a.比较其简单氢化物的沸点 b.比较其单质与氢气反应的难易程度
c.比较其简单阴离子的还原性 d.比较其氧化物的水化物的酸性
您最近一年使用:0次
2021-02-02更新
|
292次组卷
|
2卷引用:四川省宜宾市2022-2023学年高一上学期第三次月考化学试题
4 . X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最处层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为_______ 、__________ 、_______ 。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有_________ 、_______ 。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是_______ 。
此化合物在酸性条件下与高锰酸钾反应的离子方程式为________________________ ;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为__________________________ 。
(1)X、Y和Z的元素符号分别为
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是
此化合物在酸性条件下与高锰酸钾反应的离子方程式为
您最近一年使用:0次
2019-01-30更新
|
1603次组卷
|
7卷引用:2016-2017学年山西省山西大学附属中学高一3月月考化学试卷
名校
5 . 表中相关物质的信息都正确的一项是
| 选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
| A |  | 离子键、共价键 | 强氧化性 | 消毒液 |
| B |  | 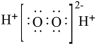 | 不稳定,易分解 | 医用消毒剂 |
| C | W(钨) | 金属键 | 银白色,具有金属光泽 | 制成灯丝 |
| D |  | 离子键 | 受热易分解 | 治疗胃酸过多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物结构如图所示。下列叙述不正确的是
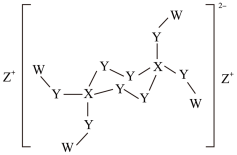

| A.简单离子半径:Y>Z |
| B.该化合物具有强氧化性,可杀菌消毒 |
C.X的最高价氧化物的水化物分子式为 |
| D.该化合物中既含有离子键,又含有极性共价键和非极性共价键 |
您最近一年使用:0次
名校
解题方法
7 . 一种由四种短周期元素组成的化合物(如图所示),具有极强的氧化性。其中元素X、Y、Z、W的原子序数依次增大,且原子序数之和为36。下列有关叙述错误的是
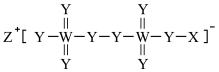
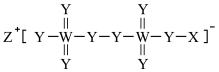
| A.该物质中含有离子键、极性共价键和非极性共价键 |
| B.工业上采用电解法制备单质Z |
| C.该物质中W的化合价为+7,可用于消毒杀菌 |
| D.原子半径的大小顺序是Z>W>Y>X |
您最近一年使用:0次
名校
8 . W、X、Y、Z是原子序数依次增大的短周期主族元素,且原子序数总和为25,Y是地壳中含量最多的元素,由这四种元素形成的某化合物结构如图所示。下列叙述正确的是


A.简单离子半径: |
| B.该化合物具有强氧化性,可杀菌消毒 |
| C.该化合物中W、X、Y、Z最外层均达到8电子稳定结构 |
| D.W分别与X、Y、Z形成的化合物所含化学键类型相同 |
您最近一年使用:0次
2022-01-24更新
|
581次组卷
|
6卷引用:四川省成都市实验中学2021-2022学年高三下学期2月月考理科综合化学试题
四川省成都市实验中学2021-2022学年高三下学期2月月考理科综合化学试题 湖南省祁阳市第一中学2023届高三第五次月考化学试题湖南省衡阳市第八中学2023届高三第五次月考化学试题湖南省邵阳市第一中学2023届高三第五次月考化学试题安徽省合肥市2022届高三上学期第一次教学质量检测化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)
名校
解题方法
9 . 下表为元素周期表的一部分,请回答有关问题:
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为_________
(2)由元素②和④形成的三核直线形分子的结构式为_________
(3)用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程_______________
(4)由上述元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为______ (填“离子键”、“极性键”或“非极性键”)④和⑦的氢化物稳定性较强的是__________ 、沸点较高的是_________ (填化学式)⑧和⑩的氢化物还原性较强的是_______ (填化学式)
(5)元素⑦、⑧、⑨的离子半径由大到小的顺序是_________ (用离子符号表示);元素⑨的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为__________
(6)能比较元素⑦和⑧非金属性强弱的实验事实是_________ (填字母序号)。
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素②和④形成的三核直线形分子的结构式为
(3)用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程
(4)由上述元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为
(5)元素⑦、⑧、⑨的离子半径由大到小的顺序是
(6)能比较元素⑦和⑧非金属性强弱的实验事实是
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
您最近一年使用:0次
名校
10 . A、X、Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题:
(1)Y元素的名称是___________ ,W在周期表中的位置是___________ 。
(2)写出化合物AZX的结构式:___________ ;化合物R2X2存在的化学键类型是___________ 。
(3)X、Z、R三种元素对应的简单离子半径由大到小大小:___________ (用离子符号表示)。
(4)下列事实能证明非金属性Z比Y强的是___________ (填序号)。
a.简单阴离子还原性Z>Y
b.简单氢化物热稳定性:Z>Y
c.氧化物对应的水化物酸性:Z>Y
d.Y的简单氢化物的水溶液中通入Z的单质有沉淀析出
(5)写出实验室制备Z的单质的离子方程式:___________ 。
(6)用电子式表示RZ的形成过程:___________ 。
(1)Y元素的名称是
(2)写出化合物AZX的结构式:
(3)X、Z、R三种元素对应的简单离子半径由大到小大小:
(4)下列事实能证明非金属性Z比Y强的是
a.简单阴离子还原性Z>Y
b.简单氢化物热稳定性:Z>Y
c.氧化物对应的水化物酸性:Z>Y
d.Y的简单氢化物的水溶液中通入Z的单质有沉淀析出
(5)写出实验室制备Z的单质的离子方程式:
(6)用电子式表示RZ的形成过程:
您最近一年使用:0次
2020-12-11更新
|
333次组卷
|
5卷引用:辽宁省开原市第二高级中学2021届高三第三次模拟考试化学试题



