名校
解题方法
1 . A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1) D元素在周期表中的位置是___________ ,乙物质的电子式是___________ 。
(2) A、B、C、D、E五种元素的原子半径由小到大的顺序是_________ (用元素符号填写)。
(3) E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是:____________________________ 。
(4)简述比较D与E金属性强弱的实验方法:_________________________ 。
(1) D元素在周期表中的位置是
(2) A、B、C、D、E五种元素的原子半径由小到大的顺序是
(3) E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是:
(4)简述比较D与E金属性强弱的实验方法:
您最近一年使用:0次
2020-07-03更新
|
103次组卷
|
3卷引用:湖南省张家界市民族中学2019-2020学年高一下学期第二次月考化学试题
2 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____ 方法区分晶体、准晶体和非晶体。
(2)基态锑(Sb)原子价电子排布的轨道式为____ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______ 、_________ 。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____ (填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____ 。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______ (填序号):
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
(4)某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=____ g/cm3。

(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过
(2)基态锑(Sb)原子价电子排布的轨道式为
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
(4)某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=

您最近一年使用:0次
2019-12-05更新
|
210次组卷
|
3卷引用:湖南省汨罗市2021届高三9月检测考试化学试题
名校
解题方法
3 . A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18,A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍。A、B、C三种元素能结合成化合物C2AB3,在lmolC2AB3中共有52mol电子。D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移。E元素的单质是一种黄绿色气体,水溶液具有漂白性。试填写下列空白:
(1)写出元素A 和E的名称:A_______ ,E_______ 。
(2)元素B在周期表中的位置为第二周期_______ 族。
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有_______ 键(填“极性”或“非极性”)的_______ 化合物(填“离子”或“共价”) ,写出该化合物的电子式_______ 。
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式_______ 。
(1)写出元素A 和E的名称:A
(2)元素B在周期表中的位置为第二周期
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
595次组卷
|
4卷引用:2016-2017学年湖南省株洲市第二中学高一下学期第一次月考化学试卷
2016-2017学年湖南省株洲市第二中学高一下学期第一次月考化学试卷2015-2016学年江苏省泰州中学高一下第一次月考化学试卷《课时同步君》2017-2018学年高一化学人教必修2-1.3 化学键(已下线)精做03 化学键——《大题精做》2017-2018学年高一化学人教必修2
名校
解题方法
4 . A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:
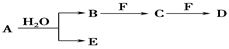
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:_________________ 。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________________ ;D中所含化学键的类型为____________________ 。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:_________________ 。
(3)若A中一种元素原子的最外层电子数为内层电子总数的 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____________ ;B转化为C的化学方程式为______________ 。

(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:
(3)若A中一种元素原子的最外层电子数为内层电子总数的
 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
您最近一年使用:0次
2016-12-09更新
|
789次组卷
|
2卷引用:湖南省长沙市第一中学2020届高三第五次月考化学试题
10-11高三上·湖南衡阳·阶段练习
解题方法
5 . 如下图所示:在上述转化关系中,已知B、D都是淡黄色固体,且A与D可反应生成离子化合物A2D。回答:

(1)写出下列物质的化学式A._______ ,H._______ 。
(2)写出C的电子式_______ ,B中含有的化学键类型是____________
(3)写出E→F的化学方程式___________________ 。

(1)写出下列物质的化学式A.
(2)写出C的电子式
(3)写出E→F的化学方程式
您最近一年使用:0次



