名校
解题方法
1 . 根据元素周期表和元素周期律判断,下列叙述不正确 的是
| A.氢元素与其他元素既可形成共价化合物也可形成离子化合物 |
| B.气态氢化物的稳定性:H2O > NH3 > SiH4 |
C.用中文“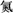 ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族 |
D.下图所示实验可证明元素的非金属性:Cl > C > Si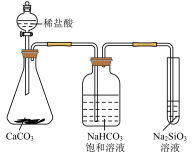 |
您最近一年使用:0次
2020-11-03更新
|
601次组卷
|
6卷引用:山东省济南市山东师范大学附属中学2019-2020学年高一下学期5月学业水平检测化学试题
山东省济南市山东师范大学附属中学2019-2020学年高一下学期5月学业水平检测化学试题(已下线)第16单元 物质的结构与性质(选考)(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)第4章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)黑龙江省大庆铁人中学2020-2021学年高一下学期开学考试化学试题安徽省蚌埠田家炳中学2020-2021学年高一4月月考化学试题辽宁省朝阳市建平县实验中学2021-2022学年高一下学期第一次月考化学试题
名校
2 . A、X、Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题:
(1)Y元素的名称是___________ ,W在周期表中的位置是___________ 。
(2)写出化合物AZX的结构式:___________ ;化合物R2X2存在的化学键类型是___________ 。
(3)X、Z、R三种元素对应的简单离子半径由大到小大小:___________ (用离子符号表示)。
(4)下列事实能证明非金属性Z比Y强的是___________ (填序号)。
a.简单阴离子还原性Z>Y
b.简单氢化物热稳定性:Z>Y
c.氧化物对应的水化物酸性:Z>Y
d.Y的简单氢化物的水溶液中通入Z的单质有沉淀析出
(5)写出实验室制备Z的单质的离子方程式:___________ 。
(6)用电子式表示RZ的形成过程:___________ 。
(1)Y元素的名称是
(2)写出化合物AZX的结构式:
(3)X、Z、R三种元素对应的简单离子半径由大到小大小:
(4)下列事实能证明非金属性Z比Y强的是
a.简单阴离子还原性Z>Y
b.简单氢化物热稳定性:Z>Y
c.氧化物对应的水化物酸性:Z>Y
d.Y的简单氢化物的水溶液中通入Z的单质有沉淀析出
(5)写出实验室制备Z的单质的离子方程式:
(6)用电子式表示RZ的形成过程:
您最近一年使用:0次
2020-12-11更新
|
333次组卷
|
5卷引用:四川省江油中学2021届高三上学期开学考试理综化学试题
3 . 现有部分元素的性质与原子(或分子)结构如下表:
请根据表中信息回答下列问题
(1)元素T在周期表中位于第_____ 周期第_____ 族
(2)元素T与X相比,原子半径较大的是________ (用元素符号表示);
(3)T、X、Y、Z中有两种元素能形成既有离子键又有共价键的化合物,
该化合物的电子式为_________ 该化合物与水反应方程式:_____________________
(4)元素Y与元素Z相比,金属性较强的是________ (用元素符号表示);
下列表述中能证明这一事实的是________ (填序号)。
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(5)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:____________________________________________ 。
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的简单离子中半径最小 |
(1)元素T在周期表中位于第
(2)元素T与X相比,原子半径较大的是
(3)T、X、Y、Z中有两种元素能形成既有离子键又有共价键的化合物,
该化合物的电子式为
(4)元素Y与元素Z相比,金属性较强的是
下列表述中能证明这一事实的是
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(5)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . Ⅰ.下面是同学们熟悉的物质:
①O2 ②H2SO4 ③NaBr ④NH4Cl ⑤NaHSO4 ⑥Ne ⑦Na2O2 ⑧NaOH
(1)这些物质中,既含有共价键又含有离子键的是_________ ;不存在化学键的是____ 。(填序号)
(2)属于共价化合物的是________ ;属于离子化合物的是________ 。(填序号)
(3)将NaHSO4固体溶于水,破坏了NaHSO4中的_______ (填化学键类型),NaHSO4在熔融状态下电离,破坏了NaHSO4中的________ (填化学键类型)。
Ⅱ.氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×105Pa),但在180℃就开始升华。据此判断,氯化铝是___________ (填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是__________________ 。
①O2 ②H2SO4 ③NaBr ④NH4Cl ⑤NaHSO4 ⑥Ne ⑦Na2O2 ⑧NaOH
(1)这些物质中,既含有共价键又含有离子键的是
(2)属于共价化合物的是
(3)将NaHSO4固体溶于水,破坏了NaHSO4中的
Ⅱ.氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×105Pa),但在180℃就开始升华。据此判断,氯化铝是
您最近一年使用:0次
2014高三·全国·专题练习
5 . 四种短周期元素在周期表中的位置如图,其中只有M为金属元素。
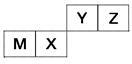
请回答下列问题:
(1)这些元素的氢化物中,水溶液碱性最强的是______ (写化学式),该氢化物的电子式为______ 。
(2)元素X和元素Y的最高价氧化物对应水化物的酸性较弱的是______ ,列举一个化学方程式证明______ 。
(3)元素Z与元素M组成的化合物中所含化学键类型为______ ,元素Z与元素X组成的化合物中所含化学键类型为______ 。

请回答下列问题:
(1)这些元素的氢化物中,水溶液碱性最强的是
(2)元素X和元素Y的最高价氧化物对应水化物的酸性较弱的是
(3)元素Z与元素M组成的化合物中所含化学键类型为
您最近一年使用:0次
名校
解题方法
6 . 2019年,人们首次在太空探测到分子阳离子HeH+。关于HeH+说法正确的是
| A.与3He具有相同的质子数 | B.与3He具有相同的电子数 |
| C.与LiH具有相同化合价的氢元素 | D.与LiH具有相同的化学键 |
您最近一年使用:0次
2021-10-24更新
|
115次组卷
|
2卷引用:上海市晋元高级中学2020-2021学年高三上学期期中考试(等级考)化学试题
名校
解题方法
7 . 海洋生物参与氮循环过程如图所示:

下列说法不正确 的是

下列说法
| A.反应①~⑤中包含3个氧化还原反应 |
| B.反应②中有极性键断裂和非极性键生成 |
| C.反应③中可能有氧气参与反应 |
D.等量 参加反应,反应④转移电子数目比反应⑤多 参加反应,反应④转移电子数目比反应⑤多 |
您最近一年使用:0次
2020-12-15更新
|
423次组卷
|
6卷引用:北京市朝阳区2021届高三上学期期中质量检测化学试题
解题方法
8 . X、Y、Z、M、W为五种原子序数递增的前20号元素。X、Y是同周期元素,原子序数相差2,族序数之和为10;Z原子最外层电子数等于其最内层电子数,M在地壳中含量居第二位;W的某种盐常用作加碘盐的碘制剂。下列说法错误的是
| A.原子半径:W>Z>M>X>Y |
| B.最高价氧化物对应的水化物的酸性:X>M |
| C.ZXY3含离子键和共价键,0.1molW2Y2含有0.4mol离子 |
| D.Z与XY2反应可置换出X单质,X与MY2反应可置换出M单质 |
您最近一年使用:0次
9 . 普伐他汀是一种调节血脂的药物其结构如图所示。下列有关该有机物的说法正确的是
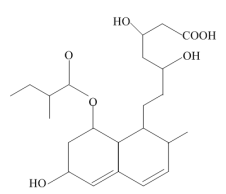

| A.其熔点主要取决于所含化学键的键能 |
| B.分子中碳原子的杂化方式有sp2、sp3杂化 |
| C.分子中存在的化学键有σ键、π键和氢键 |
| D.分子中所含元素的基态原子的第一电离能大小顺序为C>O>H |
您最近一年使用:0次
名校
解题方法
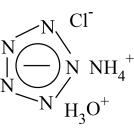
10 . 全氮阴离子盐是一种新型超高能含能材料,全氮阴离子化学式为N ,某种全氮阴离子盐结构如图。下列有关说法正确的是
,某种全氮阴离子盐结构如图。下列有关说法正确的是
 ,某种全氮阴离子盐结构如图。下列有关说法正确的是
,某种全氮阴离子盐结构如图。下列有关说法正确的是
| A.该全氮阴离子盐属于有机物 |
B.N 的摩尔质量为71g/mol 的摩尔质量为71g/mol |
C.每个 N 含有26个电子 含有26个电子 |
| D.该全氮阴离子盐既含共价键又含离子键 |
您最近一年使用:0次



