1 . 回答下列问题
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为___________ ,电负性O___________ F;其中氧原子的杂化方式为___________ 。
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。 空间结构是
空间结构是___________ ;X与Z形成化合物中含有的化学键是___________ 。
(3) 的空间结构为
的空间结构为___________ 。(用文字描述,下同): 的空间结构是
的空间结构是___________ 。
(4)在BF3分子中: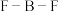 的键角是
的键角是___________ ,B原子的杂化轨道类型为___________ ,BF3和过量NaF作用可生成NaBF4, 的空间结构为
的空间结构为___________ 。
(5)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为___________ ;其中π键与σ键的个数比为___________ 。
(7)基态S原子价电子排布式___________ ;S原子的核外电子运动状态有___________ 种,空间运动状态有___________ 种:能量最高的轨道的电子云的形状是___________ 。
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。
 空间结构是
空间结构是(3)
 的空间结构为
的空间结构为 的空间结构是
的空间结构是(4)在BF3分子中:
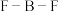 的键角是
的键角是 的空间结构为
的空间结构为(5)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为
(7)基态S原子价电子排布式
您最近半年使用:0次
2024-02-22更新
|
212次组卷
|
2卷引用:天津市耀华中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 下列图示错误的是
A.2px的电子云: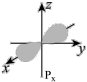 | B.金刚石晶体结构模型: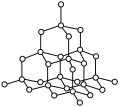 |
C.HCl形成过程: | D. 球棍模型: 球棍模型: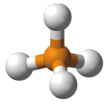 |
您最近半年使用:0次
名校
解题方法
3 . 下表是A、B、C、D、E五种短周期元素的某些性质,下列判断正确的是( )
| 元素 | A | B | C | D | E |
| 最低化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 4.0 |
| A.C、D、E的简单氢化物的稳定性:C>D>E |
| B.元素A的原子最外层中无自旋状态相同的电子 |
| C.元素B、C之间不可能形成化合物 |
D.与元素B同周期且在该周期中第一电离能最小的元素的单质能与 发生置换反应 发生置换反应 |
您最近半年使用:0次
2020-04-09更新
|
777次组卷
|
25卷引用:天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题
天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题2016-2017学年安徽省六安市第一中学高二下学期第一次阶段检测化学试卷宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题(已下线)专题11.1 原子结构与性质(练)-《2020年高考一轮复习讲练测》宁夏回族自治区吴忠市青铜峡市高级中学2019-2020学年高二上学期期末考试化学试题云南省开远市第二中学校2019-2020学年高二上学期期末考试化学试题人教化学选修3第一章第二节课时4人教化学选修3第一章第二节课时5第1章 原子结构——B拓展区综合拓展(鲁科版选修3)山东省济南市章丘区第四中学2019-2020学年高二下学期第六次教学质量检测化学试题(已下线)练习18 原子结构与元素的性质-2020-2021学年【补习教材·寒假作业】高二化学(人教版)鲁科版2019选择性必修2第1章 原子结构与元素性质 微项目 甲醛的危害与去除——利用电负性分析与预测物质性质(人教版2019)选择性必修2 第一章 原子结构与性质 B素养拓展区(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)宁夏吴忠市吴忠中学2020-2021学年高二3月月考化学试题河北省衡水市武强中学2020-2021学年高二下学期第一次月考化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二下学期5月月考化学试题河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题辽宁省沈阳市重点高中联合体2021-2022学年高二12月考试化学试题(已下线)1.2.3 元素的电负性及其变化规律-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)1.2.2 原子结构与元素周期律(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第1章 章末综合测评A-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)重庆市育才中学2021-2022学年上学期高二上学期第六次定时练习化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
4 . 下列叙述正确的是( )
| A.电负性的大小可以作为判断元素金属性和非金属性强弱的尺度 |
| B.在同一电子层上运动的电子,其自旋方向肯定不同 |
| C.镁原子的核外电子排布由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| D.基态原子价层电子排布是5s1的元素,其氢氧化物的溶液一定不能溶解氢氧化铝 |
您最近半年使用:0次
2020-03-26更新
|
155次组卷
|
6卷引用:天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题
名校
5 . 下列叙述正确的是( )
| A.可能存在基态核外电子排布式为1s22s22p63s23p64s24p1的原子 |
| B.当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相反 |
| C.1个原子轨道里最多容纳2个电子,且自旋方向相同 |
| D.基态原子的电子获得一定能量变为激发态原子,而激发态原子变为基态原子,则要放出能量 |
您最近半年使用:0次
2016-12-09更新
|
996次组卷
|
7卷引用:天津市耀华中学2020-2021学年高二上学期期末考试化学试题



