1 . 绿矾 可作补血剂,其结构如图所示:
可作补血剂,其结构如图所示:
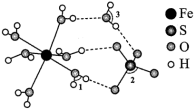
由成键一方单独提供孤电子对给予另外一方,这类“电子对给予—接受”化学键称为配位键。
(1)按照核外电子排布,可把元素周期表划分成五个区,铁元素位于元素周期表的_______ 区。
(2)基态S原子核外电子空间运动状态有___________ 种,电子占据最高能级的电子云轮廓图形状为___________ 。
(3) 中
中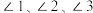 由大到小的顺序是
由大到小的顺序是___________ 。
(4)二价铁易被氧化为三价铁,结合价层电子排布式解释原因:___________ 。
 可作补血剂,其结构如图所示:
可作补血剂,其结构如图所示:
由成键一方单独提供孤电子对给予另外一方,这类“电子对给予—接受”化学键称为配位键。
(1)按照核外电子排布,可把元素周期表划分成五个区,铁元素位于元素周期表的
(2)基态S原子核外电子空间运动状态有
(3)
 中
中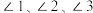 由大到小的顺序是
由大到小的顺序是(4)二价铁易被氧化为三价铁,结合价层电子排布式解释原因:
您最近一年使用:0次
2 . 下列说法正确的是
| A.多电子原子中,离原子核由近到远,电子的能量由高到低 |
| B.汤姆孙原子模型提出原子的中心有个带正电荷的核 |
C. 的酸性强于 的酸性强于 ,所以非金属性:硫>氯 ,所以非金属性:硫>氯 |
| D.元素周期表中副族共有7个 |
您最近一年使用:0次
3 . 下列化学用语不正确 的是
A.基态 原子最高能级电子云轮廓图: 原子最高能级电子云轮廓图: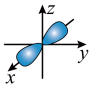 |
B.F-的结构示意图: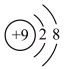 |
| C.总共含有4个能级的能层符号:N |
D.第三周期中未成对电子数最多且中子数为17的元素的原子: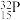 |
您最近一年使用:0次
4 . 硫酸四氨合铜 可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不法确的是
可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不法确的是
 可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不法确的是
可用于织物媒染剂、消毒剂,下列关于硫酸四氨合铜的说不法确的是| A.硫酸四氨合铜难溶于乙醇 | B.Cu元素位于周期表的ds区 |
C.硫酸四氨合铜中的铜离子为 杂化 杂化 | D.N-H键电子云轮廓图: |
您最近一年使用:0次
名校
5 . 下列说法正确的是
| A.2p、3p、4p能级的轨道数依次增多 |
| B.基态氮原子核外电子空间运动状态有5种 |
| C.焰色试验中可用无锈铁丝的原因是铁灼烧时不会产生发射光谱 |
| D.K和Cu元素的最外层电子数均为1,故均位于周期表中的s区 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.电子由2s能级跃迁至3p能级时,通过光谱仪摄取其发射光谱 |
| B.p电子云轮廓图呈哑铃形,在空间有3个伸展方向,所有电子只能在轮廓内运动 |
C.若基态N原子的轨道表示式为 ,则违反了泡利不相容原理 ,则违反了泡利不相容原理 |
| D.洪特规则适用于电子填入简并轨道,也适用于电子填入能量不同的轨道 |
您最近一年使用:0次
7 . 下列说法正确的是
| A.电子云轮廓图是电子的概率密度分布图 |
| B.s电子云轮廓图是圆形的 |
C.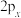 、 、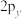 和 和 在空间内的取向相互垂直 在空间内的取向相互垂直 |
| D.同一原子的能层越低,电子云越弥散 |
您最近一年使用:0次
8 . 下列有关说法正确的是
| A.日常生活中我们看到的许多可见光都与原子核外电子跃迁吸收能量有关 |
| B.He最后一个电子填入s能级,故He属于s区 |
| C.电子云轮廓图表示电子在原子核外相应空间出现的概率,s和p电子云轮廓图均为球形 |
D.碳的基态原子轨道表示式 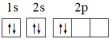 违背了洪特规则 违背了洪特规则 |
您最近一年使用:0次
9 . 下列关于物质结构或性质及解释都正确的是
| 选项 | 物质结构或性质 | 解释 |
| A | 电子云半径: |  电子的能量高,在离核更远的区域出现的概率大 电子的能量高,在离核更远的区域出现的概率大 |
| B | 键角: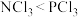 | 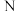 的电负性比 的电负性比 大,孤电子对对成键电子对的斥力比较大 大,孤电子对对成键电子对的斥力比较大 |
| C | 熔点: |  熔化时要断开化学键, 熔化时要断开化学键, 只需克服范德华力 只需克服范德华力 |
| D | 稳定性: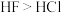 |  分子间可以形成氢键, 分子间可以形成氢键, 没有氢键 没有氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 碱金属(Li、Na、K、Rb、Cs)及其化合物在生产、生活中有着重要的应用。
请回答:
(1)基态K原子核外有___________ 种不同的电子运动状态。
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:___________
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为___________ ,其中P原子采取___________ 杂化方式。
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:___________
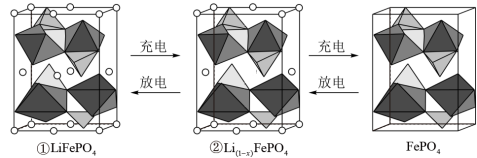
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=_________ 。
请回答:
(1)基态K原子核外有
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=

您最近一年使用:0次
2023-03-12更新
|
409次组卷
|
2卷引用:浙江省浙里卷天下2022-2023学年高三百校联考3月测试化学试题



