1 . 下列关于化学基础概念的描述正确的是
| A.氢键、共价键、离子键等是化学键 |
| B.气体摩尔体积的数值是固定的,为22.4L/mol |
| C.电子云是指核外电子高速运动,看起来像一朵云的样子 |
| D.手性碳原子是指连接四个不相同的原子或者原子团的碳原子 |
您最近一年使用:0次
2 . 人们认识世界的过程经历了从宏观到微观的过程,随着认识的不断深入,一个又一个的旧模型被打破,相应地一个又一个的新模型被建立起来。下列说法正确的是
| A.电子云是描述核外电子运动轨迹的,如s电子云是描述电子在一个特定半径的球内运动 |
| B.同一个原子中不存在两个运动状态完全一致的电子这一事实是受洪特规则限制 |
C.同一周期元素的 从左至右依次增大,同周期元素中电负性最大的元素是最右边的元素 从左至右依次增大,同周期元素中电负性最大的元素是最右边的元素 |
| D.电负性大小可以用于判断元素金属性和非金属性强弱 |
您最近一年使用:0次
2022-05-04更新
|
96次组卷
|
2卷引用:湖南省三湘名校教育联盟、五市十校教研教改共同体2021-2022学年高二下学期期中考试化学试题
3 . 下列关于Cl与S两种原子的说法正确的是
A.某条件下的S2-其核外电子排布可能是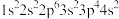 |
| B.两种原子的核外电子具有相同的运动状态数目 |
| C.两种原子的核外电子占据的原子轨道的符号不相同 |
| D.两种原子的原子光谱图谱中应该相差1条谱线 |
您最近一年使用:0次
名校
4 . 固体电解质 能提升锂-硫电池放电性能。
能提升锂-硫电池放电性能。
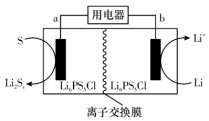
下列说法正确的是
 能提升锂-硫电池放电性能。
能提升锂-硫电池放电性能。
下列说法正确的是
| A.电池放电时b极电势高于a极 |
| B.“离子交换膜”为阴离子交换膜 |
C.a极的电极反应式为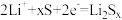 |
D.基态 的电子云轮廓图为哑铃形 的电子云轮廓图为哑铃形 |
您最近一年使用:0次
5 . 依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态V原子中具有_______ 种不同能量的电子,具有_______ 种不同空间运动状态的电子,具有_______ 种不同运动状态的电子。
(3)基态Cu原子的简化电子排布式为_______ ,基态Se原子的价电子轨道表示式为_______ ,基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性:P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Cu原子的简化电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。

可知,Li原子的第一电离能为
您最近一年使用:0次
2022-04-04更新
|
568次组卷
|
3卷引用:湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题
湖南省湖南师范大学附属中学2021-2022学年高二上学期期末考试化学试题四川省成都市武侯高级中学2021-2022学年高二下学期期中考试化学试题(已下线)寒假作业10 原子结构与性质-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
6 . 工业上用Fe(Ⅲ)作为可再生氧化剂回收工业废气中的H2S,生产单质硫。
(1)铁元素属于_______ 区(填“s”、“d”、“ds”、“p”)。
(2)Fe3+生化氧化再生法分为吸收和再生两部分。
①吸收:用Fe3+将H2S氧化为S,该反应的离子方程式是_______ 。
②再生:O2在氧化亚铁硫杆菌作用下再生Fe3+。
缺点:氧化亚铁硫杆菌生长的最佳pH范围是1.4~3.0,但酸性条件不利于H2S的吸收,结合平衡移动原理解释原因_______ 。
(3)络合铁法脱硫技术吻合节能减排、经济高效的工业化指导思想。
①碱性条件有利于H2S的吸收,但Fe3+极易形成氢氧化物和硫化物沉淀,请在图中用“↑”或“↓”补全Fe3+的电子分布图。从图中可以看出Fe3+有空轨道,可以形成溶于水的Fe3+Ln(配合物,L表示配体,n表示配位数)。_______
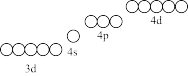
②ⅰ.写出碱性条件下Fe3+Ln氧化H2S生成S8的离子方程式_______ 。
ⅱ.O2氧化再生Fe3+Ln的离子方程式:4Fe2+Ln+O2+2H2O=4Fe3+Ln+4OH−
写出总反应的化学方程式_______ 。
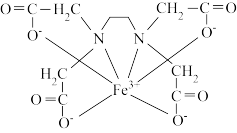
③下图是EDTA与Fe3+形成配合物的结构示意图,Fe3+外层空轨道采取sp3d2杂化,1mol该配合物中配位键有_______ mol。
(1)铁元素属于
(2)Fe3+生化氧化再生法分为吸收和再生两部分。
①吸收:用Fe3+将H2S氧化为S,该反应的离子方程式是
②再生:O2在氧化亚铁硫杆菌作用下再生Fe3+。
缺点:氧化亚铁硫杆菌生长的最佳pH范围是1.4~3.0,但酸性条件不利于H2S的吸收,结合平衡移动原理解释原因
(3)络合铁法脱硫技术吻合节能减排、经济高效的工业化指导思想。
①碱性条件有利于H2S的吸收,但Fe3+极易形成氢氧化物和硫化物沉淀,请在图中用“↑”或“↓”补全Fe3+的电子分布图。从图中可以看出Fe3+有空轨道,可以形成溶于水的Fe3+Ln(配合物,L表示配体,n表示配位数)。
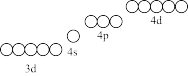
②ⅰ.写出碱性条件下Fe3+Ln氧化H2S生成S8的离子方程式
ⅱ.O2氧化再生Fe3+Ln的离子方程式:4Fe2+Ln+O2+2H2O=4Fe3+Ln+4OH−
写出总反应的化学方程式
③下图是EDTA与Fe3+形成配合物的结构示意图,Fe3+外层空轨道采取sp3d2杂化,1mol该配合物中配位键有

您最近一年使用:0次
2022-04-02更新
|
389次组卷
|
2卷引用:湖南省益阳市南县第一中学2022届高三下学期第二次模拟考试化学试题
7 . 硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为___________ ,晶体硅和碳化硅熔点较高的是___________ (填化学式);
(2) 与N-甲基咪唑
与N-甲基咪唑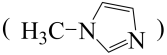 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:

N-甲基咪唑分子中碳原子的杂化轨道类型为___________ ,1个 中含有
中含有___________ 个 键;
键;
(3)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe—F键长为rpm,则B点原子的分数坐标为
)。已知Xe—F键长为rpm,则B点原子的分数坐标为___________ ;晶胞中A、B间距离d=___________ pm。

(1)基态硅原子最外层的电子排布图为
(2)
 与N-甲基咪唑
与N-甲基咪唑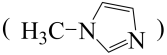 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为
 中含有
中含有 键;
键;(3)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为(
 ,
, ,
, )。已知Xe—F键长为rpm,则B点原子的分数坐标为
)。已知Xe—F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
解题方法
8 . 下列说法正确的是
| A.M能层有3s、3p、3d三个原子轨道 |
| B.同一原子中,2p、3p、4p能级的原子轨道数依次增多 |
| C.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| D.在氢原子基态电子的概率分布图中,小黑点的疏密程度表示电子在该单位体积内出现概率的大小 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.在室温下,向醋酸中加入一定量的盐酸,可改变氢离子的浓度,也可改变醋酸的电离常数 |
| B.在电解池中作为阴极的金属总是被保护的 |
| C.氢气与氯气在光照条件下反应与在点燃条件下反应的反应热是不一样的 |
| D.同一原子中,1s、2s,3s原子轨道的能量、大小、形状都相同 |
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语或图示表达正确的是
A.NaCl的电子式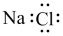 | B.SO2的VSEPR模型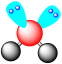 |
C.p—pσ键电子云轮廓图 | D. 的空间结构模型 的空间结构模型 |
您最近一年使用:0次
2022-01-17更新
|
515次组卷
|
7卷引用:湖南省株洲市炎陵县第一中学等2校2022-2023学年高二下学期开学考试化学试题



