1 . 磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为________ 形。
(2)Fe元素位于周期表_____ 周期_____ 族;原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为___________ 。
(3)基态Mn2+的价电子排布式为___________ ,锰的第三电离能高于铁的第三电离能,其原因是___________ 。
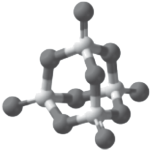
(4)P4S10的分子结构如图所示,其中含有________ 个六元环;______ g P4S10含有8molσ键。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为
(2)Fe元素位于周期表
 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为(3)基态Mn2+的价电子排布式为
(4)P4S10的分子结构如图所示,其中含有
您最近一年使用:0次
2023-12-26更新
|
155次组卷
|
4卷引用:黑龙江省齐齐哈尔市五校 黑河市四校2023-2024学年高二下学期4月期中联考化学试题
名校
2 . 如表为元素周期表的一部分,其中的编号代表对应的不同元素。
请回答下列问题:
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为___________ 。
(2)基态③原子中电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形。
(3)写出②的氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)___________
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式___________ 。
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是___________ 。
(7)⑨基态原子的简化电子排布式为___________ ,在周期表中的位置___________ 。
(8)⑩基态原子的价层电子轨道表示式为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为
(2)基态③原子中电子占据最高能级的符号是
(3)写出②的氧化物与NaOH溶液反应的化学方程式:
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是
| 元素 | 电离能(kJ•mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
(8)⑩基态原子的价层电子轨道表示式为
您最近一年使用:0次
2024-02-20更新
|
118次组卷
|
2卷引用:黑龙江省实验中学2023-2024学年高二上学期1月期末化学试题
3 . 周期表前四周期的元素a、b、c、d、e原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
(1)a的原子轨道的电子云轮廓图的形状____ 。
(2)b、c第一电离能的大小关系是____ (填元素符号),原因是____ 。
(3)e的核外电子排布式为____ 。
(4)现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为____ 。
(5)金属的焰色实验中,一些金属元素呈现不同焰色的原因是____ 。
(1)a的原子轨道的电子云轮廓图的形状
(2)b、c第一电离能的大小关系是
(3)e的核外电子排布式为
(4)现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为
(5)金属的焰色实验中,一些金属元素呈现不同焰色的原因是
您最近一年使用:0次
名校
解题方法
4 . 铁、铜及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子核外电子的运动状态有
原子核外电子的运动状态有___________ 种;
 易被氧化为
易被氧化为 ,画出
,画出 的结构示意图
的结构示意图___________ 。
(2) 是检验
是检验 的特征试剂,
的特征试剂, 中心离子配位数是
中心离子配位数是___________ ;1mol 中含有
中含有___________ mol 键,能够证明
键,能够证明 不能电离的试剂是
不能电离的试剂是___________ (填化学式)。
(3) 可形成配合物
可形成配合物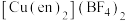 ,其中
,其中 代表
代表 分子。该配合物
分子。该配合物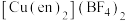 中配位离子所带电荷数为
中配位离子所带电荷数为___________ ,VSEPR模型为四面体的非金属原子共有___________ 个。 单晶的晶胞,其中原子坐标参数A为
单晶的晶胞,其中原子坐标参数A为 ;B为
;B为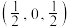 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为___________ 。
(1)基态
 原子核外电子的运动状态有
原子核外电子的运动状态有 易被氧化为
易被氧化为 ,画出
,画出 的结构示意图
的结构示意图(2)
 是检验
是检验 的特征试剂,
的特征试剂, 中心离子配位数是
中心离子配位数是 中含有
中含有 键,能够证明
键,能够证明 不能电离的试剂是
不能电离的试剂是(3)
 可形成配合物
可形成配合物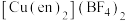 ,其中
,其中 代表
代表 分子。该配合物
分子。该配合物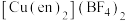 中配位离子所带电荷数为
中配位离子所带电荷数为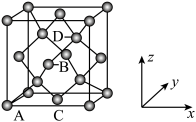
 单晶的晶胞,其中原子坐标参数A为
单晶的晶胞,其中原子坐标参数A为 ;B为
;B为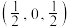 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次
9-10高二下·黑龙江鹤岗·期末
解题方法
5 . X、Y、Z、Q、E五种元素中,X原子核外M层中只有两对成对电子,Y原子核外L层电子数是K层两倍,Z是地壳内含量(质量分数)最高元素,Q核电荷数是X与Z核电荷数之和,E电负性最大。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(1)相同条件下XZ2与YZ2分子在水中溶解度较大是 ,理由是
;
(2)Q的外围电子排布为 ,在形成化合物时它的最高化合价为 ;
(3)在测定E的气态氢化物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
您最近一年使用:0次



