真题
名校
1 . 钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______ nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________ ,占据该能层电子的电子云轮廓图形状为___________ 。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________ 。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________ ,中心原子的杂化形式为________________ 。
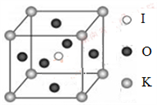
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______ nm,与K紧邻的O个数为__________ 。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______ 位置,O处于______ 位置。
 .
.
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于
 .
.
您最近一年使用:0次
2017-08-09更新
|
8928次组卷
|
22卷引用:广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题
广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)(已下线)【中等生百日捷进提升系列-基础练测】专题2.17 物质结构与性质(已下线)【艺体生文化课百题突围系列-基础练测】专题2.17 物质结构与性质(选修)(已下线)《考前20天终极攻略》5月30日 物质结构与性质(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密西藏自治区昌都第四高级中学2019届高三下学期4月月考理科综合化学试题(已下线)《2019年高考总复习巅峰冲刺》专题12 物质结构与性质应试策略云南省富宁县民族中学2020届高三上学期开学考试化学试题四川省成都实验中学2019-2020学年度高三上学期1月月考理科综合化学试题第3章 物质的聚集状态与物质性质——C挑战区 模拟高考(鲁科版选修3)云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题广东省梅州市五华县2018-2019学年高二上学期第六次质量监测化学试题河北省衡水中学2020届高三四月份质量监测理综化学试题(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题湖北省武汉市华中师范大学第一附属中学2020届高三下学期四月份网络教学质量监测理科综合化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)云南省玉溪市民族中学2021-2022学年高三1月份考试理综化学试题云南省富宁县第一中学校2021-2022学年高三下学期开学考试理综化学试题
2 . N、P、Ni及其化合物在化工医药,材料等方面应用十分广泛。回答下列有关问题:
(1)NH3分子的立体构型为______ ,热稳定性 NH3______ PH3(填“>”或“<”),原因是______ 。
(2)在短周期元素组成的物质中,与 互为等电子体的分子有
互为等电子体的分子有______ 。
(3)N元素能形成多种化合物,它们之间可以发生相互转化,如: 。
。
①N的基态原子的电子排布中,有______ 个运动状态不同的未成对电子。
②叠氮酸(HN3)在常温下是液体,沸点相对较高(为 308.8 K)主要原因是______ 。
③HNO2中 N 原子的杂化类型是______ ;NH3分子中______ (填“含有”或“不含”)π键
(4)已知次氯酸和磷酸的结构简式如图所示,试比较两者的酸性:HClO______  (填“>”或“<”),原因是
(填“>”或“<”),原因是______ (从结构角度分析)。
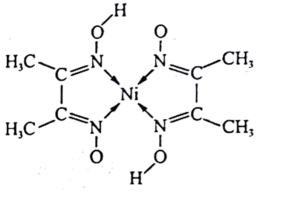
(5)Ni是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀,常被用在电镀上。工业上常用丁二酮肟来检验 Ni2+,反应生成鲜红色沉淀,丁二酮肟的结构简式如图所示,则该结构中碳氮之间的共价键类型是______ 型,氮镍之间形成的化学键是______ ,碳原子的杂化类型是______ 。
(1)NH3分子的立体构型为
(2)在短周期元素组成的物质中,与
 互为等电子体的分子有
互为等电子体的分子有(3)N元素能形成多种化合物,它们之间可以发生相互转化,如:
 。
。①N的基态原子的电子排布中,有
②叠氮酸(HN3)在常温下是液体,沸点相对较高(为 308.8 K)主要原因是
③HNO2中 N 原子的杂化类型是
(4)已知次氯酸和磷酸的结构简式如图所示,试比较两者的酸性:HClO
 (填“>”或“<”),原因是
(填“>”或“<”),原因是| 次氯酸 | 磷酸 |
| Cl—OH | 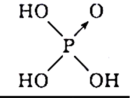 |
(5)Ni是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀,常被用在电镀上。工业上常用丁二酮肟来检验 Ni2+,反应生成鲜红色沉淀,丁二酮肟的结构简式如图所示,则该结构中碳氮之间的共价键类型是

您最近一年使用:0次
3 . 已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。
(1)X元素原子基态时的电子排布式为_______ ,Y元素原子的价层电子排布图为_____________ 。
(2)Y原子核外有________ 种不同运动状态的电子,其基态原子中能量最高的电子,其电子云在空间有_______ 个方向。
(1)X元素原子基态时的电子排布式为
(2)Y原子核外有
您最近一年使用:0次



