1 . 下列说法正确的是
| A.2px、2py、2pz轨道相互垂直,能量相等 |
| B.稀有气体元素的基态原子的价电子排布式都为ns2np6 |
| C.第一电离能越大,元素的电负性也越大 |
| D.元素周期表各周期总是从ns能级开始,以np能级结束 |
您最近半年使用:0次
2 .  能层包含的能级数和最多能容纳的电子数分别为
能层包含的能级数和最多能容纳的电子数分别为
 能层包含的能级数和最多能容纳的电子数分别为
能层包含的能级数和最多能容纳的电子数分别为| A.2 2 | B.2 8 | C.3 8 | D.3 18 |
您最近半年使用:0次
2021-07-07更新
|
828次组卷
|
6卷引用:湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题
湖北省十堰市2020-2021学年高二下学期期末调研考试化学试题(已下线)第1.1.1讲 能层与能级 基态与激发态-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二下学期期中考试化学试题广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题新疆霍尔果斯市苏港中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
3 . 有A、B、C、D、E五种元素。其相关信息如下:
请回答下列问题。
(1)D是___________ (填元素名称), D的基态原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________
(2) 若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为___________ (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(3)元素E所在的周期,未成对电子数最多的元素是___________ (填元素符号)
(4)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是___________

(5)向溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体。请写出氨水过量后沉淀逐渐溶解的离子方程式:___________ 。
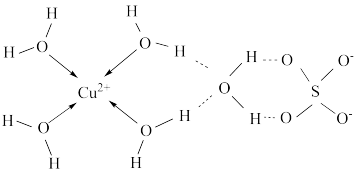
(6)科学家推测胆矾结构示意图可简单表示如图:胆矾的化学式用配合物的形式表示为___________ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有一个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和EO两种氧化物 |
请回答下列问题。
(1)D是
(2) 若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(3)元素E所在的周期,未成对电子数最多的元素是
(4)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(5)向溶液中滴加氨水,首先出现蓝色沉淀,氨水过量后沉淀逐渐溶解,加入乙醇后析出深蓝色晶体。请写出氨水过量后沉淀逐渐溶解的离子方程式:
(6)科学家推测胆矾结构示意图可简单表示如图:胆矾的化学式用配合物的形式表示为

您最近半年使用:0次
4 . 某元素的M层有4个p电子,下列叙述错误的是
| A.N层不含电子 | B.该元素是硫元素 |
| C.L层一定有8个电子 | D.原子最外层电子数为4 |
您最近半年使用:0次
2019-11-17更新
|
213次组卷
|
4卷引用:湖北省汉川实验高中2020-2021学年高二下学期期中考试化学试题
湖北省汉川实验高中2020-2021学年高二下学期期中考试化学试题海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第一节 原子结构(已下线)第1章 原子结构与性质(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)
名校
5 . 若某原子在处于能量最低状态时,外围电子排布为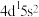 ,则下列说法错误的是
,则下列说法错误的是
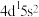 ,则下列说法错误的是
,则下列说法错误的是| A.该元素可能有+3价 |
| B.该元素位于第5周期副族 |
| C.该元素原子核外共有39个不同运动状态的电子 |
| D.该元素基态原子第N能层上还有5个空轨道 |
您最近半年使用:0次
2019-03-16更新
|
428次组卷
|
6卷引用:湖北省随州市第一中学2018-2019学年高二下学期期中考试化学试题
名校
6 . 下列说法正确的是( )
| A.s电子云是在空间各个方向上伸展程度相同的对称形状 |
| B.p电子云是平面“8”字形的 |
| C.2p能级有一个未成对电子的基态原子的电子排布式一定为1s22s22p5 |
| D.2d能级包含5个原子轨道,最多容纳10个电子 |
您最近半年使用:0次
2018-12-22更新
|
199次组卷
|
8卷引用:湖北省宜昌市葛洲坝中学2018-2019学年高二下学期期中考试化学试题
湖北省宜昌市葛洲坝中学2018-2019学年高二下学期期中考试化学试题(已下线)同步君 选修3 第一章 第一节 电子云和原子轨道高中化学人教版 选修三 第1章 原子结构与性质 电子云与原子轨道贵州省织金县第一中学2018-2019学年高二上学期期中考试化学试题云南省盐津县第二中学2018-2019学年高二上学期12月份考试化学试题云南省昭通市威信县第一中学2018-2019学年高二上学期12月份考试化学试题(已下线)1.2.1 基态原子的核外电子排布-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)BBWYhjhx1112.pdf
名校
7 . 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有有2个未成对电子;Q原子的S能级和P能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料,T处于周期表的ds区原子中只有一个未成对的电子。下列说法不正确的是
| A.Y原子核外有7中不同运动状态的电子,基态T原子有7种不同能级的电子。 |
| B.X、Y、Z的第一电离能由小到大的顺序为X<Z<Y。 |
| C.由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,且ZXY-中X原子的杂化方式为sp |
| D.Q的氧化物与X的单质在一定条件下能发生置换反应。 |
您最近半年使用:0次
2017-04-21更新
|
262次组卷
|
2卷引用:2016-2017学年湖北省武汉市第二中学高二下学期期中考试化学试卷
名校
8 . 下列说法中正确的是( )
| A.s电子绕核旋转,其轨道为一圆圈,而p电子是∞字形 |
| B.能层为1时,有自旋相反的两个轨道 |
| C.能层为3时,有3s、3p、3d、4f四个轨道 |
| D.s电子云是球形对称的,其疏密程度表示电子在该处出现的概率大小 |
您最近半年使用:0次
2017-04-12更新
|
546次组卷
|
9卷引用:湖北省襄阳市第四中学2017-2018学年高二12月月考化学试题
湖北省襄阳市第四中学2017-2018学年高二12月月考化学试题2016-2017学年甘肃省武威市第十八中学高二下学期第一次月考化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1贵州省安顺市普定县第一中学2018-2019学年高二上学期12月考试化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二下学期第一次月考化学试题云南省保山市昌宁县一中2019-2020学年高二10月月考化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)河北省石家庄市第一中学2019-2020学年高二下学期第一次月考化学试题
解题方法
9 . 化学中的某些元素与生命活动密不可分。请回答下列问题:
(1)(NH4)2SO4是一种重要的化学肥料,其中N、S原子的杂化方式分别是______ 、______ ,SO2-4的空间构型为_______________ 。
(2)钙是儿童生长不可缺少的元素,基态钙原子中,电子没有全充满的能层是________ 。
(3)蛋白质中含有N、P等元素,它们分别形成的简单气态氢化物键角大小关系是_____ (用化学式表示),原因是_________________ 。
(4)金属铁、镍及其形成的许多化合物常用作催化剂。已知NiO、FeO的晶体类型均与氯化钠晶体相同,熔点NiO>FeO,推测 Ni2+和 Fe2+离子半径的大小关系是__________ ,作出判断的依据是____________ 。
(5)某金属是抗癌药物中的明星元素,其晶体中原子的堆积方式如图所示。

晶胞中金属原子的配位数为_____ 。若已知金属的摩尔质量为M g/mol ,阿伏加德罗常数为NA,原子半径为r pm,则该晶胞的密度为 p=_____ g/ cm3。(用含M、NA、r的计算式表示,不用化简)
(1)(NH4)2SO4是一种重要的化学肥料,其中N、S原子的杂化方式分别是
(2)钙是儿童生长不可缺少的元素,基态钙原子中,电子没有全充满的能层是
(3)蛋白质中含有N、P等元素,它们分别形成的简单气态氢化物键角大小关系是
(4)金属铁、镍及其形成的许多化合物常用作催化剂。已知NiO、FeO的晶体类型均与氯化钠晶体相同,熔点NiO>FeO,推测 Ni2+和 Fe2+离子半径的大小关系是
(5)某金属是抗癌药物中的明星元素,其晶体中原子的堆积方式如图所示。

晶胞中金属原子的配位数为
您最近半年使用:0次



