解题方法
1 . 回答下列问题:
(1)1 mol CO2中含有的σ键数目为_______ ,π键数目为_______ 。
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是_______ 。
(3)铜原子的价层电子排布图:_______ ,写出钴的简化电子排布式_______ ,基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_______ 、_______ (填标号)。
A. B.
B. 
C.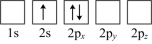 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为_______ 。
②1 mol bte分子中含σ键的数目为_______ mol。
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为_______ 。

(1)1 mol CO2中含有的σ键数目为
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是
(3)铜原子的价层电子排布图:
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. 
C.
 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为
②1 mol bte分子中含σ键的数目为
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为

您最近一年使用:0次
名校
解题方法
2 . 高效节能、寿命长的半导体照明产品正在引领照明行业的绿色变革,而氮化镓(GaN)的研制是实现半导体照明的核心技术和基础,当前我国在第三代半导体材解研制方面走在世界的前列。回答下列有关问题。
(1)基态Ga原子的价层电子排布式为_______ 。
(2)GaN在加热条件下与NaOH溶液发生如下反应:CaN+OH-+H2O=GaO +NH3↑。
+NH3↑。
①基态N、O分别失去一个电子时,需要吸收能量更多的是_______ ,判断的理由是_______ 。
②GaO 在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为
在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为_______ ,1mol[Ga(H2O)6]3+中所含有的σ键数目为_______ , 与H2O相比,键角
与H2O相比,键角
_______ H2O(填“>”或“<”)。
(3)GaN的一种晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①氮化镓中镓原子的杂化方式为_______ ,与同一个Ga原子相连的N原子构成的空间构型为_______ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如下图所示,则2、3、4原子的分数坐标不可能的是_______ (填序号)。

a.(0.75,0.75,0.25) b.(0.75,0.25,0.75)
c.(0.25,0.25,0.25) d.(0.25,0.75,025)
③GaN晶体中N和N的原子核间距为apm,GaN的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则GaN晶体的密度为_______ g·cm-3。
(1)基态Ga原子的价层电子排布式为
(2)GaN在加热条件下与NaOH溶液发生如下反应:CaN+OH-+H2O=GaO
 +NH3↑。
+NH3↑。①基态N、O分别失去一个电子时,需要吸收能量更多的是
②GaO
 在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为
在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为 与H2O相比,键角
与H2O相比,键角
(3)GaN的一种晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①氮化镓中镓原子的杂化方式为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如下图所示,则2、3、4原子的分数坐标不可能的是

a.(0.75,0.75,0.25) b.(0.75,0.25,0.75)
c.(0.25,0.25,0.25) d.(0.25,0.75,025)
③GaN晶体中N和N的原子核间距为apm,GaN的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则GaN晶体的密度为
您最近一年使用:0次
2022-04-19更新
|
519次组卷
|
2卷引用:甘肃省2022届高三第二次高考诊断考试(二模)理科综合化学试题
解题方法
3 . 近年来我国科学家发现了一系列意义重大的铁系超导材料,其中含有Fe、As、Ti等元素。回答下列问题:
(1)Fe转化为阳离子时首先失去__ 轨道电子,基态Fe3+核外电子排布式为__ 。
(2)AsH3中心原子杂化类型为__ 。
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是__ ,理由是___ 。
(4)Ti金属晶体的堆积模型为__ ,配位数为__ ,基态Ti3+中未成对电子数有_ 个。
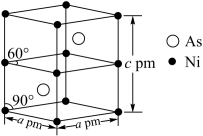
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=__ g·cm-3。
(1)Fe转化为阳离子时首先失去
(2)AsH3中心原子杂化类型为
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是
(4)Ti金属晶体的堆积模型为
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=

您最近一年使用:0次



