解题方法
1 . 回答下列问题:
(1)1 mol CO2中含有的σ键数目为_______ ,π键数目为_______ 。
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是_______ 。
(3)铜原子的价层电子排布图:_______ ,写出钴的简化电子排布式_______ ,基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_______ 、_______ (填标号)。
A. B.
B. 
C.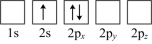 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为_______ 。
②1 mol bte分子中含σ键的数目为_______ mol。
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为_______ 。

(1)1 mol CO2中含有的σ键数目为
(2)CH4、NH3、H2O、HF分子中共价键的极性由强到弱的顺序是
(3)铜原子的价层电子排布图:
(4)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. 
C.
 D.
D. 
(5)bte的分子式为C6H8N6,其结构简式如图所示:

①bte分子中碳原子轨道杂化类型为
②1 mol bte分子中含σ键的数目为
(6)一个Cu2O晶胞(见图)中,Cu原子的数目为

您最近一年使用:0次
解题方法
2 . 氢镍电池是目前使用最广的含镍电池,废旧电池的处理对环境保护和资源的再利用意义重大。一种对废旧氢镍电池负极材料(含有NiO、Ni和少量La、Fe、Mg、MnO2、石墨粉等)进行湿法处理的流程如图所示:
②Ksp(MgF2)=6.4 ;
;
③H2SO4第一步完全电离,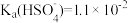 。
。
回答下列问题:
(1)Ni2+的价层电子排布式为_____________ 。
(2)能提高“酸浸”效率的措施有_____________ (任写一种)。
(3)若滤渣1的成分为 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因_________________ 。
(5)“沉镁”后滤液3中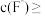
__________  (溶液中离子浓度
(溶液中离子浓度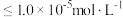 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。
(6) 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为_________________ 。
(7)“沉镍”所用试剂不宜选用氨水的原因为_________________ ,母液中可提取出的循环利用的物质为_____________ (填化学式)。
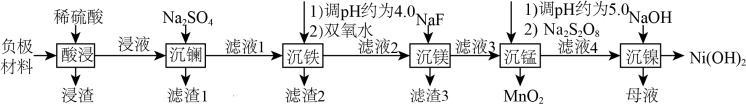
②Ksp(MgF2)=6.4
 ;
;③H2SO4第一步完全电离,
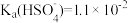 。
。回答下列问题:
(1)Ni2+的价层电子排布式为
(2)能提高“酸浸”效率的措施有
(3)若滤渣1的成分为
 ,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因
,已知“沉镧”过程中溶液的pH与沉镧率的变化关系如图所示。试分析pH<2.0时沉镧率降低的原因 
| A.KSCN溶液 |
| B.K3[Fe(CN)6]溶液 |
| C.NaOH溶液 |
| D.KSCN溶液和氯水 |
(5)“沉镁”后滤液3中
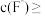
 (溶液中离子浓度
(溶液中离子浓度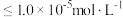 时认为该离子沉淀完全)。
时认为该离子沉淀完全)。(6)
 中存在过氧键(-O-O-),“沉锰”反应的离子方程式为
中存在过氧键(-O-O-),“沉锰”反应的离子方程式为(7)“沉镍”所用试剂不宜选用氨水的原因为
您最近一年使用:0次
3 . 我国科学家用粗氢氧化高钴 制备硫酸钴晶体(
制备硫酸钴晶体(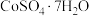 ),其工艺流程如下:
),其工艺流程如下:

已知:ⅰ.还原浸出液中的阳离子有: 、
、 、
、 和
和 等
等
ⅱ.部分物质的溶度积常数(25℃)
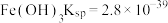
ⅲ.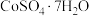 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大
(1)Co元素位于元素周期表的_______ 区,基态Co原子的核外电子排布式为_______ 。
(2)浸出 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为_______ 。
(3)写出“氧化沉铁”的离子方程式_______ ,25℃时,浊液中铁离子浓度为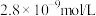 ,此时溶液
,此时溶液
_______ 。
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因_______ 。
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为: 。
。
已知:铁氰化钾标准液浓度为 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为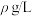 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗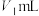 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。
计算样品中钴含量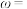
_______ (以钴的质量分数 计)。
计)。
(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为_______ 。已知:晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高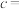
_______  (列出计算式)。
(列出计算式)。

 制备硫酸钴晶体(
制备硫酸钴晶体(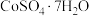 ),其工艺流程如下:
),其工艺流程如下:
已知:ⅰ.还原浸出液中的阳离子有:
 、
、 、
、 和
和 等
等ⅱ.部分物质的溶度积常数(25℃)

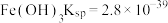
ⅲ.
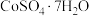 溶解度随温度升高而明显增大
溶解度随温度升高而明显增大(1)Co元素位于元素周期表的
(2)浸出
 时,理论上还原性离子和氧化性离子物质的量比为
时,理论上还原性离子和氧化性离子物质的量比为(3)写出“氧化沉铁”的离子方程式
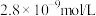 ,此时溶液
,此时溶液
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因
(5)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氯化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:
 。
。已知:铁氰化钾标准液浓度为
 ,Co(Ⅱ)标准液质量浓度为
,Co(Ⅱ)标准液质量浓度为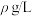 。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗
。取1.000g硫酸钴晶体,加水配成200mL溶液,取10mL待测液进行滴定,消耗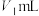 铁氰化钾标准液、
铁氰化钾标准液、 Co(Ⅱ)标准液。
Co(Ⅱ)标准液。计算样品中钴含量
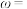
 计)。
计)。(6)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,则该晶胞的高
,则该晶胞的高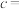
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
解题方法
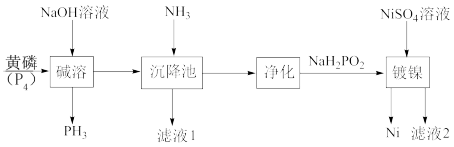
4 . 次磷酸钠(NaH2PO2)是具有珍珠光泽的晶体或白色结晶性粉末,易溶于水、乙醇、甘油,微溶于氨水,不溶于乙醚。次磷酸钠(NaH2PO2)广泛应用于化学镀镍,其制备与镀镍过程如下图所示:
(1)基态Ni原子的核外电子排布式为_____ ,PH3的分子空间构型为_____ 。
(2)“碱溶”过程中,发生反应化学方程式为_____ 。
(3)“沉降池”中通入氨气的目的是_____ ,“净化”操作需要过滤、洗涤、干燥,洗涤时,选用的洗涤剂为_____ 。
(4)“滤液2”经分离提纯可以得H3PO2,写出“镀镍”过程发生的离子反应方程式_____ ,充分反应后,向“滤液2”中,加入适量 悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
_____ [已知: ,
, ]
]
(5)Ni和La的合金是目前使用广泛的储氢材料,该合金的晶胞结构如图所示。_____ 。
②已知该晶体晶胞底面边长为apm,高为cpm,设 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为_____  (用含a、c、
(用含a、c、 的代数式表示)
的代数式表示)
(1)基态Ni原子的核外电子排布式为
(2)“碱溶”过程中,发生反应化学方程式为
(3)“沉降池”中通入氨气的目的是
(4)“滤液2”经分离提纯可以得H3PO2,写出“镀镍”过程发生的离子反应方程式
 悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
悬浊液,生成CaSO4和CaHPO4混合沉淀,此时
 ,
, ]
](5)Ni和La的合金是目前使用广泛的储氢材料,该合金的晶胞结构如图所示。
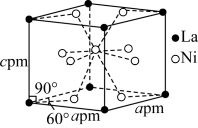
②已知该晶体晶胞底面边长为apm,高为cpm,设
 为阿伏伽德罗常数的值,则该晶体的密度为
为阿伏伽德罗常数的值,则该晶体的密度为 (用含a、c、
(用含a、c、 的代数式表示)
的代数式表示)
您最近一年使用:0次
2023-09-15更新
|
136次组卷
|
2卷引用:甘肃省酒泉市瓜州县第一中学2023-2024学年高三上学期期末化学试题
名校
解题方法
5 . 中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸中C原子的杂化方式为___________ ,晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)比较NH3分子(前者)和在 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者___________ 后者。(填“>”、“<”或“=”)
(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数
___________  (列出表达式)。
(列出表达式)。

(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸中C原子的杂化方式为
(3)比较NH3分子(前者)和在
 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
2023-09-13更新
|
270次组卷
|
2卷引用:甘肃省民乐县第一中学2023-2024学年高三10月月考化学试题
名校
解题方法
6 . 高效节能、寿命长的半导体照明产品正在引领照明行业的绿色变革,而氮化镓(GaN)的研制是实现半导体照明的核心技术和基础,当前我国在第三代半导体材解研制方面走在世界的前列。回答下列有关问题。
(1)基态Ga原子的价层电子排布式为_______ 。
(2)GaN在加热条件下与NaOH溶液发生如下反应:CaN+OH-+H2O=GaO +NH3↑。
+NH3↑。
①基态N、O分别失去一个电子时,需要吸收能量更多的是_______ ,判断的理由是_______ 。
②GaO 在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为
在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为_______ ,1mol[Ga(H2O)6]3+中所含有的σ键数目为_______ , 与H2O相比,键角
与H2O相比,键角
_______ H2O(填“>”或“<”)。
(3)GaN的一种晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①氮化镓中镓原子的杂化方式为_______ ,与同一个Ga原子相连的N原子构成的空间构型为_______ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如下图所示,则2、3、4原子的分数坐标不可能的是_______ (填序号)。

a.(0.75,0.75,0.25) b.(0.75,0.25,0.75)
c.(0.25,0.25,0.25) d.(0.25,0.75,025)
③GaN晶体中N和N的原子核间距为apm,GaN的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则GaN晶体的密度为_______ g·cm-3。
(1)基态Ga原子的价层电子排布式为
(2)GaN在加热条件下与NaOH溶液发生如下反应:CaN+OH-+H2O=GaO
 +NH3↑。
+NH3↑。①基态N、O分别失去一个电子时,需要吸收能量更多的是
②GaO
 在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为
在高氯酸的热溶液中可以生成化合物[Ga(H2O)6](ClO4)3,该化合物中提供孤电子对形成配位键的原子为 与H2O相比,键角
与H2O相比,键角
(3)GaN的一种晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替,顶点和面心的碳原子被Ga原子代替。
①氮化镓中镓原子的杂化方式为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如下图所示,则2、3、4原子的分数坐标不可能的是

a.(0.75,0.75,0.25) b.(0.75,0.25,0.75)
c.(0.25,0.25,0.25) d.(0.25,0.75,025)
③GaN晶体中N和N的原子核间距为apm,GaN的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则GaN晶体的密度为
您最近一年使用:0次
2022-04-19更新
|
521次组卷
|
2卷引用:甘肃省2022届高三第二次高考诊断考试(二模)理科综合化学试题
解题方法
7 . 近年来我国科学家发现了一系列意义重大的铁系超导材料,其中含有Fe、As、Ti等元素。回答下列问题:
(1)Fe转化为阳离子时首先失去__ 轨道电子,基态Fe3+核外电子排布式为__ 。
(2)AsH3中心原子杂化类型为__ 。
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是__ ,理由是___ 。
(4)Ti金属晶体的堆积模型为__ ,配位数为__ ,基态Ti3+中未成对电子数有_ 个。
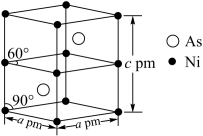
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=__ g·cm-3。
(1)Fe转化为阳离子时首先失去
(2)AsH3中心原子杂化类型为
(3)与As同主族的短周期元素有N、P,一定压强下将AsH3、NH3和PH3的混合气体降温,首先液化的是
(4)Ti金属晶体的堆积模型为
(5)某砷镍合金的晶胞结构如图所示,设阿伏加德罗常数的值为NA,则该晶体的密度ρ=

您最近一年使用:0次
8 . 元素X位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有1对成对电子。X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是( )


| A.该晶体属于原子晶体 |
| B.X2+的配位数为8,Y2-的配位数为4 |
| C.与每个X2+距离最近且相等的X2+共有12个 |
| D.该晶体的熔点比氧化锌高 |
您最近一年使用:0次
2020-05-06更新
|
841次组卷
|
5卷引用:甘肃省兰州市第一中学2019-2020学年高二下学期4月月考化学试题
甘肃省兰州市第一中学2019-2020学年高二下学期4月月考化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖北省黄冈中学2021届高三下学期6月适应性考试化学试题(已下线)考点35 晶体结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)趋势6 模块杂糅命题



