名校
解题方法
1 . A、B、C、D、E、F为原子序数依次增大的前四周期元素,A元素原子最外层电子数是其内层电子数的2.5倍,B元素是地壳中含量最高的元素,C元素的最高化合价和最低化合价的代数和等于0,D元素的单质可用于自来水消毒杀菌,E元素位于周期表的VIB族,F元素的基态原子中有4个未成对电子。
(1)A元素单质的结构式为_______ ,基态E元素原子价层电子排布图为_______ 。
(2)A的氢化物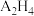 分子属于
分子属于_______ 分子(填“极性或非极性”),A与B形成的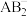 的空间构型为
的空间构型为_______ 。
(3)火箭推动剂由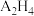 和
和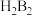 组成,加热反应时有
组成,加热反应时有 元素的单质生成,写出该化学反应方程式:
元素的单质生成,写出该化学反应方程式:_______ 。基态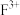 未成对电子数为
未成对电子数为_______ 个。
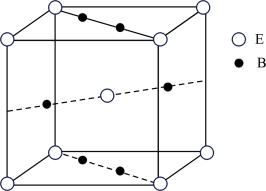
(4)元素B与E形成的一种化合物广泛应用于录音磁带上,其晶胞如图所示。若晶胞参数(边长)为apm, 为阿伏加德罗常数的值,则该晶胞的密度为
为阿伏加德罗常数的值,则该晶胞的密度为_______  。
。
(1)A元素单质的结构式为
(2)A的氢化物
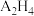 分子属于
分子属于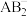 的空间构型为
的空间构型为(3)火箭推动剂由
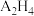 和
和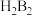 组成,加热反应时有
组成,加热反应时有 元素的单质生成,写出该化学反应方程式:
元素的单质生成,写出该化学反应方程式: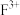 未成对电子数为
未成对电子数为(4)元素B与E形成的一种化合物广泛应用于录音磁带上,其晶胞如图所示。若晶胞参数(边长)为apm,
 为阿伏加德罗常数的值,则该晶胞的密度为
为阿伏加德罗常数的值,则该晶胞的密度为 。
。
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语表示正确的是
A.丙烯的结构简式: |
B.碳的基态原子轨道表示式: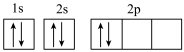 |
C.氨气的价层电子对互斥模型: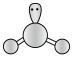 |
D.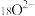 离子结构示意图: 离子结构示意图: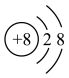 |
您最近一年使用:0次
名校
解题方法
3 .  是一种典型的配合物,下列有关说法中正确的是
是一种典型的配合物,下列有关说法中正确的是
 是一种典型的配合物,下列有关说法中正确的是
是一种典型的配合物,下列有关说法中正确的是A.基态N原子的轨道表示式为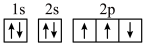 |
| B.第一电离能大小顺序:N>S>O |
C.1mol  中含有12mol共价键 中含有12mol共价键 |
D.N原子和S原子的杂化方式都为 杂化 杂化 |
您最近一年使用:0次
名校
解题方法
4 . 碳元素在生产生活中具有非常重要的作用,在新物质的制备中也发挥了举足轻重的作用。甲、乙、丙分别是石墨烯、金刚石、C60(一个小黑点代表一个C60分子)的晶胞模型,下列说法正确的是

| A.与碳同周期,且基态原子的核外未成对电子数相等的元素是N |
| B.C60为共价晶体,一个C60晶胞中含有4个C60分子 |
| C.二氧化硅结构跟金刚石结构相似,二氧化硅的空间网状结构中,Si、O形成的最小环上O原子数目是6 |
| D.石墨烯中每个C原子价层电子对个数是2,根据价层电子对互斥理论知C原子杂化类型为sp2 |
您最近一年使用:0次
5 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:(已知: 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)
(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为___________ ;配合物 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是___________ (填元素符号)。
(2)现有下列实验:___________ ,溶剂X可以是___________ (填名称),继续添加氨水,沉淀溶解的离子方程式为___________ 。
②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是___________ 。
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
 在溶液中为橙色,
在溶液中为橙色, 在溶液中为黄色)
在溶液中为黄色)(1)下列反应曾用于检测司机是否酒后驾驶,原理如下:

基态Cr原子外围电子轨道表示式为
 中与Cr3+形成配位键的原子是
中与Cr3+形成配位键的原子是(2)现有下列实验:

②该实验能说明NH3、H2O与Cu2+结合的能力由强到弱的顺序是
(3)下列有关化学实验的“操作→现象→解释”均正确的是___________(填字母)。
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 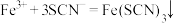 |
| B | 向由0.1mol CrCl3∙6H2O配成的溶液中加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知Cr3+的配位数为6,则CrCl3∙6H2O的化学式可表示为 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加10滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在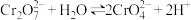 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . O3和O2互为___________ (选填“同素异形体”或“同位素”)。氧元素位于元素周期表的___________ 区。
A.s B.p C.d D.f
A.s B.p C.d D.f
您最近一年使用:0次
名校
解题方法
7 . 铁及其化合物在生活、生产中有重要应用。回答下列问题:
(1)乳酸亚铁 是一种常用的补铁剂。
是一种常用的补铁剂。
① 的价电子排布图为
的价电子排布图为___________ 。 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。
①硝普钠中 的配位数为
的配位数为___________ 。
②硝普钠中不存在的化学键有___________ (填序号)。
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 (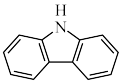 ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比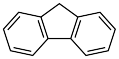 高的主要原因是
高的主要原因是___________ ,咔唑分子中所有原子共平面,咔唑与  都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑___________ 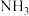 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。
(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。___________ 。
②该晶胞参数分别为 a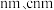 ,该晶体密度
,该晶体密度
___________ 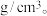 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
(1)乳酸亚铁
 是一种常用的补铁剂。
是一种常用的补铁剂。①
 的价电子排布图为
的价电子排布图为②乳酸分子( )中
)中  键与
键与  键的数目之比为
键的数目之比为
 可用于治疗急性心率衰竭。
可用于治疗急性心率衰竭。①硝普钠中
 的配位数为
的配位数为②硝普钠中不存在的化学键有
a.离子键 b.金属键 c. 配位键 d.极性共价键
(3)咔唑 (
 ),)用于制备靶向Fe2+荧光探针,咔唑沸点比
),)用于制备靶向Fe2+荧光探针,咔唑沸点比 高的主要原因是
高的主要原因是 都能与
都能与  配位,配位能力: 咔唑
配位,配位能力: 咔唑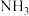 (填"> "、"<"、"=")。
(填"> "、"<"、"=")。(4)由铁、钾、硒形成的一种超导材料,其晶胞结构和xy平面投影如图所示。

②该晶胞参数分别为 a
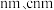 ,该晶体密度
,该晶体密度
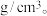 ( 用
( 用  表示阿伏加德罗常数 )
表示阿伏加德罗常数 )
您最近一年使用:0次
名校
解题方法
8 .  难溶于水但易溶于氨水,反应方程式为
难溶于水但易溶于氨水,反应方程式为 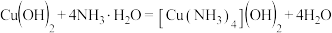 。下列化学用语表示正确的是
。下列化学用语表示正确的是
 难溶于水但易溶于氨水,反应方程式为
难溶于水但易溶于氨水,反应方程式为 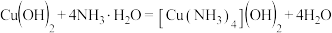 。下列化学用语表示正确的是
。下列化学用语表示正确的是A.第一电离能:  |
B.基态  原子的轨道表示式: 原子的轨道表示式: 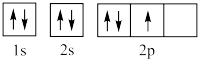 |
| C.水分子的VSEPR模型为V形 |
D. 分子的空间构型为平面三角形 分子的空间构型为平面三角形 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.s电子云表示电子绕原子核做圆周运动 |
| B.电子云图中的小黑点密度大,说明该原子核外空间电子数目多 |
C.p电子的电子云轮廓图可表示为 |
D.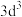 表示的电子排布图为 表示的电子排布图为 |
您最近一年使用:0次
名校
解题方法
10 . 以NaOH、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: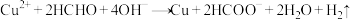
(1)基态Cu原子的价层电子轨道表示式为______
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的______ 性。
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是______ 。
a.HCHO、 均属于极性分子
均属于极性分子
b.HCHO与 之间能形成氢键
之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是______ 。
(4)为防止 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是______ 。
(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于______ 区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
①______ 。
②聚酰亚胺在碱性条件下会发生水解。
 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: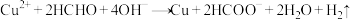
(1)基态Cu原子的价层电子轨道表示式为
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
a.HCHO、
 均属于极性分子
均属于极性分子b.HCHO与
 之间能形成氢键
之间能形成氢键c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是(4)为防止
 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 (
( )
)
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
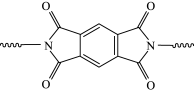
①
②聚酰亚胺在碱性条件下会发生水解。
您最近一年使用:0次



