解题方法
1 . MnS纳米粒子被广泛应用于除去重金属离子中的镉离子。
(1)锰的价层电子排布式为__________ 。
(2)磁性氧化铁纳米粒子除镉效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小
__________  (填>、<或=)。
(填>、<或=)。 中
中 的键角比
的键角比 中的
中的__________ (填大或小)
(3)Mn可以形成多种配合物, 中第二周期元素第一电离能由大到小关系为
中第二周期元素第一电离能由大到小关系为__________ ,配体 中心原子杂化类型为
中心原子杂化类型为__________ 配体 的空间构型为
的空间构型为__________ (用文字描述)。
(1)锰的价层电子排布式为
(2)磁性氧化铁纳米粒子除镉效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小

 (填>、<或=)。
(填>、<或=)。 中
中 的键角比
的键角比 中的
中的(3)Mn可以形成多种配合物,
 中第二周期元素第一电离能由大到小关系为
中第二周期元素第一电离能由大到小关系为 中心原子杂化类型为
中心原子杂化类型为 的空间构型为
的空间构型为
您最近一年使用:0次
名校
2 . 合成氨( )是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)基态氢原子中,核外电子的电子云轮廓图形状为___________ 。
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ 。 分子的电子式为
分子的电子式为___________ 。
② 分子中,与N原子相连的H显正电性。则电负性:N
分子中,与N原子相连的H显正电性。则电负性:N___________ H.(填“>”或“<”)。 分子的VSEPR理想模型的名称为
分子的VSEPR理想模型的名称为___________ ,其分子的空间结构为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较第一电离能的大小:Mg___________ Ca(填“>”或“<”)。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
请解释:(a)为什么原子的逐级电离能越来越大:___________ ;
(b)结合数据说明为什么Mg的常见化合价为+2价:___________ 。
 )是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
)是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
 分子的电子式为
分子的电子式为②
 分子中,与N原子相连的H显正电性。则电负性:N
分子中,与N原子相连的H显正电性。则电负性:N 分子的VSEPR理想模型的名称为
分子的VSEPR理想模型的名称为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较第一电离能的大小:Mg
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
电离能 | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(b)结合数据说明为什么Mg的常见化合价为+2价:
您最近一年使用:0次
名校
3 . 回答下列问题
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
根据表中数据判断其中的金属元素为___________ ,稀有气体元素为___________ ,显正二价的金属元素是___________ 。(填字母)
(2)水分子是H2O而不是H3O,是因为共价键具有___________ 性;水分子的键角为105°,是因为共价键具有___________ 性。
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为___________ 。
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为___________ 。
(1)现有5种元素A、B、C、D、E,其中有3种金属元素,1种稀有气体元素,其I1~I3分别如下表。
| 元素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
(2)水分子是H2O而不是H3O,是因为共价键具有
(3)1mol乙酸分子CH3COOH中含有的π键与σ键的数目之比为
(4)已知NH5为离子化合物,则1molNH5晶体中含有的共价键数目为
您最近一年使用:0次
4 . 不同元素的第一电离能 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
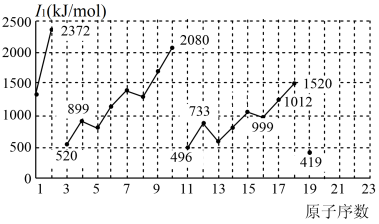
(1)总结同主族内不同元素的 变化的特点
变化的特点______ 。
(2)同周期内,随原子序数增大, 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是_______ (填序号)。
① (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)
③ (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)
(3)解释10号元素 较大的原因
较大的原因______ 。
(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围______ 。
 如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
如下图所示。试根据元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列问题。
(1)总结同主族内不同元素的
 变化的特点
变化的特点(2)同周期内,随原子序数增大,
 增大。但个别元素的
增大。但个别元素的 出现反常,试预测下列关系中正确的是
出现反常,试预测下列关系中正确的是①
 (砷)>
(砷)>  (硒) ②
(硒) ② (砷)<
(砷)<  (硒)
(硒)③
 (溴) >
(溴) >  (硒) ④
(硒) ④ (溴) <
(溴) <  (硒)
(硒)(3)解释10号元素
 较大的原因
较大的原因(4)请估计1mol气态基态Ca原子失去最外层一个电子所需能量E的范围
您最近一年使用:0次
5 . 下表为 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。
分析上表中各元素电离能的变化,回答下列问题:
(1) 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是__________
(2)为什么同一元素的各级电离能逐级增大?__________
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?__________
 、
、 、
、 的部分电离能(
的部分电离能( )数值。
)数值。| 电离能 | 元素 | ||
 |  |  | |
 | 496 | 738 | 577 |
 | 4562 | 1451 | 1817 |
 | 6912 | 7733 | 2745 |
 | 9543 | 10540 | 11575 |
(1)
 、
、 、
、 元素的第一电离能从大到小的顺序是
元素的第一电离能从大到小的顺序是(2)为什么同一元素的各级电离能逐级增大?
(3)上表中所呈现的电离能变化规律与三种元素的原子结构有什么关联?
您最近一年使用:0次
6 . 试用原子结构的知识解释下列实验事实。
(1)在第2周期元素中,氖的第一电离能最大。_______
(2)磷的第一电离能比硫的第一电离能大。_______
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子( )。
)。_______
(4) 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。_______
(1)在第2周期元素中,氖的第一电离能最大。
(2)磷的第一电离能比硫的第一电离能大。
(3)在化学反应中,镁原子通常失去两个电子,形成镁离子(
 )。
)。(4)
 是离子化合物,
是离子化合物, 是共价化合物。
是共价化合物。
您最近一年使用:0次
名校
7 . 根据元素周期表和周期律相关知识,回答下列问题:
(1)C、N、O三种元素电负性由大到小排序_______ ,第一电离能由小到大排序_______ ;
(2)①O2-,②Al3+,③Cl-,④Ca2+的半径由大到小排列为:_______ (用序号表示);
(3)元素非金属性Cl_______ S(填“>”或“<”),请举例证明:_______ (可用方程式或客观事实回答);
(4)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:_______ 。
(1)C、N、O三种元素电负性由大到小排序
(2)①O2-,②Al3+,③Cl-,④Ca2+的半径由大到小排列为:
(3)元素非金属性Cl
(4)由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出Be(OH)2与NaOH反应的化学方程式:
您最近一年使用:0次
名校
8 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ ,占据最高能级电子的电子云轮廓图为___________ 形。
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②比较Mg、Ca第一电离能的大小:___________ 。O的第一电离能小于N,原因是___________ 。
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
结合数据说明Mg的常见化合价为+2价的原因:___________ 。
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为___________ ,铁在元素周期表中的位置___________ 。
②比较Li+与H-的半径大小关系:r(Li+)___________ r(H-)(填“>”或“<”)。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
②NH3分子中,与N原子相连的H显正电性。N、H电负性大小顺序为
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②比较Mg、Ca第一电离能的大小:
③下表的数据从上到下是钠、镁、铝逐级失去电子的电离能。
| 元素 | Na | Mg | Al |
| 电离能(kJ/mol) | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(3)我国科研人员研制出了“Fe—LiH”催化剂,温度、压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Fe原子的核外电子排布式为
②比较Li+与H-的半径大小关系:r(Li+)
您最近一年使用:0次
2022-03-15更新
|
800次组卷
|
4卷引用:北京师范大学附属中学2021-2022学年高二上学期期末考试化学试题
9 . NH3在工农业生产中具有重要的作用,可以用来生产尿素(结构简式为: )等化学肥料,也可以用来制备一些配位化合物。
)等化学肥料,也可以用来制备一些配位化合物。
(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子的电子排布式:_______ 。
(2)工业上生产尿素的化学反应: ,则CO(NH2)2分子中C原子的杂化方式为
,则CO(NH2)2分子中C原子的杂化方式为_______ 。C、N、O三种元素的第一电离能由小到大的顺序为_______ 。
(3)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的 晶体,与该物质中的配体互为等电子体的阴离子的化学式为
晶体,与该物质中的配体互为等电子体的阴离子的化学式为_______ 。
(4)写出将过量氨水缓慢滴入硫酸铜溶液中发生反应的离子方程式:_______ 、_______ 。
 )等化学肥料,也可以用来制备一些配位化合物。
)等化学肥料,也可以用来制备一些配位化合物。(1)合成氨是人类科学技术上的一项重大突破,工业合成氨生产中常用铁触媒作催化剂。请写出Fe元素的基态原子的电子排布式:
(2)工业上生产尿素的化学反应:
 ,则CO(NH2)2分子中C原子的杂化方式为
,则CO(NH2)2分子中C原子的杂化方式为(3)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的
 晶体,与该物质中的配体互为等电子体的阴离子的化学式为
晶体,与该物质中的配体互为等电子体的阴离子的化学式为(4)写出将过量氨水缓慢滴入硫酸铜溶液中发生反应的离子方程式:
您最近一年使用:0次
解题方法
10 . 根据已学知识,回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是____ ,占据该能层电子的电子云轮廓图形状为____ 。
(2)写出3p轨道上有2个未成对电子的元素的符号____ 或____ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是____ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式____ ;在元素周期表中,该元素在____ (填“s”“p”“d”“f”或“ds”)区。
(5)写出与N同主族的As的基态原子的核外电子排布式____ 。
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为____ 。
(7)写出Fe2+的核外电子排布式:____ 。
(8)Zn2+的核外电子排布式为____ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)写出与N同主族的As的基态原子的核外电子排布式
(6)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(7)写出Fe2+的核外电子排布式:
(8)Zn2+的核外电子排布式为
您最近一年使用:0次



