1 . 铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe原子价电子排布图为___________ 。
(2)丙酮( )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是___________ ,C、N、O第一电离能由大到小的顺序为___________ 。
(3)C、H、O三种元素的电负性由小到大的顺序为___________ 。
(4)乙醇的沸点高于丙酮,这是因为___________ 。
(1)Fe原子价电子排布图为
(2)丙酮(
 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)C、H、O三种元素的电负性由小到大的顺序为
(4)乙醇的沸点高于丙酮,这是因为
您最近一年使用:0次
2 . (1)可正确表示原子轨道的是___________ 。
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的价电子排布式:___________ 。
(3)下列物质中,只含有极性键的分子是_____ ,既含离子键又含共价键的化合物是_______ ;只存在σ键的分子是_______ ,同时存在σ键和π键的分子是_____ 。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(4)用“>”“<”或“=”填空:第一电离能的大小:Mg____ Al;
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的价电子排布式:
(3)下列物质中,只含有极性键的分子是
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(4)用“>”“<”或“=”填空:第一电离能的大小:Mg
您最近一年使用:0次
名校
解题方法
3 . (1)短周期某主族元素,M的电离能情况如图A所示,则M在元素周期表的第_______ 族。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (写化学式)。a点所在折线元素氢化物的沸点变化规律如图B,呈现这种变化关系的原因是_______

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键_______ 。
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
亚磷酸 (H3PO3) 也是中强酸,它的结构式为_______ ;亚磷酸 (H3PO3)为_______ 元酸。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 |  |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
您最近一年使用:0次
2021-04-07更新
|
157次组卷
|
2卷引用:山西省太原市第五中学2020-2021学年高二下学期4月阶段性检测化学试题
4 . VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
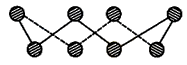
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是______ ;_______________ ;
(3)Se原子序数为_______ ,其核外M层电子的排布式为___________________ ;
(4)H2Se的酸性比H2S_________ (填“强”或“弱”)。气态SeO3分子的立体构型为______________ ,SO32-离子的立体构型为___________________ ;
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:_____________________________________ ;
② H2SeO4比 H2SeO3酸性强的原因:______________________________________________________________
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是
(3)Se原子序数为
(4)H2Se的酸性比H2S
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:
② H2SeO4比 H2SeO3酸性强的原因:
您最近一年使用:0次
2016-12-09更新
|
587次组卷
|
3卷引用:山西省晋中市新一双语学校2020-2021学年高二下学期3月月考化学试题



