1 . 按要求回答下列问题:
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为___________ ;元素Mn与O中,第一电离能较大的是___________ ,基态原子核外未成对电子数较多的是___________ 。
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为___________ 。
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。
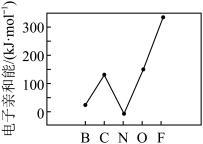
其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________ ,氮元素E1呈现异常的原因是___________ 。
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。

其中除氮元素外,其他元素的E1自左而右依次增大的原因是
您最近一年使用:0次
2022-10-20更新
|
210次组卷
|
10卷引用:广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题
广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)湖北省咸宁市嘉鱼县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)第一章 本章达标检测2河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题常州市武进区礼嘉中学2021-2022学年高二下学期第二次阶段测试化学试题湖南省衡阳县第四中学 2022-2023学年高二下学期开学摸底考试(平行班)化学试题(已下线)第一章 原子结构与性质(B卷)
2 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。
(1)元素b位于周期表中_______ 区,其基态原子核外有_______ 种运动状态不同的电子。
(2)基态c原子中有_______ 个未成对电子,其中能量最高的电子所在原子轨道的电子云轮廓图为_______ 形。
(3)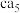 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为_______ 。
(4)基态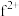 外围电子的电子排布图为
外围电子的电子排布图为_______ ,已知高温下化合物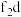 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因_______ 。
(5)b、c、d三种元素的第一电离能由大到小的顺序为_______ (填元素符号)。

(1)元素b位于周期表中
(2)基态c原子中有
(3)
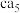 理论上为离子化合物,猜测其电子式为
理论上为离子化合物,猜测其电子式为(4)基态
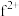 外围电子的电子排布图为
外围电子的电子排布图为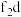 比化合物fd更稳定,试从核外电子排布的角度解释原因
比化合物fd更稳定,试从核外电子排布的角度解释原因(5)b、c、d三种元素的第一电离能由大到小的顺序为
您最近一年使用:0次
2021-07-09更新
|
899次组卷
|
6卷引用:广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题
广东省肇庆市2020-2021学年高二下学期末教学质量检测化学(物质结构与性质)试题(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第一章 原子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)广西南宁市2022-2023学年高二下学期开学考试化学试题江苏省无锡市市北高级中学2023-2024学年高二上学期期末检测化学试卷(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
名校
3 . 硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)Ga与B同主族,Ga的基态原子核外电子排布式为_______ ,第一电离能由大到小的顺序是_______ 。
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
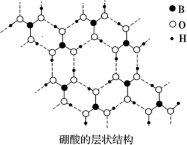
①硼酸中B原子的杂化轨道类型为_______ 。
②硼酸晶体中存在的作用力有范德华力和_______ 。
③加热时,硼酸的溶解度增大,主要原因是_______ 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:_______ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:_______ 。[BH4]-的空间构型是_______ 。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:_______ 。
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______ 。

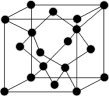
(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是_______ g· cm-3。(只要求列算式,不必计算出数值,阿伏加德罗常数用NA表示)。
(1)Ga与B同主族,Ga的基态原子核外电子排布式为
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。

①硼酸中B原子的杂化轨道类型为
②硼酸晶体中存在的作用力有范德华力和
③加热时,硼酸的溶解度增大,主要原因是
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为

(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是

您最近一年使用:0次
2021-01-18更新
|
1966次组卷
|
4卷引用:2021年广东省高考化学试卷变式题11-21
解题方法
4 . 铝、锌、铁在人类生产和生活中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Fe2+电子排布式为___ ,Zn的基态原子能级最高的电子的电子云轮廓图形状为___ 。
(2)已知Al的第一电离能为578kJ·mol-1、Mg的第一电离能为740kJ·mol-1,请解释Mg的第一电离能比Al大的原因___ 。
(3)Zn2+可形成[Zn(NH3)6]SO4络合物,1mol[Zn(NH3)6]2+配离子中含σ键___ mol,其阴离子中心原子的杂化方式是___ ,NH3的沸点高于PH3的原因是___ 。
(4)已知Zn2+等过渡元素离子形成的水合离子的颜色如下表所示:
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因:___ 。
(5)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为___ ,其中Fe的配位数为___ 。
(6)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为xcm,高为ycm,NA为阿伏加 德罗常数的值,则晶胞的密度为___ g·cm-3(列出计算式即可)。

(1)Fe2+电子排布式为
(2)已知Al的第一电离能为578kJ·mol-1、Mg的第一电离能为740kJ·mol-1,请解释Mg的第一电离能比Al大的原因
(3)Zn2+可形成[Zn(NH3)6]SO4络合物,1mol[Zn(NH3)6]2+配离子中含σ键
(4)已知Zn2+等过渡元素离子形成的水合离子的颜色如下表所示:
| 离子 | Sc3+ | Cr3+ | Fe2+ | Zn2+ |
| 水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Sc3+、Zn2+的水合离子为无色的原因:
(5)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(6)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为xcm,高为ycm,NA为阿伏加 德罗常数的值,则晶胞的密度为

您最近一年使用:0次
2020-06-28更新
|
1995次组卷
|
4卷引用:2021年高考化学押题预测卷(广东卷)(01)
(已下线)2021年高考化学押题预测卷(广东卷)(01)2021年广东省高考化学试卷变式题11-21(已下线)2021年高考全国乙卷化学试题变式题重庆市江津中学、实验中学等七校2020届高三下学期6月联考(三诊)理科综合化学试题



