1 . 四种元素基态原子的电子排布式如下:① ;②
;② ;③
;③ ;④
;④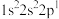 。下列有关比较中正确的是
。下列有关比较中正确的是
 ;②
;② ;③
;③ ;④
;④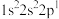 。下列有关比较中正确的是
。下列有关比较中正确的是| A.第一电离能:④>③>②>① | B.原子半径:④>③>①>② |
| C.电负性:③>④>①>② | D.最高正化合价:④=①>③=② |
您最近一年使用:0次
2024-01-24更新
|
141次组卷
|
7卷引用:陕西省西安市铁一中学2020-2021学年高二下学期期中考试化学试题
名校
解题方法
2 . 下列关于分子的结构和性质的描述错误的是
| A.碘易溶于四氯化碳溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
B.硫难溶于水,微溶于酒精,易溶于 ,说明分子极性: ,说明分子极性: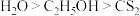 |
| C.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
D.乙醇分子(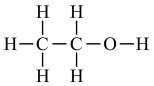 )中所有碳原子都是手性碳原子 )中所有碳原子都是手性碳原子 |
您最近一年使用:0次
名校
解题方法
3 . 已知:元素的电负性和元素的化合价一样,也是元素的一种基本性质;两成键元素间电负性差值大于1.7时,通常形成离子键,两成键元素间电负性差值小于1.7时,通常形成共价键。下表给出了14种元素的电负性,则下列说法错误的是
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
| A.随着原子序数递增,元素的电负性呈周期性变化 |
| B.元素电负性越大,其非金属性越强 |
| C.根据电负性数据可知Mg3N2中含有离子键 |
| D.BeCl2含金属元素铍,故属于离子化合物 |
您最近一年使用:0次
2023-07-29更新
|
99次组卷
|
6卷引用:陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题
陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题【全国百强校】重庆市第一中学2017-2018学年高一下学期期中考试化学试题江西省赣州市石城县石城中学2020-2021学年高一下学期3月月考化学试题(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)第一章 本章复习提升1云南省龙陵县第一中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
4 . 下列有关物质结构或性质的比较中,正确的是
A.熔点: |
B.键角: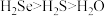 |
C.键的极性: 键 键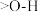 键 键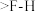 键 键 |
D.热稳定性: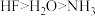 |
您最近一年使用:0次
5 . 已知元素X、Y同周期,且电负性X>Y,下列说法中一定不正确的是
| A.第一电离能:Y<X |
| B.X和Y形成的化合物中,X显负价,Y显正价 |
| C.最高价含氧酸的酸性:元素X对应酸的酸性强于Y |
| D.最简单气态氢化物的稳定性:HmY>HnX |
您最近一年使用:0次
2021-09-24更新
|
548次组卷
|
5卷引用:陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题
陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题北京市房山区2021-2022学年高二下学期期中考试化学试题江苏省南通市重点中学2021-2022学年高一下学期期中考试化学试题新疆新源县第二中学2020-2021学年高二下学期期末联考化学试题(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)
名校
解题方法
6 . 下列有关化学用语表述或性质比较正确的是
A.基态氧原子核外价电子排布轨道表示式 |
| B.磷化铜(Cu3P2)用于制造磷青铜,电负性:Cu<P |
C.用原子轨道描述氢分子中化学键的形成: |
D.在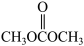 分子中, C 原子和O 原子均为 sp3杂化 分子中, C 原子和O 原子均为 sp3杂化 |
您最近一年使用:0次
2021-04-05更新
|
771次组卷
|
7卷引用:陕西省西北工业大学附中2020-2021学年高二下学期期中考试化学试题
名校
7 . 现有四种元素基态原子的电子排布式如下:① ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是
 ②
② ③
③ ④
④ 。则下列有关比较中正确的是
。则下列有关比较中正确的是| A.第一电离能:④>③>①>② | B.原子半径:④>③>②>① |
| C.电负性:④>③>①>② | D.最高正化合价:④>③=②>① |
您最近一年使用:0次
2021-02-01更新
|
1515次组卷
|
13卷引用:陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题
陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题重庆市朝阳中学2021-2022学年高二下学期期中考试化学试题湖北省武汉市钢城第四中学2021-2022学年高二下学期期中考试化学试题新疆维吾尔自治区塔城地区2022-2023学年高二下学期5月期中化学试题广东省揭阳市三所中学联考2022-2023学年高二下学期4月期中考试化学试题陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题(人教版2019)选择性必修2 阶段性综合评估测试卷(二)鲁科版2019选择性必修2阶段性综合评估测试卷(二)河北省石家庄市第二中学2022年高二寒假考试化学试题吉林省洮南市第一中学2022-2023学年高二下学期学习质量检测化学试卷江西省丰城拖船中学2022-2023学年高二下学期6月期末考试化学试题吉林省长春市新解放学校2022-2023学年高二下学期7月期末考试化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
8 . 如图为周期表的一小部分,A、B、C、D、E的位置关系如图所示。其中B元素最高化合价是最低化合价绝对值的3倍,它的最高价氧化物中含氧60%。下列说法正确的是( )
| A | ||
| D | B | E |
| C |
| A.D、B、E三种元素的第一电离能逐渐减小 |
| B.电负性:E>C |
| C.D、B、E三种元素形成的简单离子的半径逐渐增大 |
| D.气态氢化物的稳定性顺序:D>B>E |
您最近一年使用:0次
2020-06-09更新
|
342次组卷
|
9卷引用:陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题
陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题四川省西充中学 2021-2022 学年高二上学期期中考试化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 B素养拓展区专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第2课时 元素第一电离能和电负性的周期性变化福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(1卷)试题天津市耀华中学2022-2023学年高二上学期期末考试化学试题2.2.2元素第一电离能和电负性的周期性变化 课后湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题



