解题方法
1 . 下列说法正确的是
| A.元素的第一电离能越大,其金属性一定越强 |
| B.元素的第一电离能越小,其金属性一定越强 |
| C.同主族元素的单质从上到下,熔点升高 |
| D.一般情况下,金属单质与酸反应越容易,其元素的电负性越小 |
您最近一年使用:0次
名校
2 . N,N-二甲基甲酰胺[ ]是良好的溶剂。下列说法
]是良好的溶剂。下列说法不正确 的是
 ]是良好的溶剂。下列说法
]是良好的溶剂。下列说法| A.元素电负性大小:χ(N)<χ(O) | B.原子半径大小:r(C)<r(N) |
| C.分子中含σ键和π键 | D.该物质分子间存在范德华力 |
您最近一年使用:0次
2022-12-15更新
|
325次组卷
|
5卷引用: 浙江省丽水、湖州、衢州 2022 年 11 月三地市高三教学质量检测(一模)化学试题
浙江省丽水、湖州、衢州 2022 年 11 月三地市高三教学质量检测(一模)化学试题浙江省湖州市2023届高三上学期11月教学质量检测 化学试题(已下线)化学-2023年高考押题预测卷02(浙江卷)(含考试版、全解全析、参考答案、答题卡)(已下线)【2023】【高二下】【期中考试】【长河】【高中化学】【李鼎收集】湖北省武汉市第六中学2022~2023学年高二上学期第三次月考化学试题
22-23高二上·浙江·期末
解题方法
3 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布为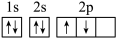 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_______ 。
(2)B元素的电负性_______ (填“大于”“小于”或“等于”)C元素的电负性。B元素的第一电离能_______ (填“大于”“小于”或“等于”)C元素的第一电离能。
(3)E基态原子中能量最高的电子,其电子云在空间有_______ 个方向。
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
(5)与F同周期,原子序数为24的元素M,其基态原子的核外电子排布式为_______ 。
(6)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是_______ 。
(7)AC 的空间结构为
的空间结构为_______ 中心原子的杂化轨道类型为_______ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)E基态原子中能量最高的电子,其电子云在空间有
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
A.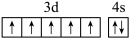 | B.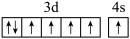 |
C.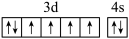 | D.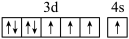 |
(6)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是
(7)AC
 的空间结构为
的空间结构为
您最近一年使用:0次
名校
解题方法
4 . 下列“类比”结果正确的是
| A.根据同周期元素的电负性变化趋势,推出Ar的电负性比Cl大 |
| B.CO2与足量Na2O2反应生成碳酸钠,则SO2与足量Na2O2反应生成亚硫酸钠 |
| C.Cu(OH)2可以溶解在浓氨水中,则Fe(OH)3也可以溶解在浓氨水中 |
| D.CH4的空间构型为正四面体型,则C(CH3)4碳骨架的空间构型为正四面体型 |
您最近一年使用:0次
2022-08-18更新
|
183次组卷
|
2卷引用:浙江省温州市瑞安中学2021-2022学年高二下学期开学考试化学试题
5 . 下列对于有机反应的原理说法不正确 的是
| A.卤代烃中C-X键电子对向C原子偏移,使X易以阴离子形式离去 |
| B.醛分子中羰基的吸电子作用,使醛基邻位碳原子上的氢容易离去 |
| C.羧酸中的氧原子电负性大,使碳氧键和氢氧键容易断裂 |
| D.苯酚分子中苯环使羟基的极性增强,使氢氧键容易断裂 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.原子能级中,p能级能量一定比s能级的能量高 |
| B.同主族元素中,从上到下元素的电负性逐渐变大 |
| C.键能、键长都是衡量共价键的稳定性重要参数 |
| D.元素周期表中,s区全部是金属元素 |
您最近一年使用:0次
7 . 如图是第二周期主族元素的某些性质随原子序数变化的柱形图,则y轴可表示

①第一电离能②电负性③原子半径④简单离子半径⑤最高正化合价⑥形成简单离子转移的电子数

①第一电离能②电负性③原子半径④简单离子半径⑤最高正化合价⑥形成简单离子转移的电子数
| A.② | B.①② | C.⑤ | D.②⑤ |
您最近一年使用:0次
名校
8 . 下列有关元素周期表及其分区的理解不正确的是
| A.元素周期表的每个周期中最后一种元素是稀有气体元素 |
| B.基态原子最外层电子排布为ns2的元素都位于周期表第IIA族 |
| C.主族元素处于元素周期表的s区和p区 |
| D.电负性最大的元素位于周期表的右上角(稀有气体除外) |
您最近一年使用:0次
2022-04-21更新
|
754次组卷
|
8卷引用:浙江省余姚中学2022-2023学年高二上学期期中考试化学试题
名校
9 . 氮化硅(Si3N4)陶瓷可代替金属制造发动机的耐热部件。工业上用气相沉淀法制备氨化硅: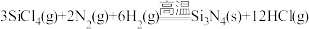 。请回答:
。请回答:
(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si___________ H(选填“<”或“>”)。
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是___________ 。
(3)氮化硅(Si3N4)的晶体类型为___________
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
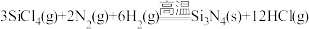 。请回答:
。请回答:(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是
(3)氮化硅(Si3N4)的晶体类型为
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
| A.是一种活泼的金属元素 |
| B.其电负性大于硫 |
| C.其单质可作为半导体材料 |
| D.其气态氢化物的稳定性低于硅的气态氢化物 |
您最近一年使用:0次
10 . 已知A、B、C、D、E、F六种元素在元素周期表中的位置如图,下列说法不正确 的是


| A.元素的电负性:A<B |
| B.元素的第一电离能:C<D |
| C.E元素原子最高能级的不同轨道都有电子 |
| D.F元素原子最外层只有一种自旋方向的电子 |
您最近一年使用:0次
2022-01-21更新
|
218次组卷
|
2卷引用:浙江省温州市2021-2022学年高二上学期期末教学质量统一检测化学试题



