1 . 2022年诺贝尔化学奖授予开发“点击化学”科学家。分子R称为“点击化学试剂”,如图所示。下列叙述错误的是
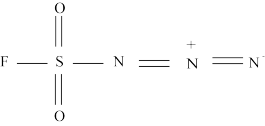
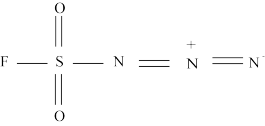
A.电负性: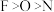 |
B.第一电离能: |
| C.S原子核外有6种运动状态不同的电子 |
| D.基态F原子核外电子占据3个能级 |
您最近一年使用:0次
2023-01-04更新
|
400次组卷
|
3卷引用:湖北省荆州市八县市2022-2023学年高二上学期期末联考化学试题
湖北省荆州市八县市2022-2023学年高二上学期期末联考化学试题(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(8-14)福建省泉州市三校2022-2023学年高二下学期4月期中联考化学试题
2 . I.雄黄( )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
(1)基态硫原子核外电子的运动轨道数有_______ 种;有___________ 种能量不同的电子;
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)S和As比较,电负性较大的是___________
(4)As元素的第一电离能___________ Se元素的第一电离能(填“大于”“小于”或“等于”),原因是_______________________________ 。
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是________ ,属于两性化合物,证明这一结论的有关离子方程式为__________________________ 、________________ 。
(6)若已知反应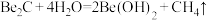 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______________________ 。
(7)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是________________ 。用电子式表示 的形成过程:
的形成过程:__________
 )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:(1)基态硫原子核外电子的运动轨道数有
(2)基态砷原子的价层电子的轨道表示式为
(3)S和As比较,电负性较大的是
(4)As元素的第一电离能
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是
(6)若已知反应
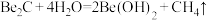 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(7)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次
名校
解题方法
3 . 某种化合物结构如图,X、Y、Z、Q、W为原子半径依次减小的短周期元素,分别位于三个不同的周期。下列说法错误的是


| A.Z的氧化物的水化物为强酸 |
| B.废弃的金属X可置于酒精中销毁 |
| C.电负性:Q>Z>Y>W>X |
| D.Z2W4和ZW3分子中Z原子的杂化方式相同 |
您最近一年使用:0次
2022-11-19更新
|
542次组卷
|
3卷引用:湖北省武汉市华中师范大学第一附属中学2022-2023学年高三上学期期中考试化学试题
湖北省武汉市华中师范大学第一附属中学2022-2023学年高三上学期期中考试化学试题湖北省武汉市第六中学2022~2023学年高二上学期第三次月考化学试题(已下线)专题02 分子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
名校
4 . 光气( )是一种重要的有机中间体。利用反应可
)是一种重要的有机中间体。利用反应可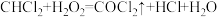 用于制备光气。下列有关叙述正确的是
用于制备光气。下列有关叙述正确的是
 )是一种重要的有机中间体。利用反应可
)是一种重要的有机中间体。利用反应可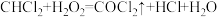 用于制备光气。下列有关叙述正确的是
用于制备光气。下列有关叙述正确的是A. 为非极性分子 为非极性分子 | B. 的电子式为 的电子式为 |
C. 、 、 分子间均能形成氢键 分子间均能形成氢键 | D.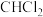 中电负性最小的元素是Cl 中电负性最小的元素是Cl |
您最近一年使用:0次
2022-08-17更新
|
105次组卷
|
3卷引用:湖北省新高考联考协作体2021-2022学年高三下学期2月联考化学试题
5 . 下列有关物质的结构与性质说法错误的是
| A.石墨晶体中,层内导电性强于层间导电性 |
B.工业盐酸中,因含有 而呈亮黄色 而呈亮黄色 |
C.氟的电负性大于氯,所以三氟乙酸的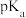 比三氯乙酸大 比三氯乙酸大 |
D.干冰中 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关 的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关 |
您最近一年使用:0次
名校
解题方法
6 . Fe、HCN与K2CO3在一定条件下发生如下反应:Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,下列说法正确的是
| A.此化学方程式中涉及的第二周期元素的电负性大小的顺序为O<N<C |
B.配合物K4Fe(CN)6的中心离子的价电子排布图为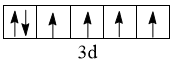 ,该中心离子的配位数是10 ,该中心离子的配位数是10 |
| C.1molHCN分子中含有σ键的数目为1.204×1024 |
| D.K2CO3中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 |
您最近一年使用:0次
2022-06-13更新
|
325次组卷
|
8卷引用:湖北省罗田县第一中学2021-2022学年高二下学期6月月考化学试题(实验班)
解题方法
7 . W、X、Y、Z是同周期主族元素,Y的最外层电子数是X次外层电子数的3倍,四种元素与锂组成的盐是一种新型的锂离子电池的电解质(结构如图,箭头指向表示共用电子对由W提供)。下列说法正确的是
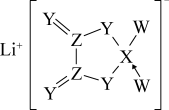

| A.原子半径:Z<Y |
| B.电负性:Y> W >Z |
| C.X的最高价氧化物对应的水化物是强酸 |
| D.该物质中W原子满足8电子稳定结构。 |
您最近一年使用:0次
名校
8 . 现有几种元素的基态离子(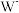 、
、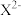 、
、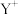 、
、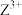 ),其核外电子排布式均为
),其核外电子排布式均为 ,下列有关叙述正确的是
,下列有关叙述正确的是
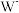 、
、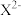 、
、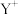 、
、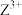 ),其核外电子排布式均为
),其核外电子排布式均为 ,下列有关叙述正确的是
,下列有关叙述正确的是| A.原子半径:Y>Z>X>W |
| B.最高正化合价:W>X>Z>Y |
| C.电负性:W>X>Y>Z |
| D.第一电离能:X>W>Z>Y |
您最近一年使用:0次
2022-03-31更新
|
149次组卷
|
2卷引用:湖北省部分学校2021-2022学年高二下学期3月联考化学试题
名校
9 . 四种元素基态原子的电子排布式如下:① ;②
;②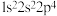 ;③
;③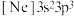 ;④
;④ 。下列有关比较中错误的是
。下列有关比较中错误的是
 ;②
;②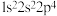 ;③
;③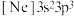 ;④
;④ 。下列有关比较中错误的是
。下列有关比较中错误的是| A.第一电离能:①>②>③>④ | B.原子半径:④>③>①>② |
| C.电负性:①>②>③>④ | D.最简单氢化物的沸点:②>①>③>④ |
您最近一年使用:0次
2022-01-28更新
|
251次组卷
|
2卷引用:湖北省十堰市2021-2022学年高三上学期元月期末调研考试化学试题
10 . 硅是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态硅(Si)原子的核外电子排布式为[Ne]_______ ,有_______ 个未成对电子。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态Ge原子的核外电子占据_______ 个能层、_______ 个能级。
②上述三种元素的电负性由大到小的顺序为_______ (填元素符号)。
③固态CO2可用于人工降雨,SiO2常用于_______ (填一种即可)。
④请写出高温条件下碳和二氧化硅反应的化学方程式:_______ 。
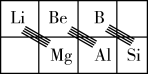
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Si与NaOH反应生成Na2SiO3和H2,则B与NaOH反应生成_______ (填化学式)和H2。
(1)基态硅(Si)原子的核外电子排布式为[Ne]
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①基态Ge原子的核外电子占据
②上述三种元素的电负性由大到小的顺序为
③固态CO2可用于人工降雨,SiO2常用于
④请写出高温条件下碳和二氧化硅反应的化学方程式:
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Si与NaOH反应生成Na2SiO3和H2,则B与NaOH反应生成

您最近一年使用:0次
2022-01-27更新
|
325次组卷
|
3卷引用:湖北省十堰市2021-2022学年高二上学期元月期末调研考试化学试题



