名校
1 . 已知冰醋酸能与 在
在 催化下发生反应生成
催化下发生反应生成 和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是
和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是
 在
在 催化下发生反应生成
催化下发生反应生成 和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是
和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是| A.实验中C―I键的产生,可通过红外光谱结果证明 |
B. 中存在 中存在 键 键 |
| C.C―I键比C―Cl键更易形成,且键能更大 |
D. 的酸性比 的酸性比 强 强 |
您最近一年使用:0次
名校
2 . 临床证明磷酸氯喹对治疗“新冠肺炎”有良好的疗效,磷酸氯喹的结构如图所示。下列有关磷酸氯喹的说法错误的是
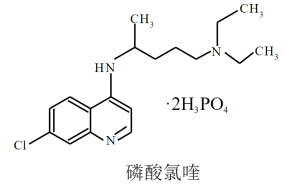

| A.磷酸氯喹既能与强酸、又能与强碱反应 |
| B.磷酸氯喹中C、N、O元素的电负性大小顺序是:N>O>C |
| C.磷酸氯喹中的N—H键的键能大于C—H键的键能 |
| D.磷酸氯喹结构中存在σ键、大π键等 |
您最近一年使用:0次
2022-07-14更新
|
542次组卷
|
2卷引用:黑龙江省哈尔滨市宾县第二中学2022-2023学年高二下学期第二次月考化学试题
解题方法
3 . 氢、氮、硫、氯、铜是元素周期表中前四周期元素。回答下列问题:
(1)氮在元素周期表中的位置_____ 。写出 的电子式
的电子式_____ , 的分子空间构型为
的分子空间构型为_____ , 中心原子的杂化方式为
中心原子的杂化方式为_____ 。
(2)氯与硫相比,非金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是_____ (填序号)。
a.常温下氯的单质呈气态,硫的单质呈固态 b.稳定性
c.酸性: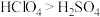 d.氯的电负性大于硫的电负性
d.氯的电负性大于硫的电负性
(3) 组成元素中,第一电离能最大的元素是
组成元素中,第一电离能最大的元素是_____ (用元素符号表示); 中含有
中含有 键数目为
键数目为_____ 。
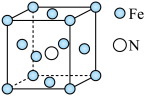
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为_____ ;设晶胞边长为 ,该晶体的密度为
,该晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
(1)氮在元素周期表中的位置
 的电子式
的电子式 的分子空间构型为
的分子空间构型为 中心原子的杂化方式为
中心原子的杂化方式为(2)氯与硫相比,非金属性较强的是
a.常温下氯的单质呈气态,硫的单质呈固态 b.稳定性

c.酸性:
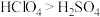 d.氯的电负性大于硫的电负性
d.氯的电负性大于硫的电负性(3)
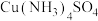 组成元素中,第一电离能最大的元素是
组成元素中,第一电离能最大的元素是 中含有
中含有 键数目为
键数目为(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为
 ,该晶体的密度为
,该晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。
您最近一年使用:0次
解题方法
4 . 钛、钒、铬、铁、镍、铜等过渡金属及其化合物在工业上有重要用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①基态 原子价层电子排布式为
原子价层电子排布式为___________ 。
②基态 原子核外电子的运动状态有
原子核外电子的运动状态有___________ 种。
(2)Ti的四卤化物熔点如下表所示,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
(3)制备 的反应为
的反应为 。
。
①上述化学方程式中非金属元素电负性由小到大的顺序为___________ (用元素符号表示)。
② 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中π键和σ键的个数比为
分子中π键和σ键的个数比为___________ ,中心原子的杂化方式为___________ 。
(4)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:___________ 。
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是___________ 。
③能准确证明该钒的硫化物是晶体的最可靠的科学方法是___________ 。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
①基态
 原子价层电子排布式为
原子价层电子排布式为②基态
 原子核外电子的运动状态有
原子核外电子的运动状态有(2)Ti的四卤化物熔点如下表所示,自
 至
至 熔点依次升高,原因是
熔点依次升高,原因是| 化合物 |  |  |  |
| 熔点/℃ | -24.12 | 38.3 | 155 |
(3)制备
 的反应为
的反应为 。
。①上述化学方程式中非金属元素电负性由小到大的顺序为
②
 分子中所有原子均满足8电子稳定结构,
分子中所有原子均满足8电子稳定结构, 分子中π键和σ键的个数比为
分子中π键和σ键的个数比为(4)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:
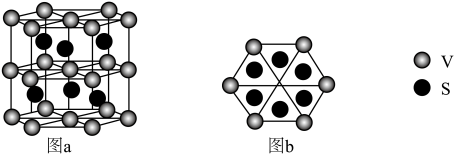
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是
③能准确证明该钒的硫化物是晶体的最可靠的科学方法是
您最近一年使用:0次
5 . 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)A原子的核外电子的原子轨道有___________ 个伸展方向。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为___________ (填元素符号)。
(3)E元素基态原子的电子排布式为___________ 。
(4)B2A4是重要的石油化工原料,其形成的高聚物的结构简式为___________ 。
(5)D元素与氟元素相比,电负性:D___________ (填“>”“=”或“<”)F,下列表述中能证明这一事实的是___________ (填字母)。
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(6)以下原子的电子排布式不符合洪特规则的是___________。
(1)A原子的核外电子的原子轨道有
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为
(3)E元素基态原子的电子排布式为
(4)B2A4是重要的石油化工原料,其形成的高聚物的结构简式为
(5)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(6)以下原子的电子排布式不符合洪特规则的是___________。
| A.1s22s22p63s23p63d74s2 | B.1s22s22p63s23p63d44s2 |
| C.1s22s22p63s23p63d104s24p1 | D.某原子的外围电子的轨道表示式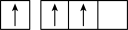 |
您最近一年使用:0次
6 . W、X、Y、Z四种短周期元素的原子序数 。四种元素原子结构描述如下:
。四种元素原子结构描述如下:
(1)根据上述信息Z元素基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,轨道呈___________ 形。
(2)元素W位于元素周期表的第___________ 周期第___________ 族,该原子的价电子轨道表示式为___________ 。
(3)Y、Z的电负性:___________ >___________ (填元素符号),两元素形成的化合物的电子式___________ 。
(4)X的基态原子核外电子排布式为___________ ,该元素位于元素周期表的___________ 区。
(5)下列事实能证明W的活泼性大于X的事实是___________。
 。四种元素原子结构描述如下:
。四种元素原子结构描述如下:| X | 原子核外s电子与p电子数之比为 |
| W | 原子的最外层没有p电子,且同周期中第一电离能最小 |
| Y | 原子最外层s电子与p电子数之比为 |
| Z | 原子核外电子中p电子数比Y原子多2个 |
(2)元素W位于元素周期表的第
(3)Y、Z的电负性:
(4)X的基态原子核外电子排布式为
(5)下列事实能证明W的活泼性大于X的事实是___________。
| A.W能与冷水反应,而X不能 | B.W最外层有一个电子,X最外层有两个电子 |
C.碱性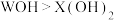 | D.W能从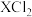 的溶液中把X置换出来 的溶液中把X置换出来 |
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D、E、F均是短周期元素,其原子序数依次增大,A和B同周期,A和E同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C、D的阳离子电子层结构相同,C与B可生成C2B或C2B2,D的阳离子半径是同周期最小的,F的原子半径是所在周期中最小的。请回答:
(1)E在元素周期表中的位置是_______ 。
(2)C所在周期电负性最强的是_______ ;AB2的结构式是_______ 。
(3)B、C、F的离子半径由大到小的顺序为_______ (用化学式回答,下同);A、D、E元素的最高价氧化物对应水化物中,酸性最强的是_______ 。
(4)B的简单氢化物比H2S沸点高的原因是_______ 。
(5)C与D两元素的最高价氧化物对应水化物反应的离子方程式:_______ 。
(6)用一个离子方程式证明A、E的非金属性强弱:_______ 。
(1)E在元素周期表中的位置是
(2)C所在周期电负性最强的是
(3)B、C、F的离子半径由大到小的顺序为
(4)B的简单氢化物比H2S沸点高的原因是
(5)C与D两元素的最高价氧化物对应水化物反应的离子方程式:
(6)用一个离子方程式证明A、E的非金属性强弱:
您最近一年使用:0次
解题方法
8 . 1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题:
(1)预测周期表中电负性最大的元素应为_______ ;估计钙元素的电负性的取值范围:_______ <X<_______ 。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为_______ 。
(3)请你预测Br与I元素的X数值的大小关系:X(Br)_______ X(I)。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_______ 原子(填元素符号)。
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是_______ ;
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:_______ 。
(7)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
(3)请你预测Br与I元素的X数值的大小关系:X(Br)
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)根据表中的所给数据分析: 同主族内的不同元素的X值变化的规律是
(6)化合物NaH能与水反应产生氢气,所以可用做生氢剂,写出该反应的化学方程式:
(7)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:HCl>H2S
B.两元素的电负性:S<Cl
C.最高价含氧酸的酸性:HClO4>H2SO4
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:Cl2+H2S=2HCl+S↓
您最近一年使用:0次
解题方法
9 . 如图所示是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
回答下列问题:
(1)元素为24号元素,其基态原子的价层电子轨道表示式(或价层电子排布图)为___________ 。
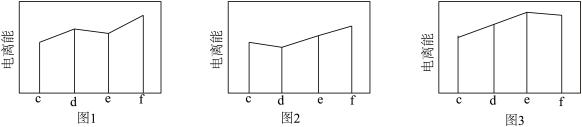
(2)图1、2、3分别表示c、d、e、f四种元素的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是图___________ (填序号),判断的依据是___________ 。
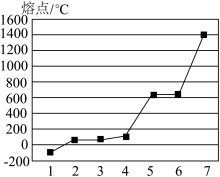
(3)第三周期7种主族元素按单质熔点高低的顺序排列如图所示,其中电负性最大的是___________ (填图中的序号)。
(4)键角:ce2___________ a2e(填“>”或“<”)。
(5)在l与p中,其单质的氧化性较强的是___________ (填元素符号),设计实验加以证明:___________
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | p | ||||||||||||||||
(1)元素为24号元素,其基态原子的价层电子轨道表示式(或价层电子排布图)为
(2)图1、2、3分别表示c、d、e、f四种元素的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是图

(3)第三周期7种主族元素按单质熔点高低的顺序排列如图所示,其中电负性最大的是

(4)键角:ce2
(5)在l与p中,其单质的氧化性较强的是
您最近一年使用:0次
名校
10 . I、下表为长式周期表的一部分,其中的编号代表对应的元素。请依据下表回答下列问题:

(1)写出元素⑩的一价离子的核外电子排布式:___________ ,该元素属于___________ 区元素。
(2)在标号 的主族元素 中,电负性最大的是___________ (填元素符号 )。
(3)元素④⑥⑦的气态氢化物热稳定性由强到弱 的顺序为:___________ (填化学式 )。
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式___________ 。
II.利用如图装置可验证同主族元素非金属性的变化规律。

(5)仪器A的名称为___________ 。
(6)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是___________ ,此装置存在的不足之处是___________ 。

(1)写出元素⑩的一价离子的核外电子排布式:
(2)在
(3)元素④⑥⑦的气态氢化物热稳定性由
(4)已知周期表中存在对角相似规则,如②与⑤在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑨的氢氧化物反应的化学方程式
II.利用如图装置可验证同主族元素非金属性的变化规律。

(5)仪器A的名称为
(6)若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4反应一段时间后,将C振荡、静置,观察到C中现象是
您最近一年使用:0次



