名校
解题方法
1 . 铁触媒是重要的催化剂,铁触媒在500 ℃左右时的活性最大,这也是合成氨反应一般选择在500 ℃左右进行的重要原因之一。CO易与铁触媒作用导致其失去催化活性:Fe+5CO===Fe(CO)5;在溶液中除去CO的化学方程式为[Cu(NH3)2]OOCCH3+CO+NH3 = 刹[Cu(NH3)3(CO)]OOCCH3。请回答下列问题:
(1)基态Fe原子的核外电子排布式为[Ar]___ ;C、N、O的电负性由大到小的顺序为______ 。
(2)Cu2+在水中呈现蓝色是因为形成了四水合铜(Ⅱ)离子,其化学式为______ ;配合物[Cu(NH3)2]OOCCH3中,铜显___ 价,碳原子的杂化轨道类型是______ ,NH3价电子对互斥理论模型是______ 。
(3)用[Cu(NH3)2]OOCCH3溶液除去CO的反应中,肯定有________ (填字母)形成。
A.离子键 B.配位键 C.非极性键 D.σ键
(4)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是________ 。
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为________ ,面心立方堆积与体心立方堆积的两种铁晶体的密度之比为________ (写出已化简的比例式即可)。(两种堆积中最邻近的铁原子的核间距相等)

(1)基态Fe原子的核外电子排布式为[Ar]
(2)Cu2+在水中呈现蓝色是因为形成了四水合铜(Ⅱ)离子,其化学式为
(3)用[Cu(NH3)2]OOCCH3溶液除去CO的反应中,肯定有
A.离子键 B.配位键 C.非极性键 D.σ键
(4)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为

您最近一年使用:0次
2019-05-07更新
|
428次组卷
|
2卷引用:【全国百强校】福建省莆田第一中学2019届高三下学期第四次月考理科综合化学试题
解题方法
2 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
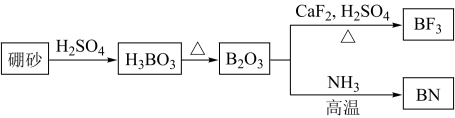
请回答下列问题:
(1)由B2O3制备BN的化学方程式是_____________________________________ ;
(2)B和N相比,电负性较大的是__________ ,BN中B元素的化合价为__________ ;
(3)在BF3分子中,F—B—F的键角是________ , B原子的杂化轨道类型为________ ;
(4)BF3和过量NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为________ ;
(5)六方氮化硼与石墨相似,层内B原子与N原子之间的化学键为_________ ,N原子L层的P电子比S电子多_________ 个。
(6)写出CaF2的电子式:________ 。

请回答下列问题:
(1)由B2O3制备BN的化学方程式是
(2)B和N相比,电负性较大的是
(3)在BF3分子中,F—B—F的键角是
(4)BF3和过量NaF作用可生成NaBF4,BF
 的立体构型为
的立体构型为(5)六方氮化硼与石墨相似,层内B原子与N原子之间的化学键为
(6)写出CaF2的电子式:
您最近一年使用:0次



