名校
解题方法
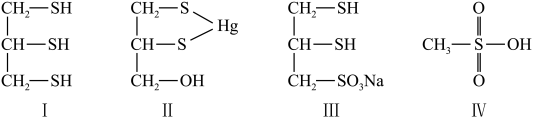
1 . 很多含巯基(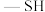 )的有机化合物是重金属元素汞和钛的解毒剂。如图中的解毒剂化合物I可与氧化汞生成化合物Ⅱ,化合物Ⅲ也是一种汞解毒剂,化合物Ⅳ是一种强酸,下列说法正确的是
)的有机化合物是重金属元素汞和钛的解毒剂。如图中的解毒剂化合物I可与氧化汞生成化合物Ⅱ,化合物Ⅲ也是一种汞解毒剂,化合物Ⅳ是一种强酸,下列说法正确的是
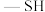 )的有机化合物是重金属元素汞和钛的解毒剂。如图中的解毒剂化合物I可与氧化汞生成化合物Ⅱ,化合物Ⅲ也是一种汞解毒剂,化合物Ⅳ是一种强酸,下列说法正确的是
)的有机化合物是重金属元素汞和钛的解毒剂。如图中的解毒剂化合物I可与氧化汞生成化合物Ⅱ,化合物Ⅲ也是一种汞解毒剂,化合物Ⅳ是一种强酸,下列说法正确的是
| A.Ⅲ比I的熔沸点高 | B.在II中S元素的电负性最大 |
C.在Ⅲ中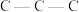 键角是 键角是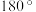 | D.在IV中硫氧键的键能均相等 |
您最近一年使用:0次
2023-11-21更新
|
59次组卷
|
2卷引用:江西省南昌市外国语学校2023-2024学年高三上学期10月月考化学试题
名校
2 . 第ⅢA和第ⅤA元素可形成多种化合物。请回答:
(1)基态B原子核外电子占据的最高能级符号是___________ ,基态As原子的价层电子排布式是___________ 。
(2)①固体储氢材料氨硼烷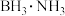 ,其结构和乙烷相似,下列有关说法正确的是
,其结构和乙烷相似,下列有关说法正确的是______ 。
A.氨硼烷中B原子的杂化方式为
B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素 形成的化合物中配位键的强度:
形成的化合物中配位键的强度:
________ 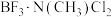 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是________ 。
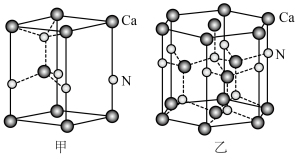
(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为___________ ,每个N原子周围距离最近的N原子数目为________ 。
(1)基态B原子核外电子占据的最高能级符号是
(2)①固体储氢材料氨硼烷
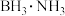 ,其结构和乙烷相似,下列有关说法正确的是
,其结构和乙烷相似,下列有关说法正确的是A.氨硼烷中B原子的杂化方式为

B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素
D. 是硼原子能量最低的激发态
是硼原子能量最低的激发态
 形成的化合物中配位键的强度:
形成的化合物中配位键的强度:
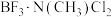 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为
您最近一年使用:0次
2023-11-15更新
|
607次组卷
|
4卷引用:江西省抚州市黎川县第二中学2023-2024学年高三上学期11月期中化学试题
江西省抚州市黎川县第二中学2023-2024学年高三上学期11月期中化学试题浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题10 物质结构与性质综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
解题方法
3 . 四种短周期主族元素在元素周期表中的相对位置如图所示,且X、Y、Z和Q四种元素的p轨道电子总数为24。化学家鲍林以Y的电负性作为参照标准,得出了各元素的电负性。下列叙述错误的是
| X | Y | |||
| Z | Q |
| A.最简单氢化物的稳定性:Y>Q>Z |
B. 分子中每个原子最外层都达到8电子稳定结构 分子中每个原子最外层都达到8电子稳定结构 |
| C.最高价氧化物对应水化物的酸性: Z<Q |
D.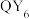 分子呈正八面体形 分子呈正八面体形 |
您最近一年使用:0次
2023-10-28更新
|
341次组卷
|
2卷引用:江西省部分高中学校2023-2024学年高三上学期10月联考化学试题
解题方法
4 . CrO2Cl2可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。下列说法正确的是
| A.CCl4为极性分子 | B.熔点:KCl>COCl2 |
| C.电负性:C>Cl | D.KCl含有非极性键 |
您最近一年使用:0次
2023-09-24更新
|
45次组卷
|
2卷引用:江西红色十校2024届高三上学期9月联考化学试题
名校
5 .  晶体具有优良的光学和物理学特性,被广泛应用于一些高科技领域。下列说法正确的是
晶体具有优良的光学和物理学特性,被广泛应用于一些高科技领域。下列说法正确的是
 晶体具有优良的光学和物理学特性,被广泛应用于一些高科技领域。下列说法正确的是
晶体具有优良的光学和物理学特性,被广泛应用于一些高科技领域。下列说法正确的是A.基态原子未成对电子数: |
B.电负性: |
C. 存在非极性键 存在非极性键 |
D.基态 原子核外电子的运动状态有5种 原子核外电子的运动状态有5种 |
您最近一年使用:0次
2023-09-10更新
|
107次组卷
|
2卷引用:江西省南昌市2023-2024学年高三上学期开学考试化学试题
解题方法
6 . 离子键的百分数是依据电负性的差值计算出来的,差值越大,离子键的百分数越大,下列几种化合物的化学键中离子键的百分数最大的是
| A.LiF | B.AlCl3 | C.MgO | D.SO3 |
您最近一年使用:0次
2023-09-09更新
|
110次组卷
|
3卷引用:江西省部分高中学校2024届高三上学期9月第一次联考化学试题
名校
7 . 我国疾控中心利用尿素(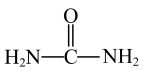 )制备出了两种低温消毒剂:三聚氰酸(
)制备出了两种低温消毒剂:三聚氰酸(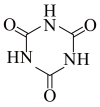 )和二氯异氰尿酸钠(
)和二氯异氰尿酸钠(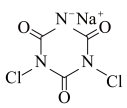 )。已知:尿素分子中所有原子共平面。下列说法错误的是
)。已知:尿素分子中所有原子共平面。下列说法错误的是
 )制备出了两种低温消毒剂:三聚氰酸(
)制备出了两种低温消毒剂:三聚氰酸( )和二氯异氰尿酸钠(
)和二氯异氰尿酸钠( )。已知:尿素分子中所有原子共平面。下列说法错误的是
)。已知:尿素分子中所有原子共平面。下列说法错误的是A.尿素分子中键角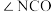 与键角 与键角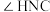 基本相等 基本相等 |
| B.二氯异氰尿酸钠中存在的化学键只有极性键、离子键 |
| C.基态氮原子的电子的空间运动状态有5种 |
D.二氯异氰尿酸钠中元素的电负性: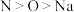 |
您最近一年使用:0次
名校
8 . 冠醚(R,结构如下)是由多个二元醇分子之间失水形成的环状化合物。冠醚与 发生的反应为如下,下列说法正确的是
发生的反应为如下,下列说法正确的是
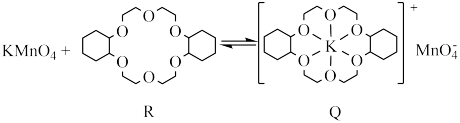
 发生的反应为如下,下列说法正确的是
发生的反应为如下,下列说法正确的是
| A.常温下,R易溶于水 |
B. 元素位于周期表中 元素位于周期表中 区 区 |
C.Q分子中,非金属元素之间的电负性: |
| D.R分子中所有的氧原子最外层均达到8电子稳定结构 |
您最近一年使用:0次
2023-08-20更新
|
176次组卷
|
3卷引用:江西省赣州市全南中学2023-2024学年高三上学期开学考试化学试题
名校
9 . 近日,科学家实现Rh催化苯乙烯的不对称氢硒化反应,如图所示。(注明:Ph为苯基,KH、KD代表速率常数)
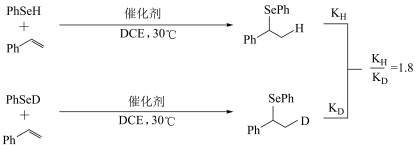
已知:C、Se、H的电负性依次为2.5、2.4、2.1。
下列叙述正确的是

已知:C、Se、H的电负性依次为2.5、2.4、2.1。
下列叙述正确的是
| A.苯乙烯不对称硒化反应属于加成反应 |
| B.相同条件下,氘、氕代速率不同的原因是它们质子数相等 |
| C.产物中碳硒键中共用电子对偏离碳原子 |
| D.上述转化中碳原子的杂化类型保持不变 |
您最近一年使用:0次
2023-08-16更新
|
119次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高三上学期开学考试化学试题
名校
10 . 某食品添加剂的主要成分为WZ(RY4)2·12X2Y。已知X、Y、Z、R、W为原子序数依次增大的前20号元素,X、Z的周期序数等于主族序数,Y和R位于同主族,基态X、W原子最外层电子排布式为ns1。下列叙述正确的是
| A.原子半径:W>R>Z>Y> X |
| B.电负性:Y>R>X>Z> W |
| C.常温下,Z、W单质都能与水发生置换反应 |
| D.R的最高价氧化物对应水化物一定有强氧化性 |
您最近一年使用:0次
2023-08-16更新
|
256次组卷
|
2卷引用:江西省部分学校(稳派)2023-2024学年高三上学期8月模拟预测化学试题



