1 . 利用铟(In)与锡(Sn)形成的金属间化合物InSn为基体,N(C2H5)3为催化剂,可将CO2与H2转化为HCOOH,反应的化学方程式为:CO2+H2 HCOOH。回答下列问题:
HCOOH。回答下列问题:
(1)In与Al为同族元素,其核外电子占据最高能层的符号为O,则In在元素周期表中的位置为___ 。基态In原子最高能级电子云轮廓图为____ 形。
(2)Sb为第ⅤA族从上到下的第四种元素,其价电子的轨道表示式为______ 。
(3)化学方程式中涉及的四种非金属元素电负性由小到大的顺序为_____ (用元素符号表示)。写出与CO2互为等电子体的一种阴离子____ (填离子符号)。
(4)催化剂N(C2H5)3分子中N原子的杂化方式为_____ ,其中碳原子成键电子对的空间构型为_____ 。
(5)HCOOH在水中溶解度远大于CO2的原因为____________ 。
(6)InSb晶体晶胞为立方晶胞(如图1),晶胞参数为631 pm,Sb位于顶点和面心,In位于Sb原子构成的四面体的体心。InSb晶体常用作金属锂的镶嵌材料,某种镶嵌锂之后的晶胞如图2,晶胞参数为664 pm(“ ”代表锂原子)。
”代表锂原子)。
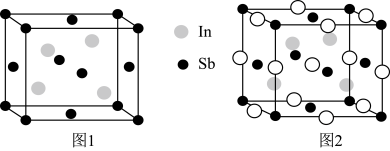
①图1所示晶胞中,距离最近的两个In原子间的距离为______ pm。(已知 ≈1.4)
≈1.4)
②图2所示晶胞的密度为______ g·cm−3。(列出计算式即可)
 HCOOH。回答下列问题:
HCOOH。回答下列问题: (1)In与Al为同族元素,其核外电子占据最高能层的符号为O,则In在元素周期表中的位置为
(2)Sb为第ⅤA族从上到下的第四种元素,其价电子的轨道表示式为
(3)化学方程式中涉及的四种非金属元素电负性由小到大的顺序为
(4)催化剂N(C2H5)3分子中N原子的杂化方式为
(5)HCOOH在水中溶解度远大于CO2的原因为
(6)InSb晶体晶胞为立方晶胞(如图1),晶胞参数为631 pm,Sb位于顶点和面心,In位于Sb原子构成的四面体的体心。InSb晶体常用作金属锂的镶嵌材料,某种镶嵌锂之后的晶胞如图2,晶胞参数为664 pm(“
 ”代表锂原子)。
”代表锂原子)。
①图1所示晶胞中,距离最近的两个In原子间的距离为
 ≈1.4)
≈1.4)②图2所示晶胞的密度为
您最近一年使用:0次
名校
解题方法
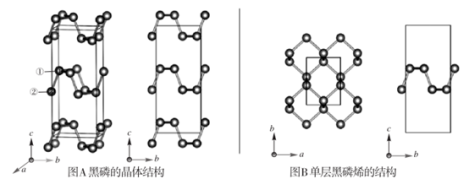
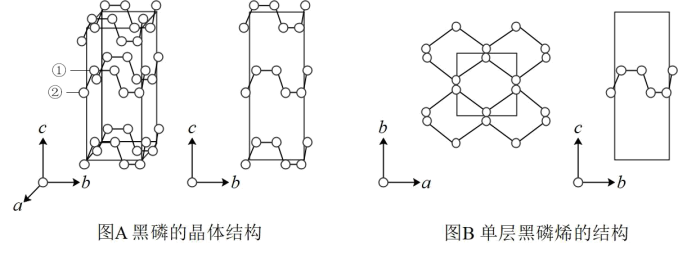
2 . 黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A,c=10.500A。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样,图A中编号为①的P原子的晶胞内坐标为(0.50,0.090,0.598)。请回答下列问题:
(1)写出P原子的价电子排布:___ 。
(2)P和F的电负性大小顺序是X(P)___ X(F)。(填“<”“=”或“>”)P和F形成的分子PF3和PF5,它们的几何构型分别为__ 、__ 。
(3)①黑磷中P原子杂化类型是__ 。黑磷中不存在__ (选填字母序号)。
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__ ,原因是__ 。
(4)图A中编号为②的P原子的晶胞内坐标为__ ,黑磷的晶胞中含有__ 个P原子。

(1)写出P原子的价电子排布:
(2)P和F的电负性大小顺序是X(P)
(3)①黑磷中P原子杂化类型是
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为
(4)图A中编号为②的P原子的晶胞内坐标为
您最近一年使用:0次
2020-07-13更新
|
233次组卷
|
2卷引用:江西省吉安、抚州、赣州市2020届高三一模理科综合化学试题
3 . 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____________ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是__________ ;金属离子与氧离子间的作用力为__________ ,Ca2+的配位数是__________ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中__________ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是__________ ;若晶胞参数为a nm,则晶体密度为_________ g·cm-3(列出计算式)。_______ 、_______ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是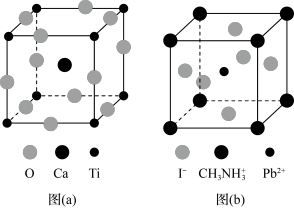
您最近一年使用:0次
2020-07-08更新
|
15371次组卷
|
21卷引用:2020年全国统一考试化学试题(新课标Ⅱ)
2020年全国统一考试化学试题(新课标Ⅱ)(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编2020年全国卷Ⅱ化学真题变式题江西省九江市2022届第二次高考模拟统一考试理综化学试题(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题北京一零一中学2021-2022学年高三上学期10月月考化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)专题18物质结构与性质(选修)-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)贵州省罗甸县边阳中学2022届高三模拟测试化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)专题20 结构与性质四川省成都锦江区嘉祥外国语高级中学2023-2024学年高三下学期第一次诊断性考试理科综合试题-高中化学河南省开封市铁路中学2020-2021学年高二下学期期中考试化学试题重庆市万州第二高级中学2021-2022学年高二下学期6月第三次质量检测化学试题
解题方法
4 . 黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A。,c=10.500A。。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位 P,所有P原子的成键环境一样,图 A中编 号为①的 P原子的晶胞内坐标为(0.500,0.090,0.598)。请回答下列问题:
(1)写出基态P原子的价电子排布图: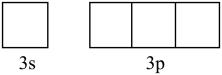
__________ 。
(2)P和 F的电负性大小顺序是 x(P)______ x(F)。(填 “<” “ =” 或 “ >” )P和 F形成的分子 PF3和PF5,它们的几何构型分别为__________ 、__________ 。
(3)①黑磷中 P原子杂化类型是__________ 。黑磷中不存在__________ (选填字母序号)。
A 共价键 B σ键 C π键 D 范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__________ ,原因是___________ 。
(4)图 A中编号为②的 P原子的晶胞内坐标为_______ ,黑磷的晶胞中含有________ 个 P原子。

(1)写出基态P原子的价电子排布图:

(2)P和 F的电负性大小顺序是 x(P)
(3)①黑磷中 P原子杂化类型是
A 共价键 B σ键 C π键 D 范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为
(4)图 A中编号为②的 P原子的晶胞内坐标为
您最近一年使用:0次
名校
解题方法
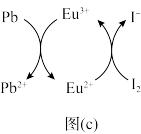
5 . 钯(Pd)、锌及其化合物在合成酮类物质中有极其重要的作用,如图为合成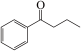 的反应过程:
的反应过程:
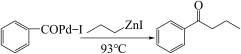
回答下列问题:
(1)I原子价电子排布式为___________ ,其能量最高的能层是___________ (填能层符号)。
(2)H、C、O三种元素的电负性由大到小的顺序为___________ 。
(3)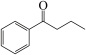 中碳原子的杂化方式为
中碳原子的杂化方式为___________ 。
(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是___________ 。
②NH3的空间构型为___________ 。
③1 mol [Zn(NH3)4]Cl2中含有___________ mol σ键。
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的___________ 。
(6)金属钯的堆积方式如图所示:
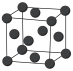
①该晶胞中原子的空间利用率为___________ (用含π的式子表示)。
②若该晶胞参数a=658 pm,则该晶胞密度为___________ (列出计算表达式)g·cm-3。
 的反应过程:
的反应过程:
回答下列问题:
(1)I原子价电子排布式为
(2)H、C、O三种元素的电负性由大到小的顺序为
(3)
 中碳原子的杂化方式为
中碳原子的杂化方式为(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O。
①上述反应涉及的物质中,固态时属于分子晶体的是
②NH3的空间构型为
③1 mol [Zn(NH3)4]Cl2中含有
(5)Zn和Cu可形成金属互化物(ZnCu),该金属互化物中所有金属原子均按面心立方最密堆积,若所有Cu均位于晶胞的面心,则Zn位于晶胞的
(6)金属钯的堆积方式如图所示:

①该晶胞中原子的空间利用率为
②若该晶胞参数a=658 pm,则该晶胞密度为
您最近一年使用:0次
2020-04-29更新
|
311次组卷
|
4卷引用:江西省南昌市八一中学2020届高三第三次模拟理科综合化学试题
江西省南昌市八一中学2020届高三第三次模拟理科综合化学试题2020年全国高考冲刺压轴卷(样卷) 理综(全国1卷)化学试题(已下线)第十一单元 物质的结构与性质测试题-2021年高考化学一轮复习名师精讲练安徽省六安市舒城中学2019-2020学年高二下学期期末考试化学试题
解题方法
6 . GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]____ 。
(2)根据元素周期律,元素的电负性Ga____ (填“大于”或“小于”,下同)As。
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为____ ,其中的阴离子的空间构型为____ 。
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是________ 。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为___ ;紧邻的As原子之间的距离为b,紧邻的As、Ca原子之间的距离为d,则b:d=____ ,该晶胞的密度为__ g ▪cm-3。(阿伏加 德罗常数用NA表示)

(1)基态Ga原子的核外电子排布式为[Ar]
(2)根据元素周期律,元素的电负性Ga
(3)科学家合成了一种阳离子为“N5n+”,其结构是对称的,5个N排成“V”形,每个N原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N5n+”化学式为“N8”的离子晶体,其电子式为
(4)组成相似的CaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价键数为

您最近一年使用:0次
名校
解题方法
7 . (NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为______ 。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是____ 。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_____ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(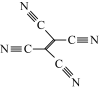 )。
)。
①CH3CN中碳原子的杂化方式是____ 和_____ 。
②TCNE中第一电离能较大的是___ (填元素符号),分子中所有原子____ (填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是 ___ 。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为___ (列出计算式)g·cm-3。
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(
 )。
)。①CH3CN中碳原子的杂化方式是
②TCNE中第一电离能较大的是
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:

Fe3C的密度为
您最近一年使用:0次
2020-04-06更新
|
618次组卷
|
4卷引用:江西省九江市十校2020届高三下学期模拟考试理综化学试题
江西省九江市十校2020届高三下学期模拟考试理综化学试题河南等省五岳2020届高三4月联考(全国I卷)理综化学试题河南省临颍县南街高级中学2020届高三下学期第一次月考理综化学试题(已下线)01 物质结构与性质综合题型集训(1) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
解题方法
8 . 2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。LiFePO4、聚乙二醇、LiPF6、LiAsF6和LiCl等可作锂离子聚合物电池的材料。回答下列问题:
(1)Fe的价层电子排布式为___ 。
(2)Li、F、P、As四种元素的电负性由大到小的顺序为___ 。
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是___ 。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。
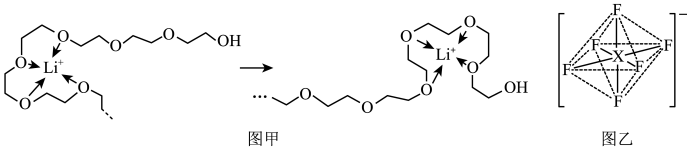
①聚乙二醇分子中,碳、氧的杂化类型分别是___ 、___ 。
②从化学键角度看,Li+迁移过程发生___ (填“物理变化”或“化学变化”)。
③PF6中P的配位数为___ 。
④相同条件,Li+在___ (填“LiPF6”或“LiAsF6”)中迁移较快,原因是___ 。
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为___ 。LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加 德罗常数的值,则LiCl·3H2O晶体的密度为___ g·cm-3(列出计算表达式)。
(1)Fe的价层电子排布式为
(2)Li、F、P、As四种元素的电负性由大到小的顺序为
(3)乙二醇(HOCH2CH2OH)的相对分子质量与丙醇(CH3CH2CH2OH)相近,但沸点高出100℃,原因是
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①聚乙二醇分子中,碳、氧的杂化类型分别是
②从化学键角度看,Li+迁移过程发生
③PF6中P的配位数为
④相同条件,Li+在
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子分数坐标。据此推断该晶胞中Cl原子的数目为

您最近一年使用:0次
2020-03-13更新
|
293次组卷
|
2卷引用:江西省上饶市2020届高三5月第三次模拟考试理综化学试题
名校
解题方法
9 . 据媒体报道,法国一家公司Tiamat日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池,预计从2020年开始实现工业生产。该电池的负极材料为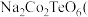 制备原料为
制备原料为 、
、 和
和 ,电解液为
,电解液为 的碳酸丙烯酯溶液。
的碳酸丙烯酯溶液。
回答下列问题:
(1)Te属于元素周期表中______ 区元素,其基态原子的价电子排布式为______ 。
(2)基态Na原子中,核外电子占据的原子轨道总数为______ 。
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为______  用元素符号表示
用元素符号表示 。
。
(4)碳酸丙烯酯的结构简式如下图所示,则其中碳原子的杂化轨道类型为______ ,1mol碳酸丙烯酯中σ键的数目为______ 。
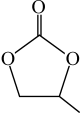
 的几何构型为正八面体形,配体是
的几何构型为正八面体形,配体是______ ,该配离子包含的作用力为______  填选项字母
填选项字母 。
。
A.离子键 B. 极性键 C. 配位键 D.氢键 E. 金属键
(6)Na和O形成的离子化合物的晶胞结构如下图所示,该晶胞的密度为ρg/ ,阿伏加 德罗常数的值为
,阿伏加 德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为_______________________ 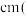 用含ρ、
用含ρ、 的代数式表示
的代数式表示 。
。
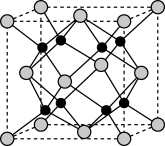
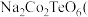 制备原料为
制备原料为 、
、 和
和 ,电解液为
,电解液为 的碳酸丙烯酯溶液。
的碳酸丙烯酯溶液。回答下列问题:
(1)Te属于元素周期表中
(2)基态Na原子中,核外电子占据的原子轨道总数为
(3)结合题中信息判断:C、O、Cl的电负性由大到小的顺序为
 用元素符号表示
用元素符号表示 。
。(4)碳酸丙烯酯的结构简式如下图所示,则其中碳原子的杂化轨道类型为

 的几何构型为正八面体形,配体是
的几何构型为正八面体形,配体是 填选项字母
填选项字母 。
。A.离子键 B. 极性键 C. 配位键 D.氢键 E. 金属键
(6)Na和O形成的离子化合物的晶胞结构如下图所示,该晶胞的密度为ρg/
 ,阿伏加 德罗常数的值为
,阿伏加 德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为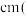 用含ρ、
用含ρ、 的代数式表示
的代数式表示 。
。
您最近一年使用:0次
2011·江西·一模
名校
解题方法
10 . 已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为:___________________________________ ,Y元素原子最外层电子的电子排布图为:____________ 。
(2)若X、Y两元素电负性分别为2.1和2.85,试判断XY4中X与Y之间的化学键为________ (填“共价键”或“离子键”)。
(3)该化合物的空间结构为______________ 形,中心原子的轨道杂化类型为__________ ,分子为______________ (填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该液体微粒间的作用力是____________ 。
(5)该化合物的沸点与SiCl4比较:________ (填化学式)的高,原因是__________________________ 。
(1)X元素的原子基态时电子排布式为:
(2)若X、Y两元素电负性分别为2.1和2.85,试判断XY4中X与Y之间的化学键为
(3)该化合物的空间结构为
(4)该化合物在常温下为液体,该液体微粒间的作用力是
(5)该化合物的沸点与SiCl4比较:
您最近一年使用:0次
2019-04-27更新
|
398次组卷
|
15卷引用:2011届江西省八所重点中学联合考试高三(理综)化学部分
(已下线)2011届江西省八所重点中学联合考试高三(理综)化学部分(已下线)2012-2013学年山东省淄博市沂源一中高二下学期期中模块检测化学卷河北省秦皇岛市卢龙县2016-2017学年高二下学期期末考试化学试题人教版2017-2018学年高二化学选修三同步训练:2.3 分子的性质(第2课时)贵州省息烽县一中2018-2019学年高二11月份考试化学试题云南省巧家县四中2018-2019学年高二上学期12月份考试化学试题贵州省从江县第一民族中学2018-2019学年高二上学期期末考试化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题云南省玉溪市江川二中2018-2019学年高二下学期5月份考试化学试题云南省昭通市永善县第二中学2019—2020学年高二上学期期末考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题(已下线)第二章 分子结构与性质【过关测试提高卷】-2020-2021学年高二化学单元复习(新教材人教版选择性必修2) 新疆生产建设兵团第二师八一中学2022-2023学年高二下学期期中考试化学试题云南省大理州实验中学2021-2022学年高二下学期化学期中考试题



