10. 1799年,英国化学家汉弗莱·戴维发现了N
2O气体。在食品行业中,N
2O可用作发泡 剂和密封剂。
(l) N
2是硝酸生产中氨催化氧化的副产物,NH
3与O
2在加热和催化剂的作用下生成N
2O的化学方程式为
________。
(2)N
2O在金粉表面发生热分解反应:2N
2O(g) =2N
2(g)+O
2(g) △H。
已知:2NH
3(g)+3N
2O(g)=4N
2(g)+3H
2O(l) △H
1=-1010KJ/mol
4NH3(g)+3O2(g) =2N2(g)+6H2O(l) △H2=-1531KJ/mol
△H=
__________。
(3)N
2O和CO是环境污染性气体,研究表明,CO与N
2O在Fe
+作用下发生反应:N
2O(g)+CO(g)

CO
2(g)十N
2(g)的能量变化及反应历程如下图所示,两步反应分别为:反应①Fe
++N
2O

FeO+N
2;反应②
______________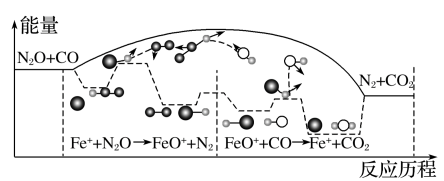
由图可知两步反应均为
____(填“放热”或“吸热”)反应,由
______(填“反应①或反应②”)决定反应达到平衡所用时间。
(4)在固定体积的密闭容器中,发生反应:N
2O(g)+CO(g)

CO
2(g)+N
2(g),改变原料气配比进行多组实验(各次实验的温度可能相同,也可能不同),测定N
2O的平衡转化率。部分实验结果如图所示:
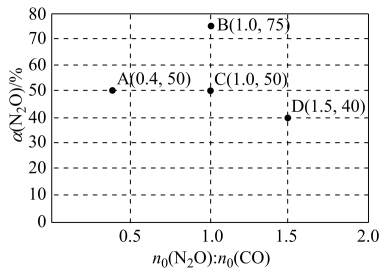
①如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是:
____ ;
②图中C、D两点对应的实验温度分别为T
C和T
D,,通过计算判断T
C____T
D(填“>”“=”或“<”)。
(5)在某温度下,向1L密闭容器中充入CO与N
2O,发生反应:N
2O(g)+CO(g)

CO
2(g)十N
2(g),随着反应的进行,容器内CO的物质的量分数变化如下表所示:
| 时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 物质的量分数 | 50.0% | 40.25% | 32.0% | 26.2% | 24.0% | 24.0% |
则该温度下反应的平衡常数K=
____。