名校
解题方法
1 . 目前我国研制的稀土催化剂催化转化汽车尾气示意图如图:

(1)Zr原子序数为40,价电子排布式为___ 。图1中属于非极性的气体分子是___ 。
(2)①氟化硼(BF3)是石油化工的重要催化剂。BF3中B-F比BF 中B—F的键长短,原因是
中B—F的键长短,原因是___ 。
②乙硼烷(B2H6)是用作火箭和导弹的高能燃料,氨硼烷(H3NBH3)是最具潜力的储氢材料之一。

B2H6的分子结构如图2所示,其中B原子的杂化方式为___ 。
③H3NBH3的相对分子质量与B2H6相差不大,但是H3NBH3的沸点却比B2H6高得多,原因是__ 。
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,该晶体中含有的化学键有__ 。
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,[Ni(CO)4]的配体中配位原子是___ 。
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图4所示,则与每个Sr2+紧邻的O2-有___ 个。
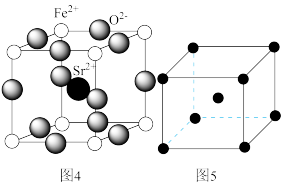
(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径为apm,相对原子质量为b,阿伏加 德罗常数为NA,试计算晶体铌的密度为___ g·cm-3(用来a、b、NA表示计算结果)。

(1)Zr原子序数为40,价电子排布式为
(2)①氟化硼(BF3)是石油化工的重要催化剂。BF3中B-F比BF
 中B—F的键长短,原因是
中B—F的键长短,原因是②乙硼烷(B2H6)是用作火箭和导弹的高能燃料,氨硼烷(H3NBH3)是最具潜力的储氢材料之一。

B2H6的分子结构如图2所示,其中B原子的杂化方式为
③H3NBH3的相对分子质量与B2H6相差不大,但是H3NBH3的沸点却比B2H6高得多,原因是
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,该晶体中含有的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,[Ni(CO)4]的配体中配位原子是
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图4所示,则与每个Sr2+紧邻的O2-有

(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径为apm,相对原子质量为b,阿伏加 德罗常数为NA,试计算晶体铌的密度为
您最近一年使用:0次
2020-07-02更新
|
290次组卷
|
2卷引用:山东师范大学附属中学2020届普通高等学校招生全国统一考试化学试题(模拟一)
2 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___ 。
(2)锗(Ge)、砷(As)、硒的第一电离能大小排序为___ (填元素符号)。H2SeO4的酸性比H2SeO3的强,其原因是___ 。
(3)H2SeO3的中心原子杂化类型是___ ,SeO32-的立体构型是___ 。与SeO42-互为等电子体的分子有___ (写一种物质的化学式即可)。
(4)H2Se属于___ (填“极性”或“非极性”)分子;单质硒的熔点为217℃,它属于___ 晶体。
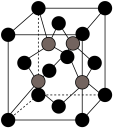
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___ ;若该晶胞的密度为ρg⋅cm-3,硒化锌的摩尔质量为Mg·mol-1。NA代表阿伏加 德罗常数的值,则晶胞参数a为___ pm。
(1)基态硒原子的价层电子排布式为
(2)锗(Ge)、砷(As)、硒的第一电离能大小排序为
(3)H2SeO3的中心原子杂化类型是
(4)H2Se属于
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

您最近一年使用:0次
名校
3 . 金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____ 。
②与BH4-互为等电子体的阳离子的化学式为_____ 。
③H、B、Ti原子的第一电离能由小到大的顺序为_____ 。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
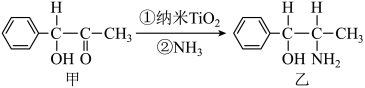
化合物乙的分子中采取sp3杂化方式的原子个数为_____ 。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____ 。
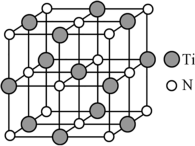
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为
②与BH4-互为等电子体的阳离子的化学式为
③H、B、Ti原子的第一电离能由小到大的顺序为
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。

化合物乙的分子中采取sp3杂化方式的原子个数为
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是

您最近一年使用:0次
2019-06-01更新
|
521次组卷
|
4卷引用:云南省楚雄姚安一中2020届高三3月线上模拟理综化学试题
解题方法
4 . 由ⅢA、VA族元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造。与BCl3互为等电子体,且由第二周期元素组成的一种阴离子为__________ (填离子符号)。
(2)氨硼烷(H3N—BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料。
①H3N—BH3中N原子的轨道杂化类型为________________ 。
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数为____________ ;BH 的立体构型是
的立体构型是_______ ;该制备反应的化学方程式为______________ 。
(3)氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
下列有关叙述错误的是_____________
(4)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为_____________ 。Ga的配位原子(As)数目为________ ;Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGacm和rAscm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为__________ 。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造。与BCl3互为等电子体,且由第二周期元素组成的一种阴离子为
(2)氨硼烷(H3N—BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料。
①H3N—BH3中N原子的轨道杂化类型为
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数为
 的立体构型是
的立体构型是(3)氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
下列有关叙述错误的是_____________
| A.氨硼烷中存在配位键 |
| B.第一电离能大小关系:N>O>C>B>H |
| C.反应前后碳原子的杂化类型不变 |
| D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形 |

您最近一年使用:0次



