10. 在化工生产、污水处理中广泛涉及硫单质及其化合物。
Ⅰ.煤制得的化工原料中含有羰基硫(O===C===S),该物质可转化为H
2S,主要反应如下:①水解反应:COS(g)+H
2O(g)

H
2S(g)+CO
2(g) Δ
H1=-94 kJ·mol
-1,②氢解反应:COS(g)+H
2(g)

H
2S(g)+CO(g) Δ
H2=-54 kJ·mol
-1。
(1)请计算CO(g)和H
2O(g)生成H
2(g)和CO
2(g)的反应热Δ
H=
______。
(2)在定温定容的密闭容器中进行反应①,下列事实说明反应①达到平衡状态的是
_____(填字母)。
A.容器的压强不再改变
B.混合气体的密度不再改变
C.化学平衡常数不再改变
D.生成1 mol H—O键,同时生成1 mol H—S键
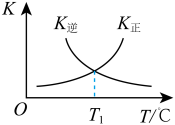
(3)反应②的正、逆反应的平衡常数(K)与温度(T)的关系如图所示。在T
1℃时,向容积为5 L的密闭容器中加入2 mol COS(g)和1 mol H
2(g),充分反应,COS的平衡转化率为
______。
Ⅱ.在容积为2 L的恒容密闭容器中,充入0.5 mol H
2S(g),发生反应:2H
2S(g)

2H
2(g)+S
2(g),在不同温度和压强下进行实验,结果如图所示。
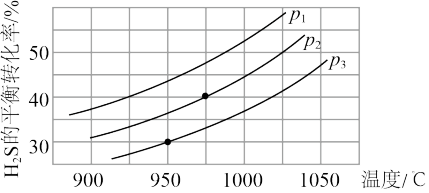
(4)图中压强p
1、p
2、p
3由大到小的顺序是
______。
(5)在950 ℃,压强为p
3时,反应经30 min达到平衡,则平均反应速率v(H
2)=
_______。
(6)在p
2=6 MPa,温度为975 ℃时,请计算该反应的平衡常数
Kc为
_____(保留2位有效数字)。对于气相反应,用某组分(B)的平衡分压(p
B)代替物质的量浓度(c
B)也可以表示平衡常数(记作
Kp),p
B=p
总×B的物质的量分数,则此条件下该反应的平衡常数
Kp=
___MPa。