名校
解题方法
1 . 铬是人体内微量元素之一,是重要的血糖调节剂。
(1)铬在元素周期表中的位置为___________ ,其基态原子核外电子占据的原子轨道数为___________ 。
(2)已知 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。
①该配合物中提供孤电子对形成配位键的原子是___________ 。
②配体中中心原子的杂化方式为___________ (填字母)。
a. b.
b. c.sp d.
c.sp d.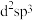
③该物质中, 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是___________ 。
(3)钛铬合金是一种高温结构材料,第二电离能
___________ (填“ ”或“
”或“ ”)
”)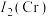 ,原因是
,原因是___________ 。
(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为 ,则B点分数坐标为
,则B点分数坐标为___________ ,已知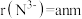 ,
,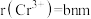 ,则AB间距离为
,则AB间距离为___________ nm。
(1)铬在元素周期表中的位置为
(2)已知
 半径小,正电场较强,容易与
半径小,正电场较强,容易与 、
、 、
、 等分子或离子形成多种配合物,
等分子或离子形成多种配合物, 是其中的一种。
是其中的一种。①该配合物中提供孤电子对形成配位键的原子是
②配体中中心原子的杂化方式为
a.
 b.
b. c.sp d.
c.sp d.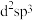
③该物质中,
 的键角比独立存在的气态氨气分子中键角略大,其原因是
的键角比独立存在的气态氨气分子中键角略大,其原因是(3)钛铬合金是一种高温结构材料,第二电离能

 ”或“
”或“ ”)
”)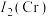 ,原因是
,原因是(4)铬的一种氮化物晶体立方晶胞结构如图所示,A点分数坐标为
 ,则B点分数坐标为
,则B点分数坐标为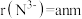 ,
,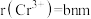 ,则AB间距离为
,则AB间距离为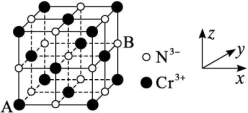
您最近一年使用:0次
名校
2 . 下列说法中正确的有
①由原子构成的晶体不一定是共价晶体
②水结成冰密度减小与水分子之间能形成氢键有关
③HF、HCl、HBr、HI的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤ 、
、 、
、 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高
⑥硬度由大到小:金刚石>碳化硅>晶体硅
①由原子构成的晶体不一定是共价晶体
②水结成冰密度减小与水分子之间能形成氢键有关
③HF、HCl、HBr、HI的热稳定性和还原性依次减弱
④共价键的强弱决定分子晶体熔、沸点的高低
⑤
 、
、 、
、 的热稳定性依次减弱,熔沸点依次升高
的热稳定性依次减弱,熔沸点依次升高⑥硬度由大到小:金刚石>碳化硅>晶体硅
| A.②③④⑥ | B.①②③⑥ | C.①②④⑤ | D.①②⑤⑥ |
您最近一年使用:0次
2024-04-25更新
|
271次组卷
|
4卷引用:宁夏石嘴山市第三中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
3 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:______________ 。
(3)ED3分子的VSEPR模型名称为____________ ,空间构型为____________ 。
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为_____________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是___________ (填序号)。
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
元素 | 相关信息 |
A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 原子核外p电子数与s电子数相等 |
C | 基态原子的价电子排布为nsn-1npn+1 |
D | 能层数与C相同,且电负性比C大 |
E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)A2B2难溶于CS2,简要说明理由:
(3)ED3分子的VSEPR模型名称为
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
您最近一年使用:0次
名校
解题方法
4 . 下列关于物质的结构或性质的比较中,错误的是
A. 的键角比 的键角比 大 大 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
C. 、MgO、 、MgO、 三者的晶体类型和化学键类型完全相同 三者的晶体类型和化学键类型完全相同 |
| D.金属晶体具有良好的延展性,是因为金属键具有方向性 |
您最近一年使用:0次
名校
解题方法
5 . 下列与分子性质有关的说法正确的是
A. 中,配位原子是N,配位数为12 中,配位原子是N,配位数为12 |
| B.用乙酸乙酯而不用水溶解油漆,是因为乙酸乙酯与油漆中的成分极性都较小,利用了相似相溶原理,而水分子极性较大,对油漆溶解效果不好 |
C. 键的键能大于 键的键能大于 键的键能,所以 键的键能,所以 的熔沸点高于 的熔沸点高于 |
D. 的沸点高于 的沸点高于 ,是因为 ,是因为 分子间的范德华力大于 分子间的范德华力大于 分子间的范德华力 分子间的范德华力 |
您最近一年使用:0次
名校
解题方法
6 . 下列叙述正确的是
A.N的电负性比P的大,可推断 分子的极性比 分子的极性比 大 大 |
B. 分子中存在 分子中存在 键,则 键,则 中也存在 中也存在 键 键 |
C. 键能大, 键能大, 性质稳定:则 性质稳定:则 键能大, 键能大, 性质也稳定 性质也稳定 |
D. 和 和 都为正四面体形, 都为正四面体形, 、 、 中键角均为109°28′ 中键角均为109°28′ |
您最近一年使用:0次
名校
解题方法
7 . 下列对有关事实的解释正确的是
| 事实 | 解释 | |
 | 某些金属盐灼烧呈现不同焰色 | 电子从低能轨道跃迁至高能轨道时吸收光波长不同 |
 | CH4与NH3分子的空间构型不同 | 二者中心原子杂化轨道类型不同 |
 | HF的热稳定性比HCl强 | H-F比H-Cl的键能大 |
 | NH3的沸点比PH3高 | NH3分子间作用力大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列事实与元素的电负性无关的是
A. 分子中 分子中 元素显-1价, 元素显-1价, 元素显+1价 元素显+1价 | B. 分子中的键角小于 分子中的键角小于 分子中的键角 分子中的键角 |
C. 是极性分子,可溶于水 是极性分子,可溶于水 | D. 易形成分子间氢键 易形成分子间氢键 |
您最近一年使用:0次
名校
9 . 下列说法不正确 的是
| A.碳碳双键、碳碳三键的键能分别是碳碳单键键能的两倍和三倍 |
B.丙烯 分子中有8个 分子中有8个 键,1个 键,1个 键 键 |
C.丙烯分子中的 键不如 键不如 键稳定 键稳定 |
D.氮气分子中的 键不如 键不如 键稳定 键稳定 |
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)第四周期未成对电子数最多的元素是___________ (填元素符号),该元素基态原子核外电子共有___________ 种不同能量的电子。
(2)丁二酮(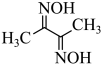 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ,该物质中,σ键与π键数目之比为___________ 。
(3)比较键角大小:AsO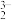
___________ AsO (填>、<或=)。
(填>、<或=)。
(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
(1)第四周期未成对电子数最多的元素是
(2)丁二酮(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为(3)比较键角大小:AsO
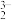
 (填>、<或=)。
(填>、<或=)。(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
| A.[Ar]3d104p1 | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
您最近一年使用:0次



