解题方法
1 . N、P、 为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
(1)基态砷原子核外有___________ 个未成对电子,位于元素周期表的___________ 区。
(2)已知: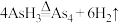 ,
, 的空间结构为
的空间结构为___________ , 原子的杂化类型为
原子的杂化类型为___________ ;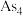 为正四面体结构,则1
为正四面体结构,则1
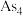 中含
中含___________ 
 键。
键。
(3)《本草纲目》中记载砒霜( )可入药,已知:
)可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有___________ ;
(4) 的键角为93.5°,
的键角为93.5°, 的键角为92.1°,
的键角为92.1°, 的键角大于
的键角大于 的键角的原因是
的键角的原因是______ ;
(5)由砷,铁,钙组成的某种新材料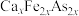 ,的晶胞结构如图所示。已知:
,的晶胞结构如图所示。已知: ,底边边长为a
,底边边长为a ,高为b
,高为b ,1号原子的高为
,1号原子的高为 。
。
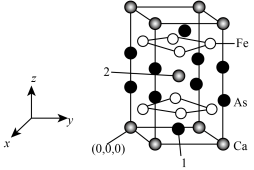
①1号原子的坐标为___________ ,距离2号原子最近的 原子有
原子有___________ 个。
②该晶体密度为___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:
为第VA族元素,该族元素及其化合物在生产,生活中有广泛应用。回答下列问题:(1)基态砷原子核外有
(2)已知:
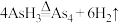 ,
, 的空间结构为
的空间结构为 原子的杂化类型为
原子的杂化类型为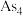 为正四面体结构,则1
为正四面体结构,则1
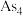 中含
中含
 键。
键。(3)《本草纲目》中记载砒霜(
 )可入药,已知:
)可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力有(4)
 的键角为93.5°,
的键角为93.5°, 的键角为92.1°,
的键角为92.1°, 的键角大于
的键角大于 的键角的原因是
的键角的原因是(5)由砷,铁,钙组成的某种新材料
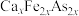 ,的晶胞结构如图所示。已知:
,的晶胞结构如图所示。已知: ,底边边长为a
,底边边长为a ,高为b
,高为b ,1号原子的高为
,1号原子的高为 。
。
①1号原子的坐标为
 原子有
原子有②该晶体密度为
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-12-16更新
|
355次组卷
|
2卷引用:海南省2023-2024学年高三上学期高考全真模拟卷(四)化学试题
解题方法
2 . 材料是人类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题:
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
(2)已知:第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色。下列离子形成的水合离子为无色的是_______。
(3)K3[Fe(CN)6]中所含元素电负性由大到小的顺序为_______ ,lmol K3[Fe(CN)6]含有_______ molσ键;Ti3+能形成化合物[TiCl(H2O)5]Cl2·H2O,该化合物中Ti3+的配位数为_______ 。
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:_______ 。
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在 、
、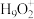 等微粒。
等微粒。
①H2O分子的键角小于H3O+离子的键角,原因是_______ 。
②画出 可能的一种结构式
可能的一种结构式_______ 。
(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。
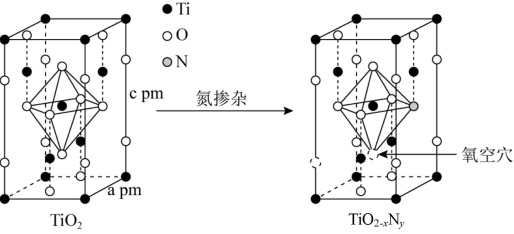
①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为_______ g/cm3。
②图乙的结构可用化学式TiO2-xNy表示,其中x=_______ 。
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
A.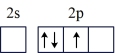 | B.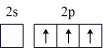 |
C.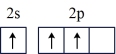 | D.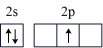 |
| A.Sc3+ | B.Cr3+ | C.Fe3+ | D.Zn2+ |
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在
 、
、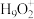 等微粒。
等微粒。①H2O分子的键角小于H3O+离子的键角,原因是
②画出
 可能的一种结构式
可能的一种结构式(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为
②图乙的结构可用化学式TiO2-xNy表示,其中x=
您最近一年使用:0次



