名校
解题方法
1 . 按要求回答下列问题:
(1)基态钛原子核外共有________ 种空间运动状态不相同的电子。Cu在周期表中的位置为________________________ ,基态Ni2+的价层电子排布式为________________________ ,Zn位于元素周期表的________________ 区。
(2)分子极性:CH4________ NH3(填“>”或“<”),熔沸点:CH4________ NH3(填“>”或“<”),键角:CH4________ NH3(填“>”或“<”)。
(3)组成为 ,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明,
,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明, 恰好与
恰好与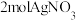 反应生成沉淀。则X的化学式为
反应生成沉淀。则X的化学式为________ 。(表示出内界和外界)
(1)基态钛原子核外共有
(2)分子极性:CH4
(3)组成为
 ,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明,
,配位数为6的晶体有两种。其中一种物质X呈绿色。实验表明, 恰好与
恰好与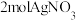 反应生成沉淀。则X的化学式为
反应生成沉淀。则X的化学式为
您最近一年使用:0次
2 . 硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷( )是最简单的硼烷,可以在
)是最简单的硼烷,可以在_______ (填“乙酸”或“乙醚”或“水”)介质中使用 还原
还原 获得,
获得, 的电子式为
的电子式为_______ ,制备乙硼烷的化学方程式为_______ 。 )的溶解度
)的溶解度
(2)操作1是蒸发浓缩、冷却结晶、过滤、_______ ,干燥;整个流程中可循环利用的物质是_______ 。
(3)硼酸( )是一元弱酸,在溶液中存在平衡:
)是一元弱酸,在溶液中存在平衡: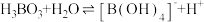 (常温下:
(常温下: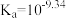 ),
), 与NaOH溶液反应可制备硼砂。常温下,在
与NaOH溶液反应可制备硼砂。常温下,在 硼砂溶液中,
硼砂溶液中,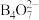 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该溶液pH=
,该溶液pH=_______ 。常温常压下,硼酸( )晶体结构为层状,其二维平面结构如图所示:
)晶体结构为层状,其二维平面结构如图所示:_______ 。
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化合物,其原因为_______ 。
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(
 )是最简单的硼烷,可以在
)是最简单的硼烷,可以在 还原
还原 获得,
获得, 的电子式为
的电子式为
 )的溶解度
)的溶解度| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 80 |
| 溶解度/g | 2.77 | 3.65 | 4.87 | 6.77 | 8.90 | 23.54 |
(2)操作1是蒸发浓缩、冷却结晶、过滤、
(3)硼酸(
 )是一元弱酸,在溶液中存在平衡:
)是一元弱酸,在溶液中存在平衡: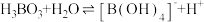 (常温下:
(常温下: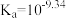 ),
), 与NaOH溶液反应可制备硼砂。常温下,在
与NaOH溶液反应可制备硼砂。常温下,在 硼砂溶液中,
硼砂溶液中,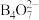 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该溶液pH=
,该溶液pH= )晶体结构为层状,其二维平面结构如图所示:
)晶体结构为层状,其二维平面结构如图所示: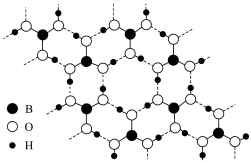
H3BO3的层状结构
从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
| 化学键 |  |  |  |
键能( ) ) | 389 | 561 | 293 |
您最近一年使用:0次
解题方法
3 . 磷的单质及其化合物在生产、生活中具有广泛应用。回答下列问题:
(1)基态磷原子价电子排布式为___________ ,核外电子占据的最高能级的电子云轮廓图为___________ 形。
(2)第三周期元素中第一电离能介于硅和磷之间的元素为___________ (填元素符号),离子半径:
___________ (填“>”“<”或“=”) 。
。
(3) 固体属于
固体属于___________ 晶体,键能: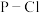
___________ (填“>”“<”或“=”) ,
, 、
、 中键角较大的是
中键角较大的是___________ 。
(4)白磷的分子结构及其晶胞结构如图所示,晶胞参数为 。
。 中磷原子的杂化方式为
中磷原子的杂化方式为___________ 。
②白磷晶体中,距离一个 最近的
最近的 个数为
个数为___________ 。
③该晶体的密度=___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态磷原子价电子排布式为
(2)第三周期元素中第一电离能介于硅和磷之间的元素为

 。
。(3)
 固体属于
固体属于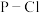
 ,
, 、
、 中键角较大的是
中键角较大的是(4)白磷的分子结构及其晶胞结构如图所示,晶胞参数为
 。
。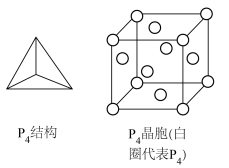
 中磷原子的杂化方式为
中磷原子的杂化方式为②白磷晶体中,距离一个
 最近的
最近的 个数为
个数为③该晶体的密度=
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
4 . M、N、R、X、Y五种元素在元素周期表中的位置如下图所示。元素M和R的原子序数之和等于N的原子序数,元素R和X的原子序数之和等于Y的原子序数。
(1)N的元素名称为_______ 。
(2)在同周期元素中,比元素M的第一电离能小的元素有______ 种。
(3)元素M与元素X、Y形可成化合物MX3、MY3,MY3分子中元素Y的化合价为+1价。
①化合物MX3分子构型为_______ 。
②比较MX3、MY3键角大小∠XMX_____ ∠YMY(填“>”、“<”或“=”)
(4)基团的诱导效应对有机酸的酸性有较大的影响。有机酸的酸性强弱可用电离常数的负对数pKa的大小来衡量,则pKa(CH2XCOOH)____ pKa(CH3COOH)(填“>”、“<”或“=”)
(5)元素X的简单氢化物HX极易溶于水,其重要原因是HX分子可以跟水分子形成氢键,那么在HX的水溶液中可能存在的氢键类型有_____ 种。
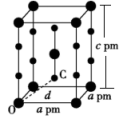
(6)化合物XeX2的晶体属四方晶系,晶胞参数如图所示(晶胞棱边夹角均为90°)。已知Xe-X键长为rpm,晶胞中O、C间距离d=___ pm。
| M | R | X |
| N | Y |
(2)在同周期元素中,比元素M的第一电离能小的元素有
(3)元素M与元素X、Y形可成化合物MX3、MY3,MY3分子中元素Y的化合价为+1价。
①化合物MX3分子构型为
②比较MX3、MY3键角大小∠XMX
(4)基团的诱导效应对有机酸的酸性有较大的影响。有机酸的酸性强弱可用电离常数的负对数pKa的大小来衡量,则pKa(CH2XCOOH)
(5)元素X的简单氢化物HX极易溶于水,其重要原因是HX分子可以跟水分子形成氢键,那么在HX的水溶液中可能存在的氢键类型有
(6)化合物XeX2的晶体属四方晶系,晶胞参数如图所示(晶胞棱边夹角均为90°)。已知Xe-X键长为rpm,晶胞中O、C间距离d=

您最近一年使用:0次
名校
5 . 2020年11月24日4时30分,长征五号遥五运载火箭在中国文昌航天发射场点火升空,将嫦娥五号月球探测器运送至地月转移轨道,开启我国首次地外天体采样返回之旅。月球的沙土中含有丰富的钛铁矿,土壤中还含有硅、铝、钾、钡、钴、铷、汞、铜和稀土元素等。
(1)钛在元素周期表中的位置是___________ ,与Ti处于同周期、未成对电子数与Ti相同的元素还有___________ 种。
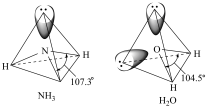
(2)[Cu(NH3)4]SO4·H2O是一种蓝色晶体,其中的NH3、H2O的空间结构和相应的键角如图所示,H2O的键角比NH3小的原因是___________ 。
(3)基态铁原子的价层电子排布图为___________ 。相同条件下,Fe3+和Fe2+相比,___________ 更稳定,原因是___________ 。
(4)某钙钛矿的晶体结构属于立方结构,具有高度的对称性,其晶胞结构如图所示。
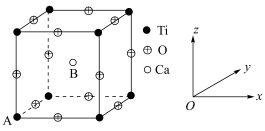
①在该晶体中每个钛离子周围与它最近且距离相等的钛离子有___________ 个。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。晶胞中A的原子分数坐标为(0,0,0),则B(Ca)的原子分数坐标为___________ 。
(1)钛在元素周期表中的位置是
(2)[Cu(NH3)4]SO4·H2O是一种蓝色晶体,其中的NH3、H2O的空间结构和相应的键角如图所示,H2O的键角比NH3小的原因是

(3)基态铁原子的价层电子排布图为
(4)某钙钛矿的晶体结构属于立方结构,具有高度的对称性,其晶胞结构如图所示。

①在该晶体中每个钛离子周围与它最近且距离相等的钛离子有
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。晶胞中A的原子分数坐标为(0,0,0),则B(Ca)的原子分数坐标为
您最近一年使用:0次
名校
解题方法
6 . 碳族元素中的碳、硅、锗及其化合物在诸多领域具有重要用途。回答下列问题:
(1)锗元素位于周期表___________ 区,基态硅原子核外电子排布式为___________ ,基态碳原子核外有___________ 种不同运动状态的电子。
(2)草酸(分子式:H2C2O4,结构简式:HOOC-COOH)与NiSO4溶液反应,可制备NiC2O4∙2H2O。
①组成H2C2O4的元素中第一电离能最大的为___________ (填元素符号),该分子中σ键与π键的个数比为___________ 。
② 中的键角为
中的键角为___________ ,该离子的空间构型为___________ 。
(3)金刚石的结构及某碳硅化合物的晶胞结构如图所示,晶胞参数为anm。___________ (NA为阿伏加德罗常数的值,下同)。
②该碳硅化合物的化学式为___________ ,其晶体的密度为___________ g∙cm-3。
(1)锗元素位于周期表
(2)草酸(分子式:H2C2O4,结构简式:HOOC-COOH)与NiSO4溶液反应,可制备NiC2O4∙2H2O。
①组成H2C2O4的元素中第一电离能最大的为
②
 中的键角为
中的键角为(3)金刚石的结构及某碳硅化合物的晶胞结构如图所示,晶胞参数为anm。

②该碳硅化合物的化学式为
您最近一年使用:0次
2023-12-26更新
|
157次组卷
|
3卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二下学期开学化学试题
名校
7 . 根据所学化学知识填空。
Ⅰ.铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,FeSO4·H2O结构如图所示:

(1)从结构的角度看,Fe2+不如Fe3+稳定,原因是_____ 。
(2)SO 和H2O分子比较,
和H2O分子比较,_____ 的键角更大。
(3)S原子核外有_____ 种能量不同的电子。
Ⅱ.物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。根据所学知识,回答问题:
(4)一定温度下,向1L0.1mol/LCH3COOH溶液中加入少量CH3COONa固体,则溶液中 的值
的值_____ (填“增大”、“减小”或“不变”)。
(5)25℃下,有浓度均为0.1mol/L的三种溶液:a.Na2CO3;b.NaClO;c.CH3COONa(已知25℃时电离常数:H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8;CH3COOH:Ka=1.8×10-5)往等浓度的Na2CO3、NaClO的混合溶液中加入少量醋酸,请写出发生反应的离子方程式_____ 。
(6)已知25℃时,Ksp(AgCl)=1.8×10-10,现将足量氯化银固体分别放入:a.100mL蒸馏水中b.100mL0.2mol/LAgNO3溶液中;c.100mL0.1mol/L氯化铝溶液中;d.100mL0.1mol/L盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是_____ (填序号)。
(7)含Cr2O 的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O 。为了使废水的排放达标,进行如图处理:
。为了使废水的排放达标,进行如图处理:

常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的pH=_____ 。备注:Ksp[Cr(OH)3]=6.0×10-31 Kw=1×10-14
Ⅰ.铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,FeSO4·H2O结构如图所示:

(1)从结构的角度看,Fe2+不如Fe3+稳定,原因是
(2)SO
 和H2O分子比较,
和H2O分子比较,(3)S原子核外有
Ⅱ.物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。根据所学知识,回答问题:
(4)一定温度下,向1L0.1mol/LCH3COOH溶液中加入少量CH3COONa固体,则溶液中
 的值
的值(5)25℃下,有浓度均为0.1mol/L的三种溶液:a.Na2CO3;b.NaClO;c.CH3COONa(已知25℃时电离常数:H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8;CH3COOH:Ka=1.8×10-5)往等浓度的Na2CO3、NaClO的混合溶液中加入少量醋酸,请写出发生反应的离子方程式
(6)已知25℃时,Ksp(AgCl)=1.8×10-10,现将足量氯化银固体分别放入:a.100mL蒸馏水中b.100mL0.2mol/LAgNO3溶液中;c.100mL0.1mol/L氯化铝溶液中;d.100mL0.1mol/L盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是
(7)含Cr2O
 的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3mol/L的Cr2O 。为了使废水的排放达标,进行如图处理:
。为了使废水的排放达标,进行如图处理:
常温下若处理后的废水中c(Cr3+)=6.0×10-7mol/L,则处理后的废水的pH=
您最近一年使用:0次



