名校
解题方法
1 . 氮元素可形成丰富的化合物,在生产生活中具有广泛用途。
(1) 是一种重要的化工原料,以
是一种重要的化工原料,以 合成
合成 ,常用
,常用 作催化剂。基态
作催化剂。基态 原子和基态
原子和基态 中未成对电子数之比为
中未成对电子数之比为_____ ;从轨道重叠方式的角度分析 的成键,
的成键, 分子中氮原子的
分子中氮原子的_____ 轨道与氢原子的 轨道重叠形成
轨道重叠形成 键。
键。
(2) 是中学化学常见微粒,键角:
是中学化学常见微粒,键角:
_____ (填“>”或“<”) 。
。
(3) (氨硼烷)的储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)的储氢量高,是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是_____
②比较沸点:
_____ (填“>”或“<”,下同) ,水溶性:
,水溶性:
_____  。
。
(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1)和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。
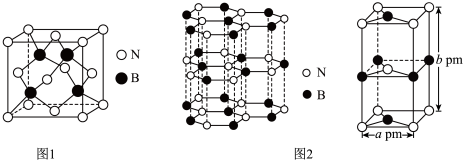
 —射线衍射实验测得立方氮化硼晶胞边长为
—射线衍射实验测得立方氮化硼晶胞边长为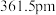 ,则立方氮化硼晶体中硼氮键的键长为
,则立方氮化硼晶体中硼氮键的键长为_____ (只列计算式) 。已知六方氮化硼密度为
。已知六方氮化硼密度为 ,底面角分别为
,底面角分别为 和
和 ,设
,设 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则
_____ (列含a、b、d的计算式即可)
(1)
 是一种重要的化工原料,以
是一种重要的化工原料,以 合成
合成 ,常用
,常用 作催化剂。基态
作催化剂。基态 原子和基态
原子和基态 中未成对电子数之比为
中未成对电子数之比为 的成键,
的成键, 分子中氮原子的
分子中氮原子的 轨道重叠形成
轨道重叠形成 键。
键。(2)
 是中学化学常见微粒,键角:
是中学化学常见微粒,键角:
 。
。(3)
 (氨硼烷)的储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)的储氢量高,是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②比较沸点:

 ,水溶性:
,水溶性:
 。
。(4)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,主要结构有立方氮化硼(如图1)和六方氮化硼(如图2),前者类似于金刚石,后者与石墨相似。

 —射线衍射实验测得立方氮化硼晶胞边长为
—射线衍射实验测得立方氮化硼晶胞边长为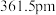 ,则立方氮化硼晶体中硼氮键的键长为
,则立方氮化硼晶体中硼氮键的键长为 。已知六方氮化硼密度为
。已知六方氮化硼密度为 ,底面角分别为
,底面角分别为 和
和 ,设
,设 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则
您最近一年使用:0次
2024-04-02更新
|
444次组卷
|
3卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高二下学期第1次月考化学试题
解题方法
2 .  既是化工原料,但也是空气污染物。回答下列问题:
既是化工原料,但也是空气污染物。回答下列问题:
(1)已知反应:
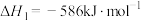 ;
;

 ;
;
则反应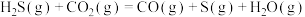 的
的
_______  。
。
(2) 与
与 在高温下发生反应:
在高温下发生反应: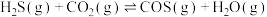
 。在610K时,将
。在610K时,将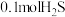 与
与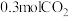 充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时
充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时 的物质的量分数为0.125,用
的物质的量分数为0.125,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
_______ 。 的平衡转化率
的平衡转化率
______ %。
(3)利用 的热分解反应可生产
的热分解反应可生产 :
: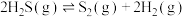 。现将
。现将 通入某恒压(压强
通入某恒压(压强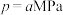 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。

已知:对于气相反应,用某组分(B)的平衡分压( )代替物质的量浓度(
)代替物质的量浓度(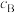 )也可表示平衡常数(
)也可表示平衡常数( )。(
)。(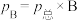 的物质的量分数,
的物质的量分数, 为平衡时气体总压强)。
为平衡时气体总压强)。
温度升高时,混合气体的平均摩尔质量_______ (填“增大”“减小”或“不变”)。温度为 ℃时。该反应的平衡常数
℃时。该反应的平衡常数
_______ MPa(用含a的代数式表示)。
(4)据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。 在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
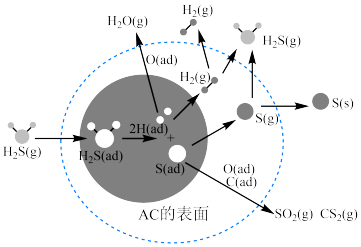
① 、
、 、
、 的键角从小到大排列顺序为
的键角从小到大排列顺序为_______ 。
②下列有关叙述错误的是_______ (填字母)。
A.图中阴影部分表示 分子的吸附与解离
分子的吸附与解离
B.AC表面的温度不同, 的去除率不同
的去除率不同
C. 在AC表面作用生成的产物有
在AC表面作用生成的产物有 、
、 、S、
、S、 、
、 等
等
D.图中反应过程中只有 链的断裂。没有
链的断裂。没有 健的形成
健的形成
 既是化工原料,但也是空气污染物。回答下列问题:
既是化工原料,但也是空气污染物。回答下列问题:(1)已知反应:

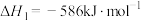 ;
;
 ;
;则反应
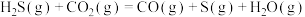 的
的
 。
。(2)
 与
与 在高温下发生反应:
在高温下发生反应: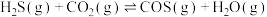
 。在610K时,将
。在610K时,将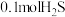 与
与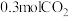 充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时
充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时 的物质的量分数为0.125,用
的物质的量分数为0.125,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
 的平衡转化率
的平衡转化率
(3)利用
 的热分解反应可生产
的热分解反应可生产 :
: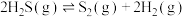 。现将
。现将 通入某恒压(压强
通入某恒压(压强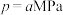 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:对于气相反应,用某组分(B)的平衡分压(
 )代替物质的量浓度(
)代替物质的量浓度(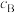 )也可表示平衡常数(
)也可表示平衡常数( )。(
)。(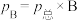 的物质的量分数,
的物质的量分数, 为平衡时气体总压强)。
为平衡时气体总压强)。温度升高时,混合气体的平均摩尔质量
 ℃时。该反应的平衡常数
℃时。该反应的平衡常数
(4)据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。
 在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
①
 、
、 、
、 的键角从小到大排列顺序为
的键角从小到大排列顺序为②下列有关叙述错误的是
A.图中阴影部分表示
 分子的吸附与解离
分子的吸附与解离B.AC表面的温度不同,
 的去除率不同
的去除率不同C.
 在AC表面作用生成的产物有
在AC表面作用生成的产物有 、
、 、S、
、S、 、
、 等
等D.图中反应过程中只有
 链的断裂。没有
链的断裂。没有 健的形成
健的形成
您最近一年使用:0次
解题方法
3 . 钛合金是以钛元素为基础加入其他元素组成的合金,因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。回答下列问题:
(1)已知 在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与
在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与 相似。
相似。 的晶体类型是
的晶体类型是__________ 。 稳定性比
稳定性比 差,试从化学键角度分析原因
差,试从化学键角度分析原因__________ 。
(2)纳米 是一种应用广泛的催化剂,其催化作用的一个实例如下所示:
是一种应用广泛的催化剂,其催化作用的一个实例如下所示:

化合物乙的沸点明显高于化合物甲,主要原因是______________________________ 。
(3)配离子 中Ti的化合价为
中Ti的化合价为__________ ,配体为__________ 。
(4)金属钛(Ti)与氮形成的某种化合物常被用作高温结构材料和超导材料。研究表明,用Al代替其中部分的Ti可提升耐磨性5倍以上,掺杂Al后的晶胞结构如图所示。已知该晶体属立方晶系,阿佛加德罗常数的值为 。回答下列问题:
。回答下列问题:

①b点原子的分数坐标为__________ 。
②掺杂Al后,晶体中
__________ 。
③已知最近的两个N原子之间的距离为cnm,则氮化钛晶体的密度为__________ 
(1)已知
 在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与
在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与 相似。
相似。 的晶体类型是
的晶体类型是 稳定性比
稳定性比 差,试从化学键角度分析原因
差,试从化学键角度分析原因(2)纳米
 是一种应用广泛的催化剂,其催化作用的一个实例如下所示:
是一种应用广泛的催化剂,其催化作用的一个实例如下所示:
化合物乙的沸点明显高于化合物甲,主要原因是
(3)配离子
 中Ti的化合价为
中Ti的化合价为(4)金属钛(Ti)与氮形成的某种化合物常被用作高温结构材料和超导材料。研究表明,用Al代替其中部分的Ti可提升耐磨性5倍以上,掺杂Al后的晶胞结构如图所示。已知该晶体属立方晶系,阿佛加德罗常数的值为
 。回答下列问题:
。回答下列问题:
①b点原子的分数坐标为
②掺杂Al后,晶体中

③已知最近的两个N原子之间的距离为cnm,则氮化钛晶体的密度为

您最近一年使用:0次
解题方法
4 . 硅和碳及其化合物多是新型无机非金属材料。
(1)金刚石属于_______ 晶体, 属于
属于_______ 晶体,石墨属于_______ 晶体,它们都是碳元素的_______ 。
(2)石墨烯是只由一层碳原子所构成的平面薄膜,富勒烯以 为代表,结构如下图。
为代表,结构如下图。
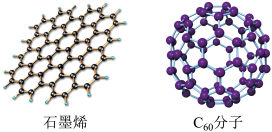
从石墨中剥离得到石墨烯需克服的作用是_______ ;在石墨烯中,每个六元环占有_______ 个C原子。1mol  分子中σ键数为
分子中σ键数为_______ (用 表示)。
表示)。
(3)碳化硅(化学式:SiC)与晶体硅(化学式:Si)和金刚石(化学式:C)相比较,三者熔点从高到低的顺序(用化学式和“>”表示):_______ 。
(4)氮化硅是一种高温陶瓷材料,已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子稳定结构,请写出氮化硅的化学式:_______ 。
(5)已知化学键的键能数据如下表:
已知反应热:△H=反应物的总键能之和-生成物的总键能之和。则反应 )的△H=
)的△H=_______ kJ/mol。
(1)金刚石属于
 属于
属于(2)石墨烯是只由一层碳原子所构成的平面薄膜,富勒烯以
 为代表,结构如下图。
为代表,结构如下图。
从石墨中剥离得到石墨烯需克服的作用是
 分子中σ键数为
分子中σ键数为 表示)。
表示)。(3)碳化硅(化学式:SiC)与晶体硅(化学式:Si)和金刚石(化学式:C)相比较,三者熔点从高到低的顺序(用化学式和“>”表示):
(4)氮化硅是一种高温陶瓷材料,已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子稳定结构,请写出氮化硅的化学式:
(5)已知化学键的键能数据如下表:
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能kJ/mol | 360 | 436 | 431 | 176 |
 )的△H=
)的△H=
您最近一年使用:0次
5 . 短周期主族元素A、B、C、D、E原子序数依次增大,B、C、D同周期,A原子核外电子只有一种自旋取向:C的基态原子的最外层有3个未成对电子,次外层有2个电子:B、D两种原子p能级上都有2个未成对电子,E原子的价电子中,在不同形状的原子轨道中运动的电子数相等,请回答下列问题(用元素符号或化学式回答问题):
(1)B、C、D三种元素第一电离能由大到小_______ 电负性由小到大的顺序_______
(2)元素As与C同族。推测As的氢化物 的空间构型
的空间构型_______ ; 沸点比
沸点比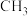 的
的_______ (填“高”或“低”),其判断理由是_______ ;元素的氢化物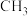 的键角
的键角_______  的键角(填>,<或=),原因是
的键角(填>,<或=),原因是_______
(3)A、B、D元素可以形成多种有机酸,如甲酸(HCOOH)、乙酸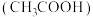 、丙酸
、丙酸 等,乙酸中碳原子的轨道杂化方式为
等,乙酸中碳原子的轨道杂化方式为_______ :甲酸的酸性大于乙酸,乙酸的酸性大于丙酸,试解释原因_______
(4)S元素与D同族, 的一种三聚体环状结构如图所示,该结构中
的一种三聚体环状结构如图所示,该结构中 键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为_______ (填a或b):E位于元素周期表的_______

(1)B、C、D三种元素第一电离能由大到小
(2)元素As与C同族。推测As的氢化物
 的空间构型
的空间构型 沸点比
沸点比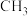 的
的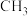 的键角
的键角 的键角(填>,<或=),原因是
的键角(填>,<或=),原因是(3)A、B、D元素可以形成多种有机酸,如甲酸(HCOOH)、乙酸
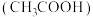 、丙酸
、丙酸 等,乙酸中碳原子的轨道杂化方式为
等,乙酸中碳原子的轨道杂化方式为(4)S元素与D同族,
 的一种三聚体环状结构如图所示,该结构中
的一种三聚体环状结构如图所示,该结构中 键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
键长有两类,一类键长约140pm,另一类键长约为169pm,较长的键为
您最近一年使用:0次



