名校
解题方法
1 . 现有下列有机物:A. B.
B. C.
C. D.
D. ,完成下列问题:
,完成下列问题:
(1)A分子中碳原子轨道的杂化类型为_______ 。
(2)1molB分子中含有的σ键的数目为_______ 。
(3)A中官能团的名称是:_______ 。
(4)写出由A制取B的化学方程式:_______ 。
(5)写出A制取C、D两种物质的有机反应类型:A→C:__ 、A→D:___ 。
 B.
B. C.
C. D.
D. ,完成下列问题:
,完成下列问题:(1)A分子中碳原子轨道的杂化类型为
(2)1molB分子中含有的σ键的数目为
(3)A中官能团的名称是:
(4)写出由A制取B的化学方程式:
(5)写出A制取C、D两种物质的有机反应类型:A→C:
您最近一年使用:0次
名校
解题方法
2 . 氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______ 。基态碳原子的核外电子占有______ 个原子轨道。
(2)光化学烟雾中除了含有NOx外,还含有HCOOH、 (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN中C的杂化方式有______ 。1mol PAN中含有的σ键数目为______ 。组成PAN的元素的电负性大小顺序为______ 。
②相同压强下,HCOOH的沸点比CH3OCH3______ (填“高”或“低”),
(3)水溶液中有H3O+、 、
、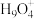 等微粒的形式。请画出
等微粒的形式。请画出 的结构式:
的结构式:______ 。
(1)宇宙中含量最多的元素是氢和
(2)光化学烟雾中除了含有NOx外,还含有HCOOH、
 (PAN)等二次污染物。
(PAN)等二次污染物。①PAN中C的杂化方式有
②相同压强下,HCOOH的沸点比CH3OCH3
(3)水溶液中有H3O+、
 、
、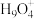 等微粒的形式。请画出
等微粒的形式。请画出 的结构式:
的结构式:
您最近一年使用:0次
名校
3 . (1)CH 、CH3、CH
、CH3、CH 都是重要的有机反应中间体,它们的电子式分别是
都是重要的有机反应中间体,它们的电子式分别是________ 、________ 、________ ;其中CH 中四个原子是共平面的,三个键角相等,则键角应是
中四个原子是共平面的,三个键角相等,则键角应是________ 。
(2)叠氮化合物在化学工业上有重要应用。N 叫做叠氮离子,请写出3种由三个原子构成的含有与N
叫做叠氮离子,请写出3种由三个原子构成的含有与N 的电子数相同的粒子的化学式
的电子数相同的粒子的化学式______ 、______ 、______ 。
(3)N≡N键的键能为946 kJ/mol,N—N键的键能为193 kJ/mol,说明N2中的________ 键比________ 键稳定(填“σ”或“π”)
(4)CaC2中C 与O
与O 互为等电子体,O
互为等电子体,O 的电子式可表示为
的电子式可表示为________________ ;1 mol O 中含有的π键数目为
中含有的π键数目为________ 。
(5)PH3在常温下是一种无色、剧毒、易自燃的气体,分子结构和NH3相似。在常温下1体积的水能溶解0.26体积的PH3,PH3和卤化氢(HX)作用生成相应的化合物PH4X,PH4X在水溶液中完全水解(PH 结构类似于CH4)。PH3的分子结构的形状是
结构类似于CH4)。PH3的分子结构的形状是________ ;在PH 中P-H键之间的夹角是
中P-H键之间的夹角是_____ 。
 、CH3、CH
、CH3、CH 都是重要的有机反应中间体,它们的电子式分别是
都是重要的有机反应中间体,它们的电子式分别是 中四个原子是共平面的,三个键角相等,则键角应是
中四个原子是共平面的,三个键角相等,则键角应是(2)叠氮化合物在化学工业上有重要应用。N
 叫做叠氮离子,请写出3种由三个原子构成的含有与N
叫做叠氮离子,请写出3种由三个原子构成的含有与N 的电子数相同的粒子的化学式
的电子数相同的粒子的化学式(3)N≡N键的键能为946 kJ/mol,N—N键的键能为193 kJ/mol,说明N2中的
(4)CaC2中C
 与O
与O 互为等电子体,O
互为等电子体,O 的电子式可表示为
的电子式可表示为 中含有的π键数目为
中含有的π键数目为(5)PH3在常温下是一种无色、剧毒、易自燃的气体,分子结构和NH3相似。在常温下1体积的水能溶解0.26体积的PH3,PH3和卤化氢(HX)作用生成相应的化合物PH4X,PH4X在水溶液中完全水解(PH
 结构类似于CH4)。PH3的分子结构的形状是
结构类似于CH4)。PH3的分子结构的形状是 中P-H键之间的夹角是
中P-H键之间的夹角是
您最近一年使用:0次
4 . PM2.5中的某些物质,易引发光化学烟雾污染,光化学烟雾中含有NOx、OCS、CH2=CH-CHO、HCOOH、以及光气等二次污染物。水污染程度可通过测定水体中铅、铬等重金属的含量判断。
(1)C、N、O三种元素的第一电离能从大到小的顺序为_______ (用元素符号表示),CH2=CH-CHO分子醛基中碳原子杂化方式为____________ 。
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为_________ ;光气(COCl2)各原子最外层都满足8电子稳定结构,则光气分子的空间构型为_________ (用文字描述);
(3)1molHCOOH中含σ键和π键数目之比为______________ 。
(4)基态Cr原子核外电子排布式是_______ ,配合物[Cr(NH3)4(H2O)2] Cl3中心离子的配体为_______ 。
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=______ (填数字)。若两个相邻面心的Kr原子的核间距为acm,用NA表示阿伏伽德罗常数,M表示Kr的相对原子质量。该晶体的密度计算式为______ g/cm3。
(1)C、N、O三种元素的第一电离能从大到小的顺序为
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
(3)1molHCOOH中含σ键和π键数目之比为
(4)基态Cr原子核外电子排布式是
(5)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中晶胞中含Kr原子为m个,与每个Kr原子紧相邻的Kr原子有n个,则m/n=

您最近一年使用:0次
真题
名校
5 . 生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式___ 。
(2)根据等电子原理,写出CO分子的结构式_________ 。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O 沉淀。
①甲醇的沸点比甲醛的高,其主要原因是____________________ ;
甲醛分子中碳原子轨道的杂化类型为_________ 。
②甲醛分子的空间构型是_________ ;
1mol甲醛分子中σ键的数目为_____ 。
③在1个Cu2O 晶胞中(结构如图所示),_______ 。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式
(2)根据等电子原理,写出CO分子的结构式
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O 沉淀。
①甲醇的沸点比甲醛的高,其主要原因是
甲醛分子中碳原子轨道的杂化类型为
②甲醛分子的空间构型是
1mol甲醛分子中σ键的数目为
③在1个Cu2O 晶胞中(结构如图所示),

您最近一年使用:0次
2016-12-09更新
|
686次组卷
|
5卷引用:河北省唐山市曹妃甸区第一中学2016-2017学年高二下学期期末考试化学试题
河北省唐山市曹妃甸区第一中学2016-2017学年高二下学期期末考试化学试题2009年普通高等学校招生统一考试化学试题(江苏卷)(已下线)2014年高二鲁科版选修3化学规范训练3.4几类其他聚集状态物质练习卷(已下线)2015届安徽省滁州中学高三九月份化学月考试卷河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷



