名校
1 .  表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A. 所含质子数为8 所含质子数为8 | B.18 g冰中含有的氢键数目为2 |
C.31 g白磷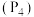 中含有P-P键的数目为6 中含有P-P键的数目为6 | D.1 mol CsCl晶体中含有CsCl分子数为 |
您最近一年使用:0次
名校
解题方法
2 .  代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.12 g金刚石中含有 共价键的数目为 共价键的数目为 |
B.20 g的 中含有的质子数为 中含有的质子数为 |
C.28 g的乙烯气体中所含原子总数为 |
D.1 mol苯含有σ键的数目为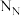 |
您最近一年使用:0次
名校
解题方法
3 . 磷、碳、氢、氧等非金属及其化合物用途广泛。回答下列问题:
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为_______ 。(用NA表示阿伏伽德罗常数的值)
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为_______ 。
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为_______ ,产生的阳离子的空间结构为_______ 。
(2)分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为_______ ,一定在同一平面上的原子有_______ 个;乙醇显中性而苯酚显酸性的原因是:在大π键中氧的p电子云向苯环转移,_______ 。
(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。
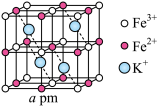
①该化合物的化学式为_______ 。
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为_______ pm;该晶体的密度为_______ g•cm-3(阿伏加德罗常数为NA)
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为
(2)分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。

①该化合物的化学式为
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为
您最近一年使用:0次
名校
4 . 黑火药是中国古代四大发明之一。爆炸反应为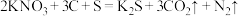 。下列有关说法不正确的是
。下列有关说法不正确的是
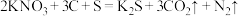 。下列有关说法不正确的是
。下列有关说法不正确的是A.离子半径: | B. 分子的空间结构为直线形 分子的空间结构为直线形 |
C. 含离子键和共价键 含离子键和共价键 | D. 分子中 分子中 键与 键与 键的数目比为 键的数目比为 |
您最近一年使用:0次
2023-05-19更新
|
540次组卷
|
5卷引用:海南省海口市2023年高三高考模拟化学试题
海南省海口市2023年高三高考模拟化学试题江西省九江市彭泽县第二高级中学2022-2023学年高二下学期7月期末化学试题(已下线)考点巩固卷06 物质结构与性质(4大考点55题)-2024年高考化学一轮复习考点通关卷(新高考通用)湖南省常德市汉寿县第一中学2023-2024学年高三上学期10月月考化学试题湖南省岳阳县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
5 . “ ”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是

 ”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
| A.分子中,中心原子采用sp3杂化的只有①③ |
| B.①分子为正四面体结构,④分子为平面形 |
| C.②分子中σ键:π键=2:1 |
| D.四种分子的键角大小顺序为②>③>①>④ |
您最近一年使用:0次
2021-04-01更新
|
171次组卷
|
4卷引用:海南省洋浦中学2023-2024学年高三上学期10月月考化学试题
6 . 乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ; lmol  中含有的π键数目为
中含有的π键数目为_______ 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为_______ 。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是_______ ;分子中处于同一直线上的原子数目最多为_______ 。
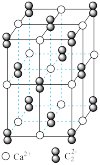
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),则该晶胞中的碳原子个数为_______ 。 CaC2晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的 数目为
数目为_______ 。
(1)CaC2中
 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的π键数目为
中含有的π键数目为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),则该晶胞中的碳原子个数为
 的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的
的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的 数目为
数目为
您最近一年使用:0次
2018-06-03更新
|
486次组卷
|
2卷引用:海南省白沙县2023届高三水平调研测试化学试题



