1 . 设 为阿伏加德罗常数的值。砷化镓
为阿伏加德罗常数的值。砷化镓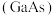 是半导体材料,气相生长法制备
是半导体材料,气相生长法制备 的原理如下:
的原理如下:
①
②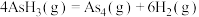
③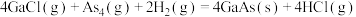
下列叙述正确的是
 为阿伏加德罗常数的值。砷化镓
为阿伏加德罗常数的值。砷化镓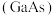 是半导体材料,气相生长法制备
是半导体材料,气相生长法制备 的原理如下:
的原理如下:①

②
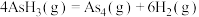
③
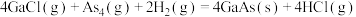
下列叙述正确的是
A.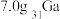 的最外层电子数为 的最外层电子数为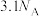 |
B.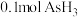 中含共价键数目为 中含共价键数目为 |
C.标准状况下,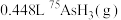 含中子的数目为 含中子的数目为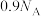 |
D.反应③中每生成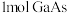 转移的电子数目为 转移的电子数目为 |
您最近一年使用:0次
名校
2 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.11.2L  含π键数目为 含π键数目为 |
B.NaCl和 的混合物中含1mol 的混合物中含1mol  ,则混合物中质子数为28 ,则混合物中质子数为28 |
C.电解熔融 ,阴极增重6.4g,外电路中通过电子的数目为0.1 ,阴极增重6.4g,外电路中通过电子的数目为0.1 |
D.1.7g  完全溶于1L 完全溶于1L  所得的溶液中, 所得的溶液中, 微粒的数目为0.1 微粒的数目为0.1 |
您最近一年使用:0次
7日内更新
|
242次组卷
|
3卷引用:2024届广东省高州市第一中学高三下学期5月考前热身训练化学试题
解题方法
3 . 咪唑( )是生产抗真菌药物的主要原料之一,下列说法错误的是
)是生产抗真菌药物的主要原料之一,下列说法错误的是
| A.咪唑分子为极性分子 | B.分子中C-N键的极性小于N-H键的极性 |
C.分子中 键与 键与 键个数比为9∶2 键个数比为9∶2 | D.咪唑中两个N原子均为 杂化 杂化 |
您最近一年使用:0次
4 . 下列说法正确的是
A.原子轨道的能量: | B.元素最高正化合价: |
C. 的键角: 的键角: | D. 中 中 键与 键与 键的数目比为 键的数目比为 |
您最近一年使用:0次
解题方法
5 . 设NA为阿伏加德罗常数的值。下列说法错误的是
| A.1mol过氧化氢所含的共价键数目为3NA |
B.1mol白磷P4(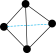 )含6NA个P-P键 )含6NA个P-P键 |
| C.等物质的量的CO2和N2中含有π键的数目均为2NA |
| D.1mol金刚石晶体中含有2NA个C-C键,1mol二氧化硅中含4NA个Si-O键 |
您最近一年使用:0次
名校
6 . 芬顿法常用于废水的处理,反应为:NH4OCN+3H2O2=N2↑+CO2↑+5H2O,设NA为阿伏加德罗常数,下列有关说法正确的是
| A.100g质量分数为17%的H2O2溶液中,氧原子总数为NA |
| B.0℃,101KPa下,22.4L CO2中含有σ键数目为4NA |
| C.25℃,101KPa下,20g D2O中含有中子数目为10NA |
| D.1mol NH4OCN参与反应时转移电子数为3NA |
您最近一年使用:0次
名校
7 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol 固体与足量的 固体与足量的 充分反应,转移 充分反应,转移 个电子 个电子 |
B.1mol 中含有 中含有 键的数目约为 键的数目约为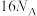 |
C.1L0.1mol/L 酸性溶液中所含 酸性溶液中所含 的数目为 的数目为 |
D.0.05mol/L的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近一年使用:0次
解题方法
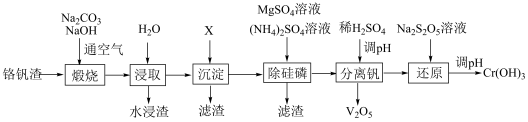
8 . 铬和钒具有广泛用途,铬钒中铬和钒以低价态含氧酸盐形式存在,主要杂质为氧化铁及铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示: 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
②氧化性: 。
。
请回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为______ ,基态V原子的未成对电子数为______ 。
(2)“煅烧”后,若铬被氧化为相应的最高价含氧酸盐,则 元素以化合物
元素以化合物______ (填化学式,下同)的形式存在;水浸渣的主要成分为 和
和______ ,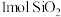 中含有的
中含有的 键数目为
键数目为______ 。
(3)“沉淀”步骤得到的滤渣为 ,X可选择______(填标号)。
,X可选择______(填标号)。
(4)“还原”步骤中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为__________________ 。
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。②氧化性:
 。
。请回答下列问题:
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)“煅烧”后,若铬被氧化为相应的最高价含氧酸盐,则
 元素以化合物
元素以化合物 和
和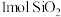 中含有的
中含有的 键数目为
键数目为(3)“沉淀”步骤得到的滤渣为
 ,X可选择______(填标号)。
,X可选择______(填标号)。A. 溶液 溶液 | B.氨水 | C.硫酸溶液 | D.盐酸 |
(4)“还原”步骤中加入
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
您最近一年使用:0次
9 . 下列有关分子结构的描述正确的是
A. 中心原子为 中心原子为 杂化,分子呈三角锥形 杂化,分子呈三角锥形 |
B. 的VSEPR模型为V形 的VSEPR模型为V形 |
| C.HCHO分子为平面三角形,分子中含3个σ键和一个π键 |
D. 为正四面体形分子,能与水分子形成分子间氢键 为正四面体形分子,能与水分子形成分子间氢键 |
您最近一年使用:0次
名校
解题方法
10 . HC≡C-CH=NH是一种星际分子。下列关于该分子结构的说法正确的是
| A.每个分子中含有6个σ键和3个π键 | B.分子中所有碳原子均为sp杂化 |
| C.分子中所有碳原子在同一直线上 | D.氮原子为sp3杂化 |
您最近一年使用:0次
2024-05-09更新
|
73次组卷
|
2卷引用:广东省珠海市第一中学2023-2024学年高二下学期第一阶段考试化学科试题



