名校
1 . 下列说法中不正确的是
A. 键比 键比 键重叠程度大,形成的共价键通常更牢固 键重叠程度大,形成的共价键通常更牢固 |
B.两个原子之间形成共价键时,最多有一个 键 键 |
C.气体单质中,一定有 键,可能有 键,可能有 键 键 |
D. 分子中有一个 分子中有一个 键,2个 键,2个 键 键 |
您最近半年使用:0次
2023-04-08更新
|
231次组卷
|
87卷引用:吉林省长春市第二十九中学2020-2021学年高二下学期第一学程考试化学试题
吉林省长春市第二十九中学2020-2021学年高二下学期第一学程考试化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题江苏省南通市如皋中学2020-2021学年高一下学期第二次阶段考试化学试题吉林省乾安县第七中学2020-2021学年高二下学期第六次质量检测化学试题江西省九江市柴桑区第一中学2020-2021学年高二下学期5月月考化学试题天津市蓟州区燕山中学2021-2022学年高三上学期第一次月考化学试题(已下线)2012-2013学年福建三明泰宁一中高二下第一次阶段考试化学试卷(已下线)2012-2013学年湖北省荆州市监利县柘木中学高二下第二次月考化学卷2015-2016学年河北省邢台一中高二上12月月考化学试卷2015-2016学年四川省成都市新都一中高二下4月月考化学试卷黑龙江省齐齐哈尔市第八中学2017-2018学年高二3月月考化学试题贵州省习水县一中2018-2019学年高二上学期12月份月考化学试题贵州省毕节市黔西县第一中学2018-2019学年高二上学期12月份考试化学试题【全国百强校】河北省衡水市武邑中学2018-2019学年高二12月月考化学试题【全国百强校】山西省实验中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二下学期4月月考化学试题福建省泉州市泉港区第一中学2018-2019学年高二下学期第二次月考化学试题云南省通海三中2018-2019学年高二下学期6月份考试化学试题吉林省汪清县第六中学2018-2019学年高二6月月考化学试题云南省丘北县第二中学2018-2019学年高二下学期6月份考试化学试题云南省玉溪市新平三中2019-2020学年高二上学期12月份月考化学试题山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题河北省正定中学2019-2020学年高二3月线上月考化学试题吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题河北省沧州市任丘市第一中学2019-2020学年高二6月月考化学试题江苏省东台创新高级中学2019-2020学年高二下学期4月份月检测化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第一节 共价键 第1课时 共价键鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第1节 共价键模型 第1课时 共价键的形成(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第1节 共价键模型高二选择性必修2(人教版2019)第二章 分子结构与性质 第一节综合训练(已下线)第2章 微粒间相互作用与物质性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)(已下线)模块同步卷11 综合检测卷(基础卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)2.1 共价键(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)新疆维吾尔自治区乌鲁木齐市第四中学2020-2021学年高二年级下学期期中考试化学试题甘肃省兰州市第一中学2020-2021学年高二下学期期中考试化学试题吉林省辽源市田家炳高级中学2020-2021学年高二下学期期中化学试题黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题福建省仙游县枫亭中学2020-2021学年高二下学期期中考试化学试题辽宁省鞍山市2020-2021学年高二下学期期末考试化学试题(已下线)课时55 分子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)2.1.1 共价键的类型-σ键和π键-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)内蒙古赤峰二中2021-2022学年高二下学期第二次月考化学试题贵州省凯里学院附属中学2021-2022学年高二下学期3月月考化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题广东省惠州市博罗县博师高级中学2022-2023学年高二下学期3月考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题(已下线)2010-2011学年福建省师大附中高二下学期期中考试化学试卷(已下线)2011-2012学年新疆农七师高级中学高二下学期期末考试试化学试卷(已下线)2012-2013学年辽宁葫芦岛第一高级中学高二下学期期中考试化学试卷(已下线)2012-2013学年河北省衡水市第十四中学高二下学期期末考试化学试卷福建省福州市八县(市)协作校2016-2017学年高二下学期期中考试化学试题福建省晋江市季延中学2017-2018学年高二上学期期中考试(理)化学试题高中化学人教版 选修三 第2章 分子结构与性质 共价键宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.1 第1课时云南省香格里拉县一中2018-2019学年高二上学期期中考试化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题云南省普洱市景东县第一中学2018-2019学年高二上学期期末考试化学试题云南省玉溪市江川区第二中学2018-2019学年高二上学期期末考试化学试题河北省唐山市开滦第二中学2018-2019学年高二下学期期中考试化学试题广西蒙山县第一中学2017-2018学年高二下学期期末考试化学试题新疆乌鲁木齐市第四中学2018-2019学年高二下学期期末考试化学试题广西壮族自治区蒙山县第一中学2019-2020学年高二下学期期末考试化学试题广西蒙山一中2018-2019学年高二下学期期末考试化学试题(已下线)专题11.2 分子结构与性质(讲)-《2020年高考一轮复习讲练测》江苏省徐州一中2019-2020学年高二上学期期末调研测试化学试题云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题河南省洛阳市2019-2020学年高二上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题宁夏回族自治区吴忠市吴忠中学2020年高二化学人教版选修3《物质结构与性质》综合测试湖北省武汉市武昌区水果湖高中 2019-2020 学年高二下学期期中考试化学试题陕西省宝鸡市渭滨区2018-2019学年高二下学期期末考试化学试题山东省泰安市2020年高二下学期化学期中考试(鲁科版)山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题新疆生产建设兵团第四师第一中学2019-2020学年高二下学期期中考试化学试题(已下线)练习19 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版)黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题(已下线)2.1.1 共价键的类型——σ键和π键(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)新疆乌鲁木齐市第四中学2021-2022学年高二下学期期中考试化学试题浙江省台州市三门启超中学等两校2021-2022学年高二下学期期中联考化学试题海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题专题3 微粒间作用力与物质性质 第三单元 共价键共价晶体 第1课时 共价键的形成及类型湖南省长沙市长郡梅溪湖中学2021-2022学年高二下学期入学考试化学试题新疆乌鲁木齐市第101中学2021-2022学年高二下学期期末考试化学试题吉林省吉林市田家炳高级中学2022-2023学年高二上学期期末线上考试化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题3.3.1共价键的形成和类型 课中
2 . NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,33.6LSO3和NO2的混合物中含有分子的数目为1.5NA |
| B.14g硅单质中含硅硅单键的数目为1NA |
| C.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间 |
| D.常温下,1 L pH=1的H2SO4溶液中H+的数目为0.2NA |
您最近半年使用:0次
3 . 含碳元素的物质是化学世界中最庞大的家族,请填写下列空格。
(1)CH4中的化学键从形成过程来看,属于_______ (填“σ”或“π”)键,从其极性来看属于_______ 键。
(2)CO2和CH3OH分子中C原子的杂化形式分别为_______ 和_______ 。
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为 ,每个COCl2分子内含有的σ键、π键数目为_______。
,每个COCl2分子内含有的σ键、π键数目为_______。
(4)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
甲:
_______ ;乙:
_______ 。
(1)CH4中的化学键从形成过程来看,属于
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)利用CO可以合成化工原料COCl2,COCl2分子的结构式为
 ,每个COCl2分子内含有的σ键、π键数目为_______。
,每个COCl2分子内含有的σ键、π键数目为_______。| A.4个σ键 | B.2个σ键、2个π键 | C.2个σ键、1个π键 | D.3个σ键、1个π键 |
甲:


您最近半年使用:0次
解题方法
4 . 下列模型分别表示 、
、 、
、 的结构,则下列说法错误的是
的结构,则下列说法错误的是

 、
、 、
、 的结构,则下列说法错误的是
的结构,则下列说法错误的是
A.32g 中含有0.125molσ键 中含有0.125molσ键 | B. 中只含有极性键 中只含有极性键 |
C.1mol 中含有3molσ键和2molπ键 中含有3molσ键和2molπ键 | D.1mol 中含有8molS—S键 中含有8molS—S键 |
您最近半年使用:0次
5 . 将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色。
(1)Cu的价电子轨道表达式为____ ;在周期表中,Cu元素属于___________ 区。
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:___________ 。
(3)向深蓝色溶液继续加入___________ ,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。[Cu(NH3)4]SO4·H2O中,1mol[Cu(NH3)4] 2+含有σ键的数目为___________ 。
(4)___________ (填“H2O”或“NH3”)与Cu2+形成的配位键更稳定。
(5)SO 的VSEPR模型名称为
的VSEPR模型名称为___________ ,H3O+空间构型为___________ 。
(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。
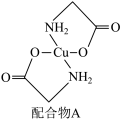
该结构中,除共价键外还存在配位键,请在图中用“→”表示出配位键___________ 。
(1)Cu的价电子轨道表达式为
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:
(3)向深蓝色溶液继续加入
(4)
(5)SO
 的VSEPR模型名称为
的VSEPR模型名称为(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。

该结构中,除共价键外还存在配位键,请在图中用“→”表示出配位键
您最近半年使用:0次
名校
解题方法
6 . Fe、HCN与K2CO3在一定条件下发生如下反应:Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,下列说法正确的是
| A.此化学方程式中涉及的第二周期元素的电负性由大到小的顺序为N>O>C |
B.配合物K4Fe(CN)6的中心离子的价电子排布图为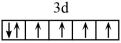 ,该中心离子的配位数是10 ,该中心离子的配位数是10 |
| C.1molHCN分子中含有σ键的数目为1.204×1024,HCN分子中碳原子轨道杂化类型是sp杂化 |
| D.K2CO3中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 |
您最近半年使用:0次
2022-04-12更新
|
136次组卷
|
2卷引用:江苏省海安高级中学2021-2022学年高二上学期阶段测试(二)化学试题
名校
7 . 在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气体)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:[Cu(NH3)2]+(aq)+CO(g)+NH3(g)⇌[Cu(NH3)3CO]+(aq) △H<0,下列有关说法错误的是
| A.低温高压有利于CO的吸收 |
| B.适当升高温度,可增大反应速率和CO的平衡转化率 |
| C.1mol[Cu(NH3)3CO]+中含有σ键为14mol |
| D.[Cu(NH3)2]+的物质的量浓度不再减小时,应达到最大限度 |
您最近半年使用:0次
名校
解题方法
8 . 请回答下列有关问题。
(1)Fe元素按周期表分区属于___________ 区元素
(2)地壳中含量最多的三种元素O、Si、Al中,电负性最大的是___________ 。
(3)钠在火焰上灼烧产生的黄光是一种___________ (填字母)
A.吸收光谱 B.发射光谱
(4)Cu的基态原子的电子排布式是___________ 。
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是___________ 。
(6)基态Fe3+与Fe2+离子中未成对的电子数之比为___________
(7)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________ 。
(8)H2O分子的空间构型为___________
(1)Fe元素按周期表分区属于
(2)地壳中含量最多的三种元素O、Si、Al中,电负性最大的是
(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)Cu的基态原子的电子排布式是
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(6)基态Fe3+与Fe2+离子中未成对的电子数之比为
(7)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(8)H2O分子的空间构型为
您最近半年使用:0次
名校
解题方法
9 . 有下列8种晶体:A.水晶B.白磷C.冰醋酸D.固态氩E.氯化铵F.铝G.金刚石H.烧碱。用序号回答下列问题:
(1)含有非极性键的原子晶体是_______ ;属于分子晶体的单质是_______ ;含有离子键、共价键、配位键的化合物是_______ ;受热熔化,需克服共价键的是_______ 。
(2)在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中的氧原子以配位键形式结合,这种结合是可逆的,比Fe2+与N的结合弱的原因是_______ 。
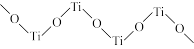
(3)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图,化学式为_______
(4)氨硼烷是一种特殊的化合物,分子式为NH3BH3.氨硼烷在催化剂作用下水解释放出氢气: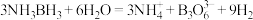 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题:

①请写出氧原子价电子轨道表达式_______ 。
②NH3BH3晶体中含有的微粒间作用力有_______ (填标号)。
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
③已知钛的一种常见化合物是 。1mol该物质中含有σ键的数目为
。1mol该物质中含有σ键的数目为_______
(5)图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是_______
(1)含有非极性键的原子晶体是
(2)在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中的氧原子以配位键形式结合,这种结合是可逆的,比Fe2+与N的结合弱的原因是
(3)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图,化学式为

(4)氨硼烷是一种特殊的化合物,分子式为NH3BH3.氨硼烷在催化剂作用下水解释放出氢气:
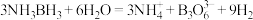 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题:
①请写出氧原子价电子轨道表达式
②NH3BH3晶体中含有的微粒间作用力有
a.非极性共价键 b.配位键 c.氢键 d.范德华力 e.金属键
③已知钛的一种常见化合物是
 。1mol该物质中含有σ键的数目为
。1mol该物质中含有σ键的数目为(5)图象是NaCl、CsCl、ZnS等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于NaCl的晶体结构的图是_______
A.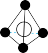 | B.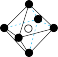 | C.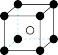 | D.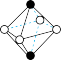 |
您最近半年使用:0次
名校
10 . 设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标况下,11.2LC3H8含有极性键数目为5NA |
| B.1mol[Cu(H2O)4]2+中含σ键数目为12NA |
| C.31g白磷分子中含有的σ键数目为NA |
| D.78gNa2O2与足量H2O反应后转移的电子数目为2NA |
您最近半年使用:0次



