解题方法
1 . 元素周期表中前四周期元素W、X、Y、Z、Q,它们的原子序数依次增大,且分布于四个不同的周期。W是宇宙中含量最多的元素;X是形成化合物种类最多的元素;Y与X同周期,Y元素最高价氧化物的水化物能与其简单氢化物反应生成盐;Z元素的电负性在同周期元素中最大;Q的基态原子在前四周期中未成对电子数最多。下列说法错误的是
| A.非金属性:Y>X>W |
| B.简单气态氢化物的沸点:Y>Z>X |
C.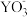 中所有的原子不都在同一平面上 中所有的原子不都在同一平面上 |
| D.Q所在的周期中,基态原子最外层电子数相同的元素有3种 |
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
| A.碱金属和碱土金属元素均位于元素周期表的p区 |
B.NaCl中化学键的离子键百分数比 中的低 中的低 |
C. 中存在 中存在 与 与 之间的强烈相互作用 之间的强烈相互作用 |
D. 中 中 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近一年使用:0次
2024·黑龙江·模拟预测
3 . 反应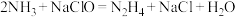 可用于制备火箭推进剂的燃料
可用于制备火箭推进剂的燃料 ,下列说法正确的是
,下列说法正确的是
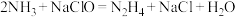 可用于制备火箭推进剂的燃料
可用于制备火箭推进剂的燃料 ,下列说法正确的是
,下列说法正确的是| A.N2H4分子中没有非极性键 | B.NaClO的电子式为 |
C.H2O、NH3的 模型一致 模型一致 | D.食盐的分子式为NaCl |
您最近一年使用:0次
解题方法
4 . 下列化学用语表述错误的是
A. 的电子式为 的电子式为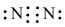 |
B.中子数为28的钙原子是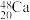 |
C. 分子的 分子的 模型为 模型为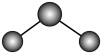 |
D.基态 原子的价层电子排布图为 原子的价层电子排布图为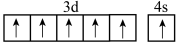 |
您最近一年使用:0次
解题方法
5 . 下列化学用语的表达错误的是
A | B |
| BeCl2的球棍模型 | 尿素的空间填充模型 |
|
|
C | D |
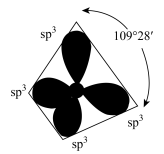
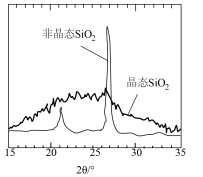
| CH4分子中碳原子杂化轨道的电子云轮廓图 | 非晶态和晶态SiO2粉末X射线衍射图谱对比 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列有关化学用语表不正确的是
A.反-2-丁烯结构简式: |
B. 电子式: 电子式: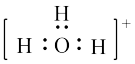 |
C. 的VSEPR模型: 的VSEPR模型: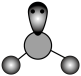 |
D.HCl中σ键的形成: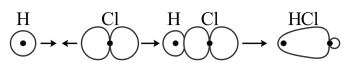 |
您最近一年使用:0次
解题方法
7 . 硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )在我国分布广泛,储量丰富。目前一种利用硫铁矿制备新能源汽车电池的电极
)在我国分布广泛,储量丰富。目前一种利用硫铁矿制备新能源汽车电池的电极 的工艺流程如下图所示:
的工艺流程如下图所示:
(1)基态Fe原子的价电子排布式为_______ 。
(2) 的VSEPR模型是
的VSEPR模型是_______ 。
(3)“焙烧”时,发生的主要反应的化学方程式是_______ 。
(4)从“焙烧”到“氧化”要经历4步,请从下列步骤选择正确的步骤并合理排序_______ 。_______ 。
(6)产品纯度的测定。分别取2.000g产品三次,用稀硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.1000
 溶液滴定至溶液由浅绿色变为蓝紫色,平均消耗
溶液滴定至溶液由浅绿色变为蓝紫色,平均消耗 溶液20.00mL,则产品
溶液20.00mL,则产品 的纯度为
的纯度为_______ 。(精确到0.1%)
(7)已知新能源汽车的磷酸亚铁锂电池(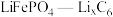 )放电时的总反应为:
)放电时的总反应为: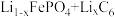
 。充电时阳极反应为:
。充电时阳极反应为:_______ 。
 ,含少量
,含少量 、
、 和
和 )在我国分布广泛,储量丰富。目前一种利用硫铁矿制备新能源汽车电池的电极
)在我国分布广泛,储量丰富。目前一种利用硫铁矿制备新能源汽车电池的电极 的工艺流程如下图所示:
的工艺流程如下图所示: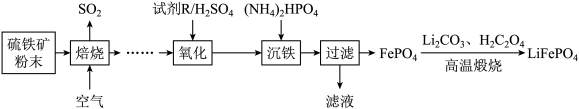
| 金属氢氧化物 |  |  |  |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 3.7 | 9.7 | 5.2 |
(1)基态Fe原子的价电子排布式为
(2)
 的VSEPR模型是
的VSEPR模型是(3)“焙烧”时,发生的主要反应的化学方程式是
(4)从“焙烧”到“氧化”要经历4步,请从下列步骤选择正确的步骤并合理排序

(6)产品纯度的测定。分别取2.000g产品三次,用稀硫酸溶解,滴加二苯胺磺酸钠指示剂,用0.1000

 溶液滴定至溶液由浅绿色变为蓝紫色,平均消耗
溶液滴定至溶液由浅绿色变为蓝紫色,平均消耗 溶液20.00mL,则产品
溶液20.00mL,则产品 的纯度为
的纯度为(7)已知新能源汽车的磷酸亚铁锂电池(
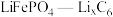 )放电时的总反应为:
)放电时的总反应为: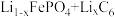
 。充电时阳极反应为:
。充电时阳极反应为:
您最近一年使用:0次
解题方法
8 . X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X、Y、Z位于同一周期,且互不相邻,三者的最外层电子数之和为15,基态Y原子的价电子层中有3个未成对电子,Z与Q同主族,M原子在同周期中原子半径最大,下列说法不正确 的是
| A.化学键中离子键成分的百分数:MZ>MQ |
| B.键角:XZ3<YQ3 |
| C.Z、M、Q原子形成稀有气体电子构型的简单离子的半径:M<Z<Q |
| D.最高价氧化物对应水化物的酸性:X<Y |
您最近一年使用:0次
解题方法
9 . 下列表示不正确 的是
A.质子数为92、中子数为146的U原子: |
B.HClO的电子式: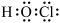 |
C.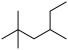 的名称:2,2,4-三甲基己烷 的名称:2,2,4-三甲基己烷 |
D.H2S的价层电子对互斥(VSEPR)模型: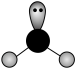 |
您最近一年使用:0次
2024-05-13更新
|
680次组卷
|
2卷引用:浙江省宁波市2024届高三下学期二模化学试题
10 . 下列化学用语或图示表达正确的是
A.中子数为18的氯原子:  |
B.碳的基态原子轨道表示式: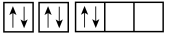 |
C. 的 的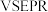 模型: 模型: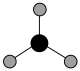 |
D. 分子中 分子中 键的形成: 键的形成: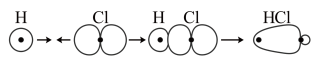 |
您最近一年使用:0次