1 . 物质类别和元素价态是认识物质两个重要维度。下图列为硫及其化合物的价类二维图,下列说法错误的是
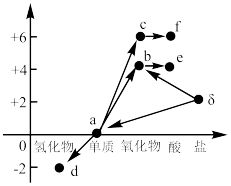
A.附着有a的试管,可用 清洗 清洗 | B.b和d反应生成a时,d发生还原反应 |
| C.b、c两种氧化物的VSEPR模型相同 | D.g的钠盐可与f的稀溶液反应生成a和b |
您最近半年使用:0次
名校
解题方法
2 . NA为阿伏加德罗常数的值。下列说法错误的是
| A.46gCH3CH2OH中sp3杂化的原子数为2NA | B.0.5molXeF4中氙的价层电子对数为3NA |
| C.标准状况下,80gSO3中含有分子数为NA | D.1mol晶体硅中Si-Si键的数目为2NA |
您最近半年使用:0次
名校
3 . 下列说法中正确的个数为
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③ 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致
④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
①Cu的第二电离能大于Zn的第二电离能
②H与Cl以1﹕1的关系结合为HCl是因为共价键具有方向性
③
 的VSEPR模型与空间结构一致
的VSEPR模型与空间结构一致④在冰晶体中,每个H2O分子周围紧邻的分子有4个,是因为水分子之间存在氢键,氢键也具有方向性和饱和性
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
名校
4 . 黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)基态Cu原子的价层电子的轨道表达式为___________ 。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体H2S产生。
①H2S分子的立体构型是___________ ,中心原子杂化类型为___________ ,属于___________ (填极性"或“非极性”)分子。
②H2S分子量比水大,沸点却比水低,主要原因是___________ 。
(3)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为___________ ,键角___________ 120°(填“>”或“=”或“<"),原因是___________ 。
(4)CuFeS2晶胞结构如图所示。___________ 。
②已知:晶胞为长方体,三个边长分别为anm、bnm、cnm,NA为阿伏加德罗常数,CuFeS2晶体的密度___________ g·cm-3(列出计算式)。(1nm=10-9m)
(1)基态Cu原子的价层电子的轨道表达式为
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体H2S产生。
①H2S分子的立体构型是
②H2S分子量比水大,沸点却比水低,主要原因是
(3)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
(4)CuFeS2晶胞结构如图所示。
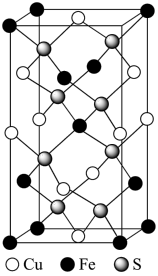
②已知:晶胞为长方体,三个边长分别为anm、bnm、cnm,NA为阿伏加德罗常数,CuFeS2晶体的密度
您最近半年使用:0次
解题方法
5 . 化合物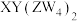 可作食品膨松剂,W、X、Y、Z为原子序数依次增大的短周期元素,W的基态原子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含量最多的金属元素,下列说法正确的是
可作食品膨松剂,W、X、Y、Z为原子序数依次增大的短周期元素,W的基态原子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含量最多的金属元素,下列说法正确的是
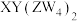 可作食品膨松剂,W、X、Y、Z为原子序数依次增大的短周期元素,W的基态原子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含量最多的金属元素,下列说法正确的是
可作食品膨松剂,W、X、Y、Z为原子序数依次增大的短周期元素,W的基态原子s能级上的电子总数和p能级上的电子总数相等,W和Z同族,Y是地壳中含量最多的金属元素,下列说法正确的是| A.第一电离能:X>Y>Z | B.简单氢化物沸点:Z>W |
| C.原子半径:Z>Y>X>W | D.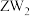 和 和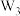 的空间结构均为V形 的空间结构均为V形 |
您最近半年使用:0次
名校
解题方法
6 . 物质的结构影响物质的性质。请回答下列问题。
(1)P4S3可用于制造火柴,其分子结构如图所示。电负性:硫___________ 磷(填“>”“<”或“=”),P4S3分子中硫原子的杂化轨道类型为___________ 。1molP4S3分子中孤电子对的数目为___________ ,∠S—P—S___________ 109°28'(填“>”“<”或“=”)。

(2)化合物Cl2O的空间结构为___________ ,中心原子的价层电子对数为___________ 。
(3) 、
、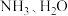 分子的空间结构和相应的键角如图甲所示。
分子的空间结构和相应的键角如图甲所示。___________ ,原因是___________ 。H2O的键角小于NH3的,分析原因:___________ 。
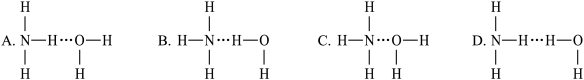
(4)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为___________ 。(填序号)
(1)P4S3可用于制造火柴,其分子结构如图所示。电负性:硫

(2)化合物Cl2O的空间结构为
(3)
 、
、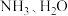 分子的空间结构和相应的键角如图甲所示。
分子的空间结构和相应的键角如图甲所示。
(4)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
您最近半年使用:0次
2024-04-29更新
|
92次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题
解题方法
7 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.22.4 L氨气中孤电子对数为NA |
| B.0.5 mol XeF4中Xe的价层电子对数为3NA |
| C.23 g CH3CH2OH中sp3杂化的原子数为NA |
| D.氢原子数为0.4NA的CH3OH分子中σ键数为0.4NA |
您最近半年使用:0次
名校
解题方法
8 . 下列说法正确的是
| A.杂化轨道只用于形成σ键 |
B. 分子N原子的杂化方式为 分子N原子的杂化方式为 |
C. 的VSEPR模型为三角锥形 的VSEPR模型为三角锥形 |
D.HF分子间氢键可表示为: |
您最近半年使用:0次
解题方法
9 . 下列离子的 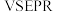 模型与其空间结构一致的是
模型与其空间结构一致的是
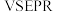 模型与其空间结构一致的是
模型与其空间结构一致的是A. | B. | C. | D. |
您最近半年使用:0次
10 . 下列说法正确的是
| A.利用红外光谱可以测定分子的相对分子质量 |
B.苹果酸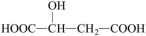 含有1个手性碳原子 含有1个手性碳原子 |
| C.AsH3分子的中心原子上的孤电子对数为3 |
| D.基态S原子核外电子的运动状态有9种 |
您最近半年使用:0次
2024-04-29更新
|
332次组卷
|
2卷引用:广东省湛江市第二十一中学2023-2024学年高二下学期第一次月考化学试卷



