解题方法
1 . ABm型分子的价电子对数的计算方法
对于ABm型分子(A是中心原子,B是配位原子),分子的价电子对数可以通过下式确定:
价电子对数目(n)=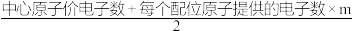
(1)中心原子的价电子数=___________ ;
(2)配位原子提供的价电子数:
卤素原子、氢原子按提供1个价电子数计算,O、S作为配位原子时按不提供价电子计算。如PCl5中n=___________ 。
(3)对于复杂离子,在计算价电子对数时,还应加上或减去离子所带的电荷数。如 中n=
中n=___________ , 中n=
中n=___________ 。
(4)若剩余1个电子,即出现奇数电子,也把这个单电子当作1对电子处理。如NO2中n=________ 。
对于ABm型分子(A是中心原子,B是配位原子),分子的价电子对数可以通过下式确定:
价电子对数目(n)=
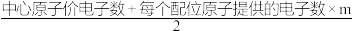
(1)中心原子的价电子数=
(2)配位原子提供的价电子数:
卤素原子、氢原子按提供1个价电子数计算,O、S作为配位原子时按不提供价电子计算。如PCl5中n=
(3)对于复杂离子,在计算价电子对数时,还应加上或减去离子所带的电荷数。如
 中n=
中n= 中n=
中n=(4)若剩余1个电子,即出现奇数电子,也把这个单电子当作1对电子处理。如NO2中n=
您最近一年使用:0次
解题方法
2 . 价层电子对互斥模型的基本要点
(1)价电子对:包括孤电子对和成键电子对,即价电子对数=_______ +_______ 。在价层电子对互斥模型中,成键电子对数等于成键数目,不用区别单键还是双键。
(2)价电子对的几何构型:
分子中的价电子对由于相互排斥作用,而趋向于尽可能___________ 以减小斥力,分子尽可能采取___________ 的空间构型。
价电子对数分别为2、3、4时,价电子对的几何分布分别为______ 、_______ 、_______ 。
(1)价电子对:包括孤电子对和成键电子对,即价电子对数=
(2)价电子对的几何构型:
分子中的价电子对由于相互排斥作用,而趋向于尽可能
价电子对数分别为2、3、4时,价电子对的几何分布分别为
您最近一年使用:0次
解题方法
3 . H2O分子的空间构型
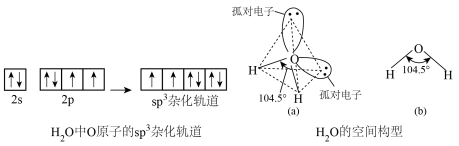
(1)杂化轨道类型:O原子上的1个2s轨道与3个2p轨道混合,形成4个_______ 化轨道,杂化轨道的空间构型是_______ 。
(2)成键情况:O原子的2个_______ 杂化轨道分别与H原子的_______ 轨道重叠,形成2个_______ 键,_______ 对孤电子对没有参加成键。
(3)空间构型:由于孤电子对—成键电子对的排斥作用_______ 成键电子对—成键电子对作用,使键角_______ 109°28'。H2O分子的空间构型为_______ ,键角为104°30'。

(1)杂化轨道类型:O原子上的1个2s轨道与3个2p轨道混合,形成4个
(2)成键情况:O原子的2个
(3)空间构型:由于孤电子对—成键电子对的排斥作用
您最近一年使用:0次
解题方法
4 . sp杂化与BeCl2分子的空间构型
(1)杂化轨道的形成
Be原子2s轨道上的1个电子进入2p轨道,_______ 个2s轨道和_______ 个2p轨道发生杂化,形成_______ 相等、_______ 相同的_______ 个sp杂化轨道。
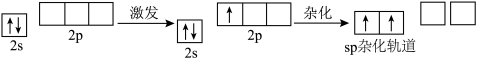

Be原子的sp杂化轨道呈_______ ,其夹角为_______ 。
(2)共价键的形成
Be原子的2个_______ 轨道分别与2个Cl原子的1个_______ 轨道重叠形成2个相同的_______ 键。
(3)BeCl2分子的空间构型
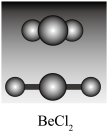
BeCl2分子为空间构型为_______ ,分子中Be—Cl键之间的夹角为_______ 。
(1)杂化轨道的形成
Be原子2s轨道上的1个电子进入2p轨道,


Be原子的sp杂化轨道呈
(2)共价键的形成
Be原子的2个
(3)BeCl2分子的空间构型

BeCl2分子为空间构型为
您最近一年使用:0次
解题方法
5 . 某元素基态原子价电子排布式为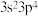 ,下列说法不正确的是
,下列说法不正确的是
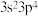 ,下列说法不正确的是
,下列说法不正确的是| A.该原子位于周期表p区 |
| B.该元素的最高正价为+4价 |
| C.该基态原子中存在两个未成对电子 |
| D.该元素最简单氢化物的空间构型是V形 |
您最近一年使用:0次
解题方法
6 . 下列说法中正确的是
A.p轨道与p轨道不能形成 键 键 |
B. 键可以绕键轴旋转, 键可以绕键轴旋转, 键不能绕键轴旋转 键不能绕键轴旋转 |
| C.BF3分子含有非极性共价键,空间结构为平面正三角形 |
| D.乙烯中碳碳双键的键能是乙烷中碳碳单键的键能的2倍 |
您最近一年使用:0次
真题
解题方法
7 . 下列化学用语表示正确的是
A. 分子的球棍模型: 分子的球棍模型: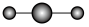 |
B. 的价层电子对互斥模型: 的价层电子对互斥模型: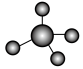 |
C. 的电子式: 的电子式: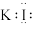 |
D.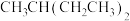 的名称:3−甲基戊烷 的名称:3−甲基戊烷 |
您最近一年使用:0次
8 . 下列化学用语表述错误的是
A.HClO的电子式: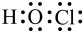 |
B.中子数为10的氧原子: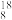 O O |
C.NH3分子的VSEPR模型: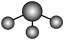 |
D.基态N原子的价层电子排布图: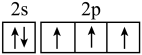 |
您最近一年使用:0次
2023-06-16更新
|
11411次组卷
|
34卷引用:专题02 化学用语
(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)专题02 化学用语(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第18讲原子结构和核外电子排布(已下线)专题02 化学用语的正误判断-2023年高考化学真题题源解密(全国通用)(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)考点17 原子结构和核外电子排布(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)吉林省长春市2024届高三上学期质量监测(一)化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)天津市第四中学2023-2024学年高三上学期第二次月考化学试卷辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)北京市师范大学附属实验中学2024届高三零模化学试题山西省太原师范学院附属中学 师苑中学校2023-2024学年高二下学期准高三第二次月考化学试题黑龙江省肇东市第四中学2023-2024学年高三上学期期末考试化学试题北京市大兴区第一中学2023-2024学年高二下学期期中考试化学试题广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题北京市顺义区第一中学2023-2024学年高二下学期期中考试化学试题2023年高考湖南卷化学真题(已下线)2023年湖南卷高考真题变式题(选择题1-5)甘肃省武威市凉州区2024届高三上学期第一次诊断考试化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷广西玉林市博白县中学2023-2024学年高三上学期开学考试化学试题宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷广东省深圳市盐田高级中学2023-2024学年高二上学期1月期末化学试题(已下线)选择题6-10宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期第四次月考理综试题(已下线)化学(九省联考考后提升卷,贵州卷)-2024年1月“九省联考”真题完全解读与考后提升湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 (已下线)2023-2024学年度第二学期高三化学零模试卷安徽省淮北市第一中学2023-2024学年高二下学期第一次月考化学试题黑龙江省齐齐哈尔市第八中学校2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
9 . 检验微量砷的原理为 。
。 常温下为无色气体。下列说法正确的是
常温下为无色气体。下列说法正确的是
 。
。 常温下为无色气体。下列说法正确的是
常温下为无色气体。下列说法正确的是A.As的基态核外电子排布式为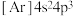 | B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C.固态 属于共价晶体 属于共价晶体 | D. 既含离子键又含共价键 既含离子键又含共价键 |
您最近一年使用:0次
2023-06-02更新
|
1213次组卷
|
8卷引用:江苏省扬州市2023届高三下学期三模化学试题
江苏省扬州市2023届高三下学期三模化学试题(已下线)考点巩固卷06 物质结构与性质(4大考点55题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)热点17 分子结构与性质江苏省淮安市2022-2023学年高二下学期6月期末考试化学试题江苏省基地大联考2023-2024学年高三上学期第一次质量监测化学试题江苏省南京师范大学苏州实验学校2023-2024学年高三上学期零模考试热身练化学试题山东省济宁市第一中学2024届高三下学期4月份定时检测化学试题江苏省苏州市南京师范大学苏州实验学校2024届高三下学期二模考试化学(选修)试卷
名校
10 . 下列化学用语或图示表达,错误的是
A.三氯氧磷的电子式: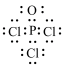 | B.二氧化硫的VSEPR模型: |
C.溴乙烷的空间填充模型: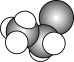 | D.铝原子最高能级的电子云轮廓图: |
您最近一年使用:0次



