解题方法
1 . 回答下列问题。
(1)计算下列分子中中心原子的孤电子对数:
①H2S ___________ ;②P Cl5___________ ;③B F3___________ ;④N H3___________ 。
(2)计算下列分子中中心原子的价层电子对数:
①CCl4___________ ;②BeCl2___________ ;③BCl3___________ ;④PCl3___________ 。
(1)计算下列分子中中心原子的孤电子对数:
①H2
(2)计算下列分子中中心原子的价层电子对数:
①CCl4
您最近一年使用:0次
名校
2 . 随着科学的发展,氟及其化合物的用途日益广泛。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。 是制备此离子液体的原料。
是制备此离子液体的原料。
(1)微粒中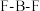 键角:
键角:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2) 可以与
可以与 反应生成
反应生成 的原因是
的原因是___________ 。
Ⅱ.氟化镁钾( )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。 晶体中,每个
晶体中,每个 周围有
周围有___________ 个距离最近的F。
(4) 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态 价电子的轨道表示式为
价电子的轨道表示式为___________ 。
②某实验室合成新型催化剂材料 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为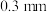 、面积为
、面积为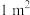 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为___________  (
(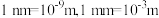 ,阿伏加德罗常数约为
,阿伏加德罗常数约为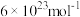 )。
)。
(5)我国科研工作者以 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。已知
。已知 与
与 的结构简式如下:
的结构简式如下: 中N原子的杂化方式为
中N原子的杂化方式为___________ , 中心N原子的杂化方式为
中心N原子的杂化方式为___________ 。
② 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着___________ ,上述相互作用不会随 的转动改变。
的转动改变。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。
 是制备此离子液体的原料。
是制备此离子液体的原料。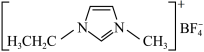
(1)微粒中
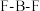 键角:
键角:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)
 可以与
可以与 反应生成
反应生成 的原因是
的原因是Ⅱ.氟化镁钾(
 )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。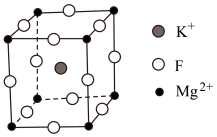
 晶体中,每个
晶体中,每个 周围有
周围有(4)
 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。①基态
 价电子的轨道表示式为
价电子的轨道表示式为②某实验室合成新型催化剂材料
 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为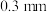 、面积为
、面积为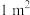 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为 (
(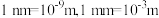 ,阿伏加德罗常数约为
,阿伏加德罗常数约为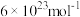 )。
)。(5)我国科研工作者以
 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
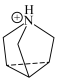
位置沿棱方向嵌入直线型 。已知
。已知 与
与 的结构简式如下:
的结构简式如下: :
:
 :
: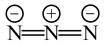
 中N原子的杂化方式为
中N原子的杂化方式为 中心N原子的杂化方式为
中心N原子的杂化方式为②
 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着 的转动改变。
的转动改变。
您最近一年使用:0次
名校
3 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
2024-04-26更新
|
178次组卷
|
2卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高二下学期入学考试化学试题
名校
解题方法
4 . 下列描述正确的是
①CS2为V形的极性分子;② 的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和
的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和 的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
①CS2为V形的极性分子;②
 的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和
的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和 的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键| A.①②③ | B.②③④ | C.③④⑤ | D.①④⑤ |
您最近一年使用:0次
2024-04-13更新
|
239次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高二下学期开学考试化学试题
解题方法
5 . 高氯酸三碳酰肼合镍化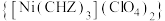 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:
(1)基态铜原子的价电子的轨道表示式为________ 。
(2)基态碳原子核外电子有________ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为________ , 的VSEPR模型是
的VSEPR模型是________ 。
(4)化学式中的CHZ为碳酰肼,其结构为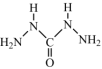 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:
①CHZ中氮原子的杂化轨道类型为________ 。
②1molCHZ中含有的 键数目为
键数目为________  。
。
③键角:
________ (填“>”“<”或“=”) 。
。
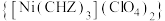 是一种新型的起爆药,回答下列问题:
是一种新型的起爆药,回答下列问题:(1)基态铜原子的价电子的轨道表示式为
(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)化学式中的CHZ为碳酰肼,其结构为
 ,是一种新型的环保锅炉水除氧剂:
,是一种新型的环保锅炉水除氧剂:①CHZ中氮原子的杂化轨道类型为
②1molCHZ中含有的
 键数目为
键数目为 。
。③键角:

 。
。
您最近一年使用:0次
名校
解题方法
6 . 下列说法错误的是
| A.价层电子对包括σ键电子对和中心原子上的孤电子对 |
B. 和 和 都是正四面体形微粒,且键角都为 都是正四面体形微粒,且键角都为 |
C. 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强 |
D. 、 、 、 、 、 、 分子中每个原子的最外层电子都满足了8电子稳定结构 分子中每个原子的最外层电子都满足了8电子稳定结构 |
您最近一年使用:0次
名校
7 . 侯氏制碱法主要反应之一为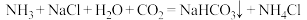 。下列说法正确的是
。下列说法正确的是
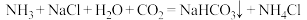 。下列说法正确的是
。下列说法正确的是A. 电子式: 电子式: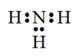 |
B. 在水溶液中的电离: 在水溶液中的电离: |
C. 与 与 具有相同的电子层结构 具有相同的电子层结构 |
D. 与 与 的 的 模型均为四面体 模型均为四面体 |
您最近一年使用:0次
解题方法
8 . 火药制备是我国古代闻名世界的化学工艺,原理为 。下列表示反应中相关粒子的化学用语正确的是
。下列表示反应中相关粒子的化学用语正确的是
 。下列表示反应中相关粒子的化学用语正确的是
。下列表示反应中相关粒子的化学用语正确的是A. 的结构示意图: 的结构示意图: |
B.在元素周期表中钾元素、硫元素均在 区 区 |
C. 的VSEPR模型: 的VSEPR模型: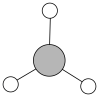 |
D. 的结构式为 的结构式为 ,且 ,且 键与 键与 键个数之比为 键个数之比为 |
您最近一年使用:0次
名校
9 .  为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是

 为原子序数依次增大的前四周期元素,基态原子中,
为原子序数依次增大的前四周期元素,基态原子中, 为元素周期表中半径最小的原子,
为元素周期表中半径最小的原子, 原子最外层电子数为次外层电子数的三倍,
原子最外层电子数为次外层电子数的三倍, 原子的价电子排布为
原子的价电子排布为 形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
形成的阳离子如图所示(狭长八面体结构),下列说法正确的是
A.原子半径: |
B.气态氢化物的稳定性: |
C.加热时该离子首先失去的组分是 |
D.两种配体中的键角: |
您最近一年使用:0次
名校
10 . 下列化学用语表述不正确的是
A.基态 原子的价层电子排布图(轨道表示式): 原子的价层电子排布图(轨道表示式):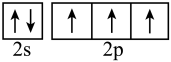 |
B. 分子的球棍模型: 分子的球棍模型: |
C. 的空间结构: 的空间结构: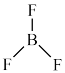 (平面三角形) (平面三角形) |
D. 分子的 分子的 模型: 模型: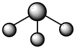 |
您最近一年使用:0次



