名校
1 . CuCl2和SO2发生氧化还原反应,离子方程式为 。设
。设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 。设
。设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.1 mol氯化铜固体含有的Cu2+数目小于 |
B.标准状况下,2.24 L H2O中心O原子的价层电子对数为0.4 |
C.1 mol SO2溶于水,电离出的H+数目为2 |
D.生成1 mol CuCl,转移的电子数为 |
您最近一年使用:0次
解题方法
2 . 近年来我国在高温超导材料的研究取得了重大突破,高温超导体仅出现在共价性很强的氧化物中,例如带有直线形的Cu-O-Cu链节的网格层对超导性有重要的作用。回答下列问题:
(1)基态Cu原子核外电子排布式为______ 。
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为______ 。
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为______ ;H2O2中氧原子的杂化方式为_______ 。
(4)硫酸铜溶于水后形成的水合铜离子的结构式为____ ,向硫酸铜溶液中逐滴加入氨水直至过量,观察到的现象为___ ,所得结论:与Cu2+形成配位键的能力H2O___ (填“强于”或“弱于”)NH3
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。
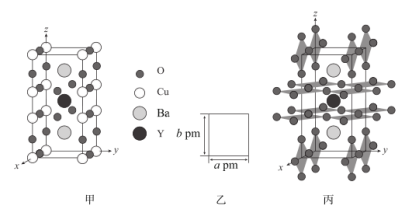
已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为______ 。
②若阿伏加德罗常数的值为NA,则晶体的密度为_____ g·cm-3(用含a、b、c和NA的表达式表示)。
(1)基态Cu原子核外电子排布式为
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为
(4)硫酸铜溶于水后形成的水合铜离子的结构式为
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。

已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为
②若阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
2022-01-22更新
|
1045次组卷
|
4卷引用:广东省肇庆市2021-2022学年高三第二次模拟考试化学试题
广东省肇庆市2021-2022学年高三第二次模拟考试化学试题安徽省“皖南八校”2022届高三下学期第三次联考理综化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)广东省2021-2022学年高三一轮复习质量检测化学试题
名校
解题方法
3 . 铜是人类广泛使用的第一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子最高能层的电子排布式为
原子最高能层的电子排布式为___________ 。
(2) 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。
(3) 与
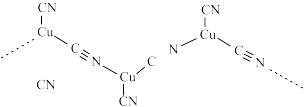
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为___________ 。
(4)铜能与拟卤素 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸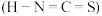 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为___________ ;写出一种与 互为等电子体的分子式
互为等电子体的分子式___________ 。
(5) 可形成
可形成 ,其中
,其中 代表
代表 。
。
①该化合物分子中, 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有___________ 个。
②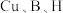 的电负性由大到小的顺序为
的电负性由大到小的顺序为___________ 。
(6)一种由 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
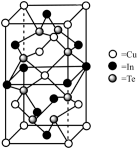
① 的配位数为
的配位数为___________ ;晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ 。
②若晶胞底边的边长均为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态
 原子最高能层的电子排布式为
原子最高能层的电子排布式为(2)
 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。A. | B. | C. | D. |
 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为
(4)铜能与拟卤素
 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸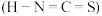 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为 互为等电子体的分子式
互为等电子体的分子式(5)
 可形成
可形成 ,其中
,其中 代表
代表 。
。①该化合物分子中,
 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有②
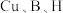 的电负性由大到小的顺序为
的电负性由大到小的顺序为(6)一种由
 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
①
 的配位数为
的配位数为 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为②若晶胞底边的边长均为
 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2021-12-03更新
|
1003次组卷
|
5卷引用:河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题
河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】20河北省石家庄市2022届高三上学期教学质量检测(一)化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题
名校
解题方法
4 . 我国科学家合成的某种离子化合物结构如下图,该物质由两种阳离子和两种阴离子构成,其中有两种10电子离子和一种18电子离子。X、Y、Z、M均为短周期元素,且均不在同一族;X是半径最小的元素,Z是空气中含量最多的元素,Y的电负性大于Z。下列说法不正确的是
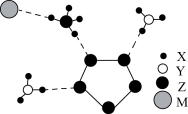

| A.X与Y形成的化合物沸点高于Y同族元素与X形成化合物的沸点主要原因是容易形成分子间氢键 |
| B.Z的最高价氧化物对应水化物的阴离子中Z的杂化方式为sp2杂化 |
| C.元素第一电离能:Y<Z |
| D.该盐中,存在离子键、极性共价键、非极性共价键、配位键和氢键等化学键 |
您最近一年使用:0次
名校
解题方法
5 . 短周期元素X、Y、Z、W的原子序数依次增大,元素X与Z可形成三角锥形的 分子,W与Y可形成平面三角形的
分子,W与Y可形成平面三角形的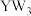 分子,X2遇W2即发生爆炸。下列说法中错误的是
分子,X2遇W2即发生爆炸。下列说法中错误的是
 分子,W与Y可形成平面三角形的
分子,W与Y可形成平面三角形的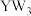 分子,X2遇W2即发生爆炸。下列说法中错误的是
分子,X2遇W2即发生爆炸。下列说法中错误的是A. 分子中Z原子的杂化方式为 分子中Z原子的杂化方式为 |
B.最高价氧化物的水化物的酸性 |
| C.Z的第一电离能在4种元素中最大 |
D. 分子与 分子与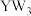 分子间可形成配位键 分子间可形成配位键 |
您最近一年使用:0次
2021-05-16更新
|
367次组卷
|
4卷引用:辽宁省沈阳市2021届高三年级教学质量监测(三)化学试题
解题方法
6 . 东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用丁造币,亦可用于制作仿银饰品。
回答下列问题:
(1)基态Ni原子的电子排布式为_______ ;Ni2+与Cu2+的3d能级上未成对电子数之比为_______ 。
(2)单质铜及镍都是由_______ 键形成的晶体。
(3)Ni2+与丁二酮肟反应生成鲜红色丁二酮肟镍沉淀(如图所示),该反应可用于检验Ni2+。
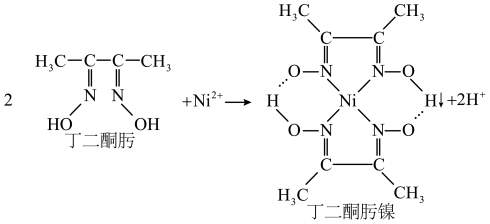
①1mol丁二酮肟分子中含有σ键的数目为_______ (用NA代表阿伏加德罗常数的值)。
②丁二酮肟镍分子中碳原子的杂化轨道类型为_______ 。
(4)CuSO4和Cu(NO3)2是自然界中重要的铜盐,其中S、O、N三种元素的第一电离能由大到小的顺序为_______ , SO 的立体构型是
的立体构型是_______ 。
(5)Cu、N两元素形成的某种化合物的晶胞结构如图。
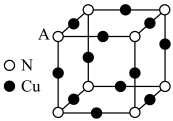
①该化合物的化学式为_______ 。
②该晶胞中,距离A处N原子最近的N原子构成的空间构型为_______ 。
③已知该晶胞的密度为ρg/cm-3,用NA代表阿伏加德罗常数的值,则紧邻的N原子与Cu原子之间的距离为_______ nm。(用含ρ、NA的代数式表示)
回答下列问题:
(1)基态Ni原子的电子排布式为
(2)单质铜及镍都是由
(3)Ni2+与丁二酮肟反应生成鲜红色丁二酮肟镍沉淀(如图所示),该反应可用于检验Ni2+。

①1mol丁二酮肟分子中含有σ键的数目为
②丁二酮肟镍分子中碳原子的杂化轨道类型为
(4)CuSO4和Cu(NO3)2是自然界中重要的铜盐,其中S、O、N三种元素的第一电离能由大到小的顺序为
 的立体构型是
的立体构型是(5)Cu、N两元素形成的某种化合物的晶胞结构如图。

①该化合物的化学式为
②该晶胞中,距离A处N原子最近的N原子构成的空间构型为
③已知该晶胞的密度为ρg/cm-3,用NA代表阿伏加德罗常数的值,则紧邻的N原子与Cu原子之间的距离为
您最近一年使用:0次
名校
解题方法
7 . 铁被称为“第一金属”,硫被称为“生命元素”,它们形成的物质种类非常丰富,在生产、生活中用途广泛。
(1)基态S原子有___ 种能量不同的电子,其价电子排布图为___ 。
(2)硫能形成S2O 、SO
、SO 等多种含氧酸根,试推测S2O
等多种含氧酸根,试推测S2O 的空间构型为
的空间构型为___ ,SO 的中心原子杂化方式为
的中心原子杂化方式为___ 。
(3)SCN-与Fe3+能发生显色反应,该反应常用作检验Fe3+的存在。
①铁元素位于元素周期表的___ 区。
②SCN-的三种元素的电负性由大到小的顺序为___ (用元素符号表示)。写出与SCN-互为等电子体的分子的分子式___ (任写一种)。
③Fe(SCN)3中不存在的化学键有___ (填标号)。
A.离子键B.极性键C.非极性键D.配位键E.σ键F.π键
(4)部分卤化铁的熔点如下表所示:
解释表中物质之间熔点差异的原因___ 。
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B两种方块组成。
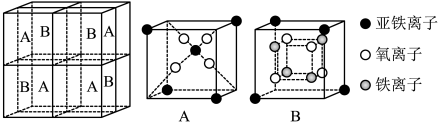
①该氧化物中Fe2+、Fe3+、O2-个数的最简整数比为___ 。
②已知该晶体的密度为dg·cm-3,阿伏加 德罗常数的值为NA,则晶胞参数a为___ nm(用含d和NA的代数式表示)。
(1)基态S原子有
(2)硫能形成S2O
 、SO
、SO 等多种含氧酸根,试推测S2O
等多种含氧酸根,试推测S2O 的空间构型为
的空间构型为 的中心原子杂化方式为
的中心原子杂化方式为(3)SCN-与Fe3+能发生显色反应,该反应常用作检验Fe3+的存在。
①铁元素位于元素周期表的
②SCN-的三种元素的电负性由大到小的顺序为
③Fe(SCN)3中不存在的化学键有
A.离子键B.极性键C.非极性键D.配位键E.σ键F.π键
(4)部分卤化铁的熔点如下表所示:
| 卤化铁 | FeF3 | FeCl3 |
| 熔点/℃ | 1100 | 306 |
解释表中物质之间熔点差异的原因
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B两种方块组成。

①该氧化物中Fe2+、Fe3+、O2-个数的最简整数比为
②已知该晶体的密度为dg·cm-3,阿伏加 德罗常数的值为NA,则晶胞参数a为
您最近一年使用:0次
解题方法
8 . 我国科研人员在钠离子电池研究中又取得新突破。钠离子电池与锂离子电池工作原理相同、制造工艺相似,而且具有资源丰富、成本低廉、安全性能好等特点。一种钠离子电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解质溶液为的碳酸丙烯酯溶液。
回答下列问题:
(1)基态Na原子的电子排布式为__ ,最高能层电子云轮廓图形状为___ 。
(2)Te与S同主族,与 同周期,Te属于元素周期表中
同周期,Te属于元素周期表中__ 区元素,其基态原子的价电子排布图(即轨道表示式)为___ 。
(3)碳酸丙烯酯的结构简式为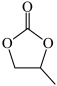 ,则其中π键和σ键的数目之比为
,则其中π键和σ键的数目之比为___ ,碳原子的杂化轨道类型为____ 。
(4)C元素的最高价氧化物的电子式为___ ,CO32-的VSEPR模型名称是___ ,ClO4-的立体构型是__ 。
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是__ ,该配离子包含的作用力为___ (填选项字母)。
A.极性键 B.金属键 C.氢键 D.配位键
(6)由原料制备负极材料的反应过程中,是否有电子转移___ (填“是”或者“否”)。
回答下列问题:
(1)基态Na原子的电子排布式为
(2)Te与S同主族,与
 同周期,Te属于元素周期表中
同周期,Te属于元素周期表中(3)碳酸丙烯酯的结构简式为
 ,则其中π键和σ键的数目之比为
,则其中π键和σ键的数目之比为(4)C元素的最高价氧化物的电子式为
(5)[Co(H2O)6]3+的几何构型为正八面体形,配体是
A.极性键 B.金属键 C.氢键 D.配位键
(6)由原料制备负极材料的反应过程中,是否有电子转移
您最近一年使用:0次
2020-05-19更新
|
148次组卷
|
2卷引用:天津市红桥区2020届高三下学期居家学习线上检测第一次模拟化学试题
名校
解题方法
9 . Fe、HCN与K2CO3在一定条件下发生如下反应:
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为___________________ 。
(2)配合物K4Fe(CN)6的中心离子是____________ ,该离子价电子的基态电子排布图为____________ 。
(3)lmol HCN分子中含有σ键的数目为____________ ,HCN分子中碳原子轨道杂化类型是____________ ,与CN-互为等电子体的阴离子是____________ 。
(4)K2CO3中阴离子的空间构型为____________ ,其中碳原子的价层电子对数为____________ 。
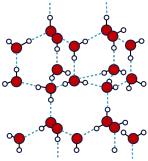
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有__________ 个氢键,若氢键键长为d nm,则晶体密度(g/cm3)计算式为____________ (用NA表示阿伏加德罗常数的值)。
Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为
(2)配合物K4Fe(CN)6的中心离子是
(3)lmol HCN分子中含有σ键的数目为
(4)K2CO3中阴离子的空间构型为
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞有

您最近一年使用:0次
2017-05-07更新
|
498次组卷
|
4卷引用:黑龙江省哈尔滨师范大学附属中学2017届高三第三次模拟考试化学试题



