解题方法
1 .  汽车尾气处理系统的原理是利用
汽车尾气处理系统的原理是利用 脱除
脱除 并转化为
并转化为 。
。
(1)已知在25℃, 时:
时:
反应ⅰ:

反应ⅱ: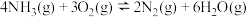
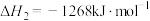
反应ⅲ:

________ 
(2)当 与
与 的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为
的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为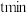 ,
, 的脱除率随温度变化的曲线如下图所示:
的脱除率随温度变化的曲线如下图所示: 与
与 的物质的量之比为
的物质的量之比为________ 。
②若曲线a中 的起始浓度为
的起始浓度为 ,则在900℃时
,则在900℃时 的脱除速率为
的脱除速率为________  。
。
③在800℃~1100℃时,催化剂活性较稳定。则 脱除的最佳温度为
脱除的最佳温度为________ ℃, 的脱除率在最佳温度之前逐渐增大的原因是
的脱除率在最佳温度之前逐渐增大的原因是________ 。
④940℃时,反应ⅲ的平衡常数
________ (用物质的量分数代替浓度,列计算式)。
⑤若其它条件不变,提高催化剂的活性,940℃时 的脱除率
的脱除率________ (选填“增大”“减小”或“不变”)。
(3)一定比例的 和
和 也能很好的脱除
也能很好的脱除 ,某催化反应机理如下图所示:
,某催化反应机理如下图所示: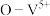 表示V化合价为
表示V化合价为 价,其它相似)
价,其它相似)
①该反应的催化剂为________ 。
② 转化为
转化为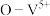 过程中
过程中 与
与 的物质的量比为
的物质的量比为________ 。
③ 转化为
转化为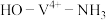 ,
, 键角增大的原因是
键角增大的原因是________ 。
 汽车尾气处理系统的原理是利用
汽车尾气处理系统的原理是利用 脱除
脱除 并转化为
并转化为 。
。(1)已知在25℃,
 时:
时:反应ⅰ:


反应ⅱ:
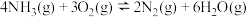
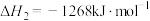
反应ⅲ:



(2)当
 与
与 的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为
的物质的量之比按1:3、3:1、4:1分别以相同流速通过催化剂,通过时间均为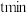 ,
, 的脱除率随温度变化的曲线如下图所示:
的脱除率随温度变化的曲线如下图所示:
 与
与 的物质的量之比为
的物质的量之比为②若曲线a中
 的起始浓度为
的起始浓度为 ,则在900℃时
,则在900℃时 的脱除速率为
的脱除速率为 。
。③在800℃~1100℃时,催化剂活性较稳定。则
 脱除的最佳温度为
脱除的最佳温度为 的脱除率在最佳温度之前逐渐增大的原因是
的脱除率在最佳温度之前逐渐增大的原因是④940℃时,反应ⅲ的平衡常数

⑤若其它条件不变,提高催化剂的活性,940℃时
 的脱除率
的脱除率(3)一定比例的
 和
和 也能很好的脱除
也能很好的脱除 ,某催化反应机理如下图所示:
,某催化反应机理如下图所示:
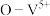 表示V化合价为
表示V化合价为 价,其它相似)
价,其它相似)①该反应的催化剂为
②
 转化为
转化为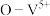 过程中
过程中 与
与 的物质的量比为
的物质的量比为③
 转化为
转化为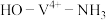 ,
, 键角增大的原因是
键角增大的原因是
您最近一年使用:0次
2024·黑龙江·模拟预测
解题方法
2 . CO2资源化利用受到越来越多的关注,它能有效减少碳排放,有效应对全球的气候变化,并且能充分利用碳资源。二氧化碳催化加氢制甲醇有利于减少温室气体排放,涉及的反应如下:
I.


II.
 kJ⋅mol-1
kJ⋅mol-1 
III.
 kJ⋅mol-1
kJ⋅mol-1 
回答下列问题:
(1)CO2分子的空间结构为___________ 形。
(2)
___________ kJ⋅mol-1。
(3)平衡常数
___________ (用 、
、 表示)。
表示)。
(4)为提高反应Ⅲ中 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。
(5)不同压强下,按照 投料,发生反应I,实验测得
投料,发生反应I,实验测得 的平衡转化率随温度的变化关系如下图所示。
的平衡转化率随温度的变化关系如下图所示。 、
、 由大到小的顺序为
由大到小的顺序为___________ ,判断的依据是___________ 。
②图中A点对应的甲醇的体积分数是___________ %(计算结果保留1位小数)。
(6)在恒温恒压(压强为p)的某密闭容器中,充入1mol 和3mol
和3mol ,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得
,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[
的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[ ]},则该温度下反应I的平衡常数
]},则该温度下反应I的平衡常数
___________ (写出计算式即可,分压=总压×物质的量分数)。
I.



II.

 kJ⋅mol-1
kJ⋅mol-1 
III.

 kJ⋅mol-1
kJ⋅mol-1 
回答下列问题:
(1)CO2分子的空间结构为
(2)

(3)平衡常数

 、
、 表示)。
表示)。(4)为提高反应Ⅲ中
 的平衡产率,应选择的反应条件为___________(填标号)。
的平衡产率,应选择的反应条件为___________(填标号)。| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
 投料,发生反应I,实验测得
投料,发生反应I,实验测得 的平衡转化率随温度的变化关系如下图所示。
的平衡转化率随温度的变化关系如下图所示。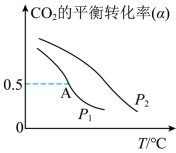
 、
、 由大到小的顺序为
由大到小的顺序为②图中A点对应的甲醇的体积分数是
(6)在恒温恒压(压强为p)的某密闭容器中,充入1mol
 和3mol
和3mol ,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得
,仅发生反应I和II,经过一段时间后,反应I和II达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[
的平衡转化率为20%,甲醇的选择性为50%{甲醇选择性[ ]},则该温度下反应I的平衡常数
]},则该温度下反应I的平衡常数
您最近一年使用:0次
解题方法
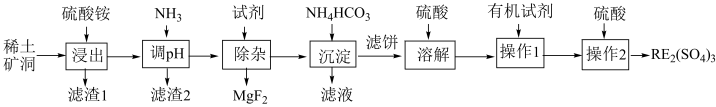
3 . 我国稀土工艺技术水平世界领先。从离子型稀土矿中(含RE、K、Al、Mg、Si、F等多种铝硅酸盐化合物,RE代表稀土元素)通过阳离子交换法提取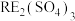 工艺流程如图。
工艺流程如图。
已知:①稀土矿中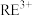 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子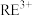
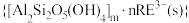 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将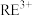 与
与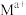 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。
②常温下部分难溶物的溶度积如表:
③pH对稀土和铝浸出率的影响如图:

回答下列问题:
(1)“滤渣1”中存在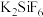 ,其阴离子的空间构型为
,其阴离子的空间构型为___________ 。“浸出”时最佳 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因___________ 。
(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式___________ (注明物质状态)。
(3)“沉淀”稀土离子的离子方程式为___________ 。
(4)回收利用“滤液”的操作单元是___________ 。
(5)“操作2”的名称为___________ ,实验室进行该步操作需要用到的玻璃仪器有___________ 。
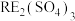 工艺流程如图。
工艺流程如图。
已知:①稀土矿中
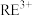 、
、 、
、 等主要吸附于铝硅酸盐中,稀土元素离子
等主要吸附于铝硅酸盐中,稀土元素离子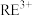
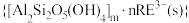 和杂质离子
和杂质离子 在矿洞中可与加入的盐溶液发生阳离子交换,将
在矿洞中可与加入的盐溶液发生阳离子交换,将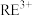 与
与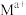 从铝硅酸盐中交换出来。
从铝硅酸盐中交换出来。②常温下部分难溶物的溶度积如表:
| 物质 |  |  | 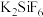 |
 | 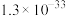 |  |  |

回答下列问题:
(1)“滤渣1”中存在
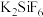 ,其阴离子的空间构型为
,其阴离子的空间构型为 为4.5,大于4.5稀土浸出率降低,解释原因
为4.5,大于4.5稀土浸出率降低,解释原因(2)矿洞中“浸出”时发生复杂反应,写出稀土离子交换的离子方程式
(3)“沉淀”稀土离子的离子方程式为
(4)回收利用“滤液”的操作单元是
(5)“操作2”的名称为
您最近一年使用:0次
解题方法
4 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族,颗粒约2~30微米,伴生矿物有钛铁矿等。回答下列问题:
(1)基态钛原子价电子排布式为_______ 。
(2)Fe的配合物有多种。 、
、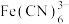 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是_______ (写元素符号,下同);第一电离能由大到小的顺序为_______ 。
(3)磷酸为磷的最高价含氧酸,其空间结构如图:
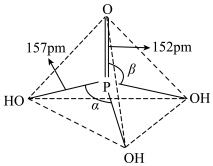
①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
② 的立体构型为
的立体构型为_______ ,中心原子的杂化类型是_______ 。
(4)反型钙钛矿电池无须使用具有光催化活性的 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
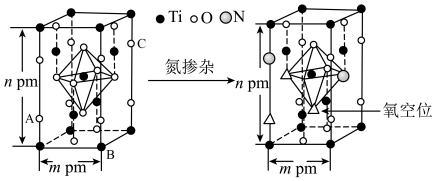
 晶体中
晶体中
_______ ;已知原子A、B的分数坐标分别为 和
和 ,则原子C的坐标为
,则原子C的坐标为_______ ,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为_______ g·cm 。
。
(1)基态钛原子价电子排布式为
(2)Fe的配合物有多种。
 、
、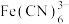 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是(3)磷酸为磷的最高价含氧酸,其空间结构如图:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②
 的立体构型为
的立体构型为(4)反型钙钛矿电池无须使用具有光催化活性的
 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
 晶体中
晶体中
 和
和 ,则原子C的坐标为
,则原子C的坐标为 ,
, 的密度为
的密度为 。
。
您最近一年使用:0次
2023-01-02更新
|
387次组卷
|
3卷引用:陕西省榆林市2023届高三第一次模拟理科综合化学试题
5 . 近年,我国科学家通过热磷化法制备出了电催化分解水的催化剂Co-Fe-P和Ni-Fe-P等过渡金属磷化物,将推动电解水制氢技术的快速发展。回答下列问题:
(1)铁元素在元素周期表中的位置_______ ,Fe3+的价电子排布式_______ 。
(2)磷的一些卤化物的熔沸点如表所示,试解释PF3、PCl3、PBr3、PI3熔沸点逐渐升高的原因_______
(3)磷酸具有很强的配位能力,PO 的中心原子杂化类型为
的中心原子杂化类型为_______ ,写出与PO 互为等电子体的一种分子
互为等电子体的一种分子_______
(4)钴的配合物种类很多,如[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl等,[Co(NO2)(NH3)5]2+的配位数是_______ ,其配体中的NH3的分子空间构型为_______ ;等物质的量的[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl分别与足量的硝酸银溶液反应,两者生成氯化银的质量比为_______ 。
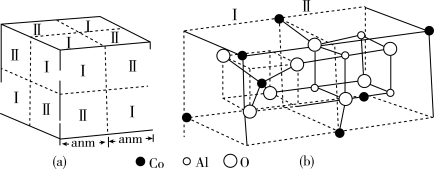
(5)钴蓝晶体结构如图(a)所示,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,求晶体的化学式为_______ ,密度为_______ g·cm-3。
(1)铁元素在元素周期表中的位置
(2)磷的一些卤化物的熔沸点如表所示,试解释PF3、PCl3、PBr3、PI3熔沸点逐渐升高的原因
| 卤化磷 | 熔点/K | 沸点/K |
| PF3 | 121.5 | 171.5 |
| PCl3 | 161 | 348.5 |
| PBr3 | 233 | 451.2 |
| PI3 | 334 | 573 |
 的中心原子杂化类型为
的中心原子杂化类型为 互为等电子体的一种分子
互为等电子体的一种分子(4)钴的配合物种类很多,如[Co(NO2)(NH3)5]Cl2和[Co(NH3)4Cl2]Cl等,[Co(NO2)(NH3)5]2+的配位数是
(5)钴蓝晶体结构如图(a)所示,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,求晶体的化学式为

您最近一年使用:0次
解题方法
6 . 中国科学技术大学吴长征教授团队通过四烷基铵阳离子的插层及随后对合适氧化还原电位的选择,成功剥离制备出二维非范德华 纳米片。回答下列问题:
纳米片。回答下列问题:
(1)基态硫原子核外有_______ 种电子运动状态,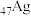 与铜元素同族,其基态原子价电子排布式
与铜元素同族,其基态原子价电子排布式_______ 。
(2)氧族元素有氧、硫、硒、碲等元素。 的
的 模型为
模型为_______ , 中碲的杂化轨道类型是
中碲的杂化轨道类型是_______ 。
(3)高氧化态 的过氧化物大多不稳定,容易分解,但
的过氧化物大多不稳定,容易分解,但 却是稳定的。这种配合物仍保持
却是稳定的。这种配合物仍保持 的过氧化物的结构特点,
的过氧化物的结构特点, 该配合物含有
该配合物含有_______  配位键(
配位键( 与O、N均形成了配位键);该结构中
与O、N均形成了配位键);该结构中 键角
键角_______ 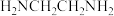 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4) 晶胞与
晶胞与 晶胞相似(如图),
晶胞相似(如图), 晶胞中部分原子的分数坐标为:A点
晶胞中部分原子的分数坐标为:A点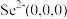 ,从该晶胞中找出距离B点
,从该晶胞中找出距离B点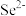 最远的
最远的 的位置
的位置_______ (用分数坐标表示),晶胞中距离最近的两个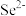 的距离为
的距离为 ,请计算
,请计算 晶胞的密度
晶胞的密度_______  。
。

 纳米片。回答下列问题:
纳米片。回答下列问题:(1)基态硫原子核外有
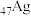 与铜元素同族,其基态原子价电子排布式
与铜元素同族,其基态原子价电子排布式(2)氧族元素有氧、硫、硒、碲等元素。
 的
的 模型为
模型为 中碲的杂化轨道类型是
中碲的杂化轨道类型是(3)高氧化态
 的过氧化物大多不稳定,容易分解,但
的过氧化物大多不稳定,容易分解,但 却是稳定的。这种配合物仍保持
却是稳定的。这种配合物仍保持 的过氧化物的结构特点,
的过氧化物的结构特点, 该配合物含有
该配合物含有 配位键(
配位键( 与O、N均形成了配位键);该结构中
与O、N均形成了配位键);该结构中 键角
键角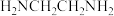 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)
 晶胞与
晶胞与 晶胞相似(如图),
晶胞相似(如图), 晶胞中部分原子的分数坐标为:A点
晶胞中部分原子的分数坐标为:A点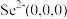 ,从该晶胞中找出距离B点
,从该晶胞中找出距离B点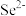 最远的
最远的 的位置
的位置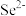 的距离为
的距离为 ,请计算
,请计算 晶胞的密度
晶胞的密度 。
。
您最近一年使用:0次
名校
解题方法
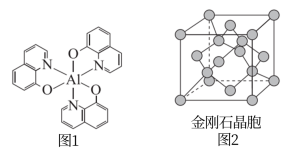
7 . 光电材料在能源军事等领域有重要应用,分为无机光电材料如ZnS、ZnSe、GaAs、 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:
(1)基态Zn原子的价层电子排布图为_____ ;Ga、As、Se的第一电离能由大到小的顺序为___________ 。
(2)图1所示化合物中所含有的化学键类型有_____ (填选项字母),N原子的杂化方式为_____ 。
A.共价键 B.离子键 C.配位键 D.氢键
(3)在水溶液中,以 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:
①表中氧化物之间沸点差异的原因为___________ 。
② 的VSEPR模型为
的VSEPR模型为___________ 。
③ 和
和 分子中,键角更大的是
分子中,键角更大的是___________ 。
(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为___________ 。
②若阿伏加德罗常数的值为 ,ZnS晶体的密度为
,ZnS晶体的密度为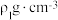 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为___________ 。
 等,及有机光电材料(如图1所示化合物)。回答下列问题:
等,及有机光电材料(如图1所示化合物)。回答下列问题:(1)基态Zn原子的价层电子排布图为
(2)图1所示化合物中所含有的化学键类型有
A.共价键 B.离子键 C.配位键 D.氢键

(3)在水溶液中,以
 为电子供体,
为电子供体, 在
在 光催化剂上可还原为CO,部分氧化物的沸点如表所示:
光催化剂上可还原为CO,部分氧化物的沸点如表所示:| 氧化物 |  |  |  |
| 沸点/℃ | 100 | -10 | -78.5 |
②
 的VSEPR模型为
的VSEPR模型为③
 和
和 分子中,键角更大的是
分子中,键角更大的是(4)ZnS和ZnSe晶体的立方晶胞结构相似,均可看作将金刚石晶胞(如图2)内部的碳原子用Zn代替,晶胞顶角与面心位置的碳原子被S或Se代替。
①ZnS晶体中,Zn原子在S原子围成的正四面体空隙中的占用率为
②若阿伏加德罗常数的值为
 ,ZnS晶体的密度为
,ZnS晶体的密度为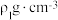 ,ZnSe晶体的密度为
,ZnSe晶体的密度为 ,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
,则ZnS晶体中Zn与S原子最短距离和ZnSe晶体中Zn与Se原子最短距离之比为
您最近一年使用:0次
2022-03-23更新
|
295次组卷
|
2卷引用:河北省张家口市2022届高三第一次模拟考试化学试题
解题方法
8 . 近年来我国在高温超导材料的研究取得了重大突破,高温超导体仅出现在共价性很强的氧化物中,例如带有直线形的Cu-O-Cu链节的网格层对超导性有重要的作用。回答下列问题:
(1)基态Cu原子核外电子排布式为______ 。
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为______ 。
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为______ ;H2O2中氧原子的杂化方式为_______ 。
(4)硫酸铜溶于水后形成的水合铜离子的结构式为____ ,向硫酸铜溶液中逐滴加入氨水直至过量,观察到的现象为___ ,所得结论:与Cu2+形成配位键的能力H2O___ (填“强于”或“弱于”)NH3
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。
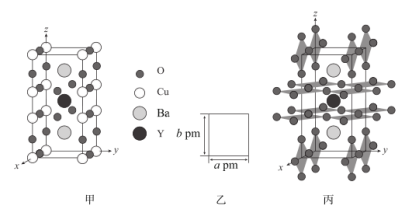
已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为______ 。
②若阿伏加德罗常数的值为NA,则晶体的密度为_____ g·cm-3(用含a、b、c和NA的表达式表示)。
(1)基态Cu原子核外电子排布式为
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为
(4)硫酸铜溶于水后形成的水合铜离子的结构式为
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。

已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为
②若阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
2022-01-22更新
|
1041次组卷
|
4卷引用:广东省肇庆市2021-2022学年高三第二次模拟考试化学试题
广东省肇庆市2021-2022学年高三第二次模拟考试化学试题安徽省“皖南八校”2022届高三下学期第三次联考理综化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)广东省2021-2022学年高三一轮复习质量检测化学试题
名校
解题方法
9 . 锰(Mn)、钴(Co)、镍(Ni)等过渡金属元素化合物的应用研究是前沿科学之一,回答下列问题:
(1)Mn的价电子排布式为___________ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用“___________ 理论”解释。
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列___________ (填序号),每个Mn原子周围紧邻的原子数为___________ 。
A.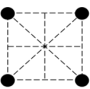 B.
B.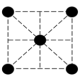 C.
C.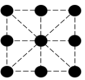 D.
D.
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为SO(CH3)2。DMSO中硫原子的杂化轨道类型为___________ ,SO(CH3)2中键角∠C—S—O___________ CH3COCH3中键角∠C—C—O(填“大于”“小于”或“等于”),ClO 的空间构型是
的空间构型是___________ ,元素S、Cl、O的电负性由大到小的顺序为___________ 。
(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(CH2=CH—CH2OH),其相对分子质量等于丙醛(CH3CH2CHO),但两者沸点相差较大,原因是___________ 。
(5)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为___________ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为apm,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为___________ g(用含a、NA的代数式表示)。
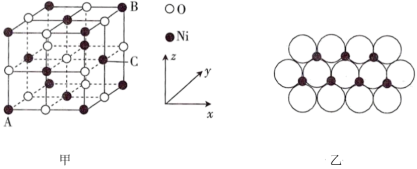
(1)Mn的价电子排布式为
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列
A.
 B.
B. C.
C. D.
D.
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为SO(CH3)2。DMSO中硫原子的杂化轨道类型为
 的空间构型是
的空间构型是(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(CH2=CH—CH2OH),其相对分子质量等于丙醛(CH3CH2CHO),但两者沸点相差较大,原因是
(5)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为

您最近一年使用:0次
2021-12-23更新
|
1198次组卷
|
9卷引用:四川省成都市成都外国语学校2022届高三下学期第二次诊断性考试理科综合化学试题
四川省成都市成都外国语学校2022届高三下学期第二次诊断性考试理科综合化学试题四川省南充高级中学2023-2024学年高三下学期第二次模拟考试化学四川省南充高级中学2024届高三第二次模拟考试理综-化学试题广东省“六校联盟”2021-2022学年高三上学期第三次联考化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)黑龙江省哈尔滨师范大学附属中学2022-2023学年高三上学期10月月考化学试题黑龙江省绥化市绥棱县第一中学2022-2023学年高三上学期10月月考化学试题
名校
解题方法
10 . 铜是人类广泛使用的第一种金属,含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子最高能层的电子排布式为
原子最高能层的电子排布式为___________ 。
(2) 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。
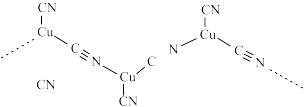
(3) 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为___________ 。
(4)铜能与拟卤素 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸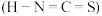 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为___________ ;写出一种与 互为等电子体的分子式
互为等电子体的分子式___________ 。
(5) 可形成
可形成 ,其中
,其中 代表
代表 。
。
①该化合物分子中, 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有___________ 个。
②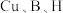 的电负性由大到小的顺序为
的电负性由大到小的顺序为___________ 。
(6)一种由 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
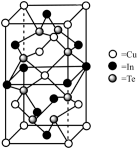
① 的配位数为
的配位数为___________ ;晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ 。
②若晶胞底边的边长均为 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态
 原子最高能层的电子排布式为
原子最高能层的电子排布式为(2)
 稀溶液中存在
稀溶液中存在 。已知d轨道也可以参与杂化,则
。已知d轨道也可以参与杂化,则 中
中 的杂化方式为___________(填选项字母)。
的杂化方式为___________(填选项字母)。A. | B. | C. | D. |
 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键数目之比为
键数目之比为
(4)铜能与拟卤素
 反应。拟卤素
反应。拟卤素 对应的酸有两种,理论上异硫氰酸
对应的酸有两种,理论上异硫氰酸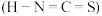 的沸点高于硫氰酸
的沸点高于硫氰酸 ,其原因为
,其原因为 互为等电子体的分子式
互为等电子体的分子式(5)
 可形成
可形成 ,其中
,其中 代表
代表 。
。①该化合物分子中,
 模型为四面体或正四面体的非金属原子共有
模型为四面体或正四面体的非金属原子共有②
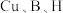 的电负性由大到小的顺序为
的电负性由大到小的顺序为(6)一种由
 组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
①
 的配位数为
的配位数为 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为②若晶胞底边的边长均为
 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,设晶体的最简式的式量为
,设晶体的最简式的式量为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2021-12-03更新
|
997次组卷
|
5卷引用:河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题
河北省石家庄市2021-2022学年高三上学期毕业班教学质量检测(一)化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】20河北省石家庄市2022届高三上学期教学质量检测(一)化学试题(已下线)解密13 物质结构与性质(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)广东省佛山市李兆基中学、郑裕彤中学两校2021-2022学年高三下学期3月联考化学试题



