解题方法
1 . 下列元素或化合物的性质变化顺序正确的是
| A.第一电离能:Cl>S>P>Si |
| B.共价键的极性:HF>HCl>HBr>HI |
| C.价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近一年使用:0次
解题方法
2 . 短周期主族元素A、B可形成AB3分子,下列有关叙述正确的是
A.若A、B为同一周期元素,则 分子一定为平面三角形 分子一定为平面三角形 |
B.若 分子的价电子数为24,则 分子的价电子数为24,则 分子可能为平面三角形 分子可能为平面三角形 |
C.若A、B为同一主族元素,则 分子一定为三角锥形 分子一定为三角锥形 |
D.若 分子为三角锥形,则 分子为三角锥形,则 分子可能为 分子可能为 |
您最近一年使用:0次
2022-08-28更新
|
387次组卷
|
2卷引用:第二节 分子的空间结构 第1课时 分子结构的测定 多样的分子空间结构 价层电子对互斥模型
3 . 在半导体生产或灭火剂的使用中,会向空气中逸散气体,如 、
、 、
、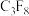 ,它们虽是微量的,有些却是强温室气体。下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体。下列有关推测正确的是
 、
、 、
、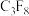 ,它们虽是微量的,有些却是强温室气体。下列有关推测正确的是
,它们虽是微量的,有些却是强温室气体。下列有关推测正确的是A.  属于非极性分子 属于非极性分子 |
B.分子的极性: |
C.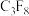 是非极性分子,在 是非极性分子,在 中的溶解度比在水中大 中的溶解度比在水中大 |
D.由价层电子对互斥模型可确定 分子中N原子是 分子中N原子是 杂化,分子呈平面三角形 杂化,分子呈平面三角形 |
您最近一年使用:0次
解题方法
4 . 《科学》杂志发表了中国科学家的原创性重大突破——首次在实验室实现CO2到淀粉的合成的文章,其合成路线如图所示,下列说法正确的是


| A.淀粉分子中含有π键 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C.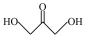 为手性分子。 为手性分子。 |
| D.HCHO中键角:∠OCH大于∠HCH |
您最近一年使用:0次
名校
5 . 价层电子对互斥( )模型是预测分子空间结构的重要方法,下列说法正确的是
)模型是预测分子空间结构的重要方法,下列说法正确的是
 )模型是预测分子空间结构的重要方法,下列说法正确的是
)模型是预测分子空间结构的重要方法,下列说法正确的是A. 的 的 模型为平面三角形 模型为平面三角形 | B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 中心原子杂化轨道类型为 中心原子杂化轨道类型为 杂化 杂化 | D. 的键角小于 的键角小于 |
您最近一年使用:0次
6 . 元素周期表是学习物质结构与性质的重要工具, 如图所示是元素周期表前三周期的一部分。下到关于五种元素的叙述正确的是
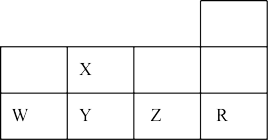

| A.Z的基态原子最外层p轨道上有2个未成对电子 |
| B.WZ3分子的VSEPR模型为三角锥形 |
| C.H2Y键角小于H2X |
| D.第一电离能:R>Y>W |
您最近一年使用:0次
解题方法
7 . Edvhweiler-Clarke反应是在过量甲酸作用下,一级胺或二级胺与甲醛反应生成甲基化的三级胺,具体反应历程如图所示。
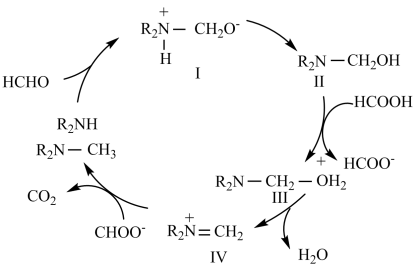
已知:R代表烷基。下列说法正确的是

已知:R代表烷基。下列说法正确的是
| A.反应过程中N的成键数目保持不变 |
| B.物质(I)、物质(II)、物质(III)中N原子VSEPR模型不相同 |
| C.物质III→物质IV过程中有配位键的形成 |
D.总反应为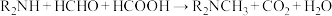 |
您最近一年使用:0次
8 . 短周期主族元素X、Y、Z、W、Q形成的化合物结构如图所示。其中Z、W相邻且与Q同周期,Y、Q同主族,X、Z同主族且Z原子半径更小。下列说法正确的是
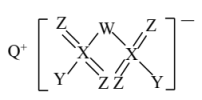
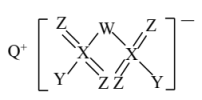
| A.X、Y、Z、W四种元素可形成离子化合物 |
B.电负性: |
| C.Q的单质可保存在煤油中 |
| D.X与Z形成的两种化合物中,X原子杂化方式相同 |
您最近一年使用:0次
21-22高二上·河北衡水·阶段练习
解题方法
9 . 下列分子或离子中,价层电子对互斥模型与分子或离子的几何构型不一致的是
| A.NH3 | B.SO3 | C.CCl4 | D.H2O |
您最近一年使用:0次
名校
解题方法
10 . 下列描述中正确的是
| A.CS2为V形的极性分子 |
B.ClO 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.SF6中有6对完全相同的成键电子 |
D.SiF4和SO 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
您最近一年使用:0次
2021-04-12更新
|
282次组卷
|
2卷引用:第二节 分子的空间结构 第2课时 杂化轨道理论



