解题方法
1 . Ⅰ.MnS纳米粒子被广泛应用于除去重金属离子中的铬离子。
(1)锰的价层电子排布式为______ 。
(2)磁性氧化铁纳米粒子除铬效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-______ S2-(填“>”“<”或“=”)。H3O+中H—O—H的键角比H2O中的______ (填“大”或“小”)
(3)Mn可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为______ ,Mn与CO的C原子形成配位键,该配合物的配位数为______ ,配体NH3的空间结构为______ (用文字描述)。
Ⅱ.
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为______ 。

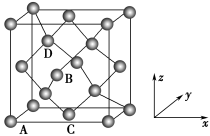
(5)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为______ 。已知金刚石的晶胞参数为apm,则其密度为______ g·cm-3(列出计算式)。
(1)锰的价层电子排布式为
(2)磁性氧化铁纳米粒子除铬效率不如MnS纳米粒子,试比较两种纳米材料中的阴离子的半径大小O2-
(3)Mn可以形成多种配合物,[Mn(CO)(H2O)2(NH3)3]Cl2·H2O中第二周期元素第一电离能由大到小关系为
Ⅱ.
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为

(5)图为金刚石晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
您最近一年使用:0次
名校
2 . NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_____ 。
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_____ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_____ 。
②NaHCO3分解得Na2CO3., 空间结构为
空间结构为_____ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3的中心原子的杂化轨道类型为_____ 。
②比较熔点:NH3BH3_____ CH3CH3(填“>”或“<”)。
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为_____ 。
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是_____ 。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3.,
 空间结构为
空间结构为(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N | F |
| 电负性 | 2.1 | 2.0 | 3.0 | 4.0 |
②比较熔点:NH3BH3
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是
您最近一年使用:0次
2024-03-03更新
|
275次组卷
|
2卷引用:北京市第十九中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
3 . 磷及其化合物在工业生产中起着重要的作用。
(1)基态磷原子的价层电子排布图为
___________ 。
(2)磷元素有白磷、黑磷等常见的单质。黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体具有与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是
___________ (填字母序号)。
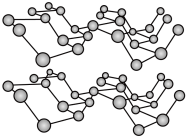
a.黑磷与白磷互为同素异形体 b.层与层之间的作用力是共价键
c.黑磷晶体属于混合型晶体 d.分子中磷原子杂化类型为 杂化
杂化
(3) 与水会形成黄色的配离子
与水会形成黄色的配离子
 ,为避免颜色干扰,常在
,为避免颜色干扰,常在
 溶液中加入
溶液中加入
 形成无色的
形成无色的
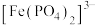 。由此推测,与
。由此推测,与
 能形成更稳定配离子的配体是
能形成更稳定配离子的配体是
___________ ,其空间结构是
___________ 。
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟(InP)的熔点分别为2000、1070℃,二者属于___________ 晶体,其熔点差异的主要原因是___________ 。
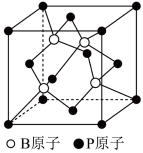
②磷化硼是一种半导体材料,其晶胞结构如图所示。已知晶胞边长apm,阿伏加德罗常数为 ,则磷化硼晶体的密度是
,则磷化硼晶体的密度是___________  (列出表达式)。
(列出表达式)。
(1)基态磷原子的价层电子排布图为
(2)磷元素有白磷、黑磷等常见的单质。黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体具有与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

a.黑磷与白磷互为同素异形体 b.层与层之间的作用力是共价键
c.黑磷晶体属于混合型晶体 d.分子中磷原子杂化类型为
 杂化
杂化(3)
 与水会形成黄色的配离子
与水会形成黄色的配离子 ,为避免颜色干扰,常在
,为避免颜色干扰,常在 溶液中加入
溶液中加入 形成无色的
形成无色的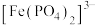 。由此推测,与
。由此推测,与 能形成更稳定配离子的配体是
能形成更稳定配离子的配体是(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟(InP)的熔点分别为2000、1070℃,二者属于
②磷化硼是一种半导体材料,其晶胞结构如图所示。已知晶胞边长apm,阿伏加德罗常数为
 ,则磷化硼晶体的密度是
,则磷化硼晶体的密度是 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
名校
解题方法
4 . A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子层结构,C、D为同周期元素,C元素原子核外电子总数是最外层电子数的3倍;D元素同周期中原子半径最小的元素。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号),其中C原子的核外电子排布式为_______ 。
(2)A的两种单质互为同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为_______ 和_______ 。
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为_______ ,中心原子的杂化轨道类型为_______ 。
(4)化合物D2A的空间结构为_______ ,中心原子的价层电子对数为_______ ;
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。
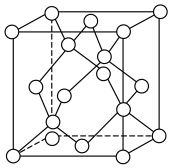
若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为_______ g·cm-3。
(1)四种元素中电负性最大的是
(2)A的两种单质互为同素异形体,其中沸点高的是
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为
(4)化合物D2A的空间结构为
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。

若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
名校
解题方法
5 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布嫦娥五号最新科学成果,中核集团核工业北京地质研究院科研团队首次在月球上发现的新矿物,被命名为“嫦娥石”,我国成为世界上第三个在月球发现新矿物的国家。
回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体___________ 实验等一系列高新技术手段,成功解译其晶体结构。
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为___________ 。
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式___________ ,PO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(4)从结构角度分析Fe3+比Fe2+稳定的原因___________ 。
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为___________ g·cm-3(列出计算式即可)。

回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式
 的VSEPR模型名称为
的VSEPR模型名称为(4)从结构角度分析Fe3+比Fe2+稳定的原因
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为

您最近一年使用:0次
2023-08-12更新
|
396次组卷
|
2卷引用:浙江省金丽衢十二校2022-2023学年高三上学期第一次联考化学试题
解题方法
6 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.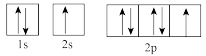 d.
d.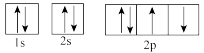
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
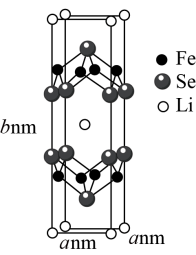
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热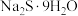 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
解题方法
7 . X、Z、Q、R、T为前四周期元素,且原子序数依次增大。X和Q属同族元素,X和R可形成化合物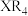 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;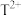 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。
(1)Z基态原子的电子排布式是___________ ;
(2)利用价层电子对互斥模型判断 的空间结构是
的空间结构是___________ ;
(3)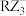 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为___________ 。
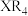 ;
; 为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;
为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;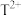 的3d轨道中有5个电子。请回答下列问题。
的3d轨道中有5个电子。请回答下列问题。(1)Z基态原子的电子排布式是
(2)利用价层电子对互斥模型判断
 的空间结构是
的空间结构是(3)
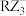 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为
您最近一年使用:0次
名校
解题方法
8 . 中国早在周朝已能冶炼铸铁了。目前,铁及其化合物广泛地应用到各个领域。请回答下列问题:
(1)基态铁原子的电子排布式为_______ 。
(2)我国菱铁矿FeCO3储量较为丰富。其中CO 的空间结构为
的空间结构为_______ 。
(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是_______ 。
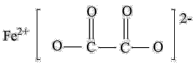
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于_______ 晶体。
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是_______ 。若该晶体的密度是dg·cm-3,则两个最近的Fe间的距离为_______ cm(设NA为阿伏加德罗常数的值)。
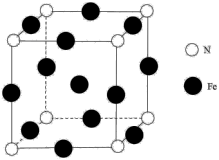
(1)基态铁原子的电子排布式为
(2)我国菱铁矿FeCO3储量较为丰富。其中CO
 的空间结构为
的空间结构为(3)草酸亚铁可作为电池正极材料磷酸铁锂的原料,其结构简式如下,碳原子的杂化方式是
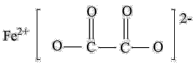
(4)Fe(CO)5溶于汽油、苯、丙酮等有机溶剂,熔点、沸点分别在-20℃、103.6℃左右。因此可知Fe(CO)5属于
(5)铁与氨气反应生成一种如图所示晶胞结构的产物,N周围最近的Fe数目是

您最近一年使用:0次
名校
解题方法
9 . 碳族元素中的Sn和氧族元素中的Te的有机化合物受到广泛关注。文献报道了利用有八面体结构的有机碲酸A与三甲基氯化锡B合成了一种具有抗癌活性的含碲和锡有机化合物C,反应前后Te和Sn的杂化方式不变。请回答下列问题:

(1)Te原子的最高能层理论上所具有的轨道数为_____ 。
(2)气态TeO3分子的立体构型为_____ ;共价化合物B中Sn的杂化方式为_____ 。化合物A中Te与下列化合物中S的杂化方式相同的是_____ (填序号)。
①H2S ②SO2③SO3④SF6
(3)用一个溴原子和一个氯原子取代有机碲酸A中与Te相连的两个羟基,结构仍为八面体,取代后的有机碲酸可能有_____ 种。
(4)有机化合物C核磁共振氢谱显示等效氢的个数比为_____ 。
(5)化合物B可以用SnI4合成,α-SnI4为立方晶体,其晶胞沿面对角线的投影如图所示:
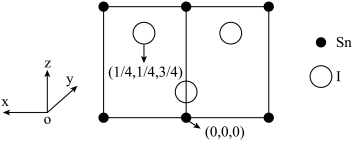
①晶胞中Sn和I之间的最近距离为apm,α-SnI4的密度的计算式为_____ g/cm3(设阿伏加德罗常数为NA);晶胞中由碘原子所围成的空隙中心坐标为_____ 。
②常温常压下SiF4为气态而SiCl4为液态,原因____ ,SnF4和SnCl4都为离子晶体,而SnF4为固体,SiCl4为液体,这是由于F到Cl的变化使得与Sn的卤化物中化学键的离子性____ 、共价性____ 。(填“增强”“不变”或“减弱”)

(1)Te原子的最高能层理论上所具有的轨道数为
(2)气态TeO3分子的立体构型为
①H2S ②SO2③SO3④SF6
(3)用一个溴原子和一个氯原子取代有机碲酸A中与Te相连的两个羟基,结构仍为八面体,取代后的有机碲酸可能有
(4)有机化合物C核磁共振氢谱显示等效氢的个数比为
(5)化合物B可以用SnI4合成,α-SnI4为立方晶体,其晶胞沿面对角线的投影如图所示:

①晶胞中Sn和I之间的最近距离为apm,α-SnI4的密度的计算式为
②常温常压下SiF4为气态而SiCl4为液态,原因
您最近一年使用:0次
名校
解题方法
10 . S单质的常见形式为S8,其环状结构如图所示,
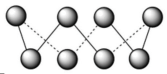
(1)S原子价电子排布式___________ ;S原子的核外不同运动状态的电子数是___________ 个,能量最高的3p轨道的电子云的形状是___________
(2) S8的S原子采用的轨道杂化方式是___________ 。
(3)气态SeO3分子的空间立体构型为___________ , 离子的VSEPR模型为
离子的VSEPR模型为___________ 。
(4)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角___________ (填大或小)

(1)S原子价电子排布式
(2) S8的S原子采用的轨道杂化方式是
(3)气态SeO3分子的空间立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(4)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角
您最近一年使用:0次



