名校
解题方法
1 . 磷及其化合物在工业生产中起着重要的作用。
(1)基态磷原子的价层电子排布图为
___________ 。
(2)磷元素有白磷、黑磷等常见的单质。黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体具有与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是
___________ (填字母序号)。
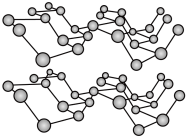
a.黑磷与白磷互为同素异形体 b.层与层之间的作用力是共价键
c.黑磷晶体属于混合型晶体 d.分子中磷原子杂化类型为 杂化
杂化
(3) 与水会形成黄色的配离子
与水会形成黄色的配离子
 ,为避免颜色干扰,常在
,为避免颜色干扰,常在
 溶液中加入
溶液中加入
 形成无色的
形成无色的
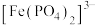 。由此推测,与
。由此推测,与
 能形成更稳定配离子的配体是
能形成更稳定配离子的配体是
___________ ,其空间结构是
___________ 。
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟(InP)的熔点分别为2000、1070℃,二者属于___________ 晶体,其熔点差异的主要原因是___________ 。
②磷化硼是一种半导体材料,其晶胞结构如图所示。已知晶胞边长apm,阿伏加德罗常数为 ,则磷化硼晶体的密度是
,则磷化硼晶体的密度是___________  (列出表达式)。
(列出表达式)。
(1)基态磷原子的价层电子排布图为
(2)磷元素有白磷、黑磷等常见的单质。黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体具有与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

a.黑磷与白磷互为同素异形体 b.层与层之间的作用力是共价键
c.黑磷晶体属于混合型晶体 d.分子中磷原子杂化类型为
 杂化
杂化(3)
 与水会形成黄色的配离子
与水会形成黄色的配离子 ,为避免颜色干扰,常在
,为避免颜色干扰,常在 溶液中加入
溶液中加入 形成无色的
形成无色的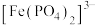 。由此推测,与
。由此推测,与 能形成更稳定配离子的配体是
能形成更稳定配离子的配体是(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟(InP)的熔点分别为2000、1070℃,二者属于
②磷化硼是一种半导体材料,其晶胞结构如图所示。已知晶胞边长apm,阿伏加德罗常数为
 ,则磷化硼晶体的密度是
,则磷化硼晶体的密度是 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
名校
解题方法
2 . A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子层结构,C、D为同周期元素,C元素原子核外电子总数是最外层电子数的3倍;D元素同周期中原子半径最小的元素。回答下列问题:
(1)四种元素中电负性最大的是_______ (填元素符号),其中C原子的核外电子排布式为_______ 。
(2)A的两种单质互为同素异形体,其中沸点高的是_______ (填分子式),原因是_______ ;A和B的氢化物所属的晶体类型分别为_______ 和_______ 。
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为_______ ,中心原子的杂化轨道类型为_______ 。
(4)化合物D2A的空间结构为_______ ,中心原子的价层电子对数为_______ ;
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。
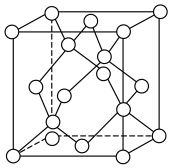
若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为_______ g·cm-3。
(1)四种元素中电负性最大的是
(2)A的两种单质互为同素异形体,其中沸点高的是
(3)C和D可按原子个数比为1∶3形成化合物E,E的空间结构为
(4)化合物D2A的空间结构为
(5)面心立方ZnS晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含粒子数的一半。

若该ZnS晶胞的晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
名校
解题方法
3 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布嫦娥五号最新科学成果,中核集团核工业北京地质研究院科研团队首次在月球上发现的新矿物,被命名为“嫦娥石”,我国成为世界上第三个在月球发现新矿物的国家。
回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体___________ 实验等一系列高新技术手段,成功解译其晶体结构。
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为___________ 。
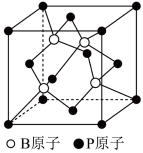
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式___________ ,PO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(4)从结构角度分析Fe3+比Fe2+稳定的原因___________ 。
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为___________ g·cm-3(列出计算式即可)。

回答下列问题:
(1)中核集团核工业北京地质研究院科研团队,通过晶体
(2)嫦娥石是一种陨磷钠镁钙石类矿物,基态P、Na、Mg、Ca四种元素的原子第一电离能由大到小的顺序为
(3)从晶体结构上看,嫦娥石可以分为两大部分,其中阴离子结构单元为[Fe(PO4)6]16-,请写出Fe2+的基态价层电子排布式
 的VSEPR模型名称为
的VSEPR模型名称为(4)从结构角度分析Fe3+比Fe2+稳定的原因
(5)嫦娥石的一种伴生矿物为方石英,方石英结构和金刚石相似,其晶胞结构如图所示,Si-O键长为anm,∠AED=109°28′,已知阿伏伽德罗常数为NA,则方石英晶体的的密度为

您最近一年使用:0次
2023-08-12更新
|
414次组卷
|
2卷引用:浙江省金丽衢十二校2022-2023学年高三上学期第一次联考化学试题
解题方法
4 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.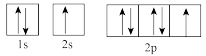 d.
d.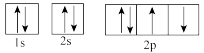
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
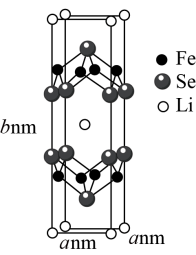
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热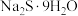 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
名校
解题方法
5 . S单质的常见形式为S8,其环状结构如图所示,
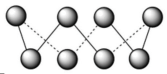
(1)S原子价电子排布式___________ ;S原子的核外不同运动状态的电子数是___________ 个,能量最高的3p轨道的电子云的形状是___________
(2) S8的S原子采用的轨道杂化方式是___________ 。
(3)气态SeO3分子的空间立体构型为___________ , 离子的VSEPR模型为
离子的VSEPR模型为___________ 。
(4)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角___________ (填大或小)

(1)S原子价电子排布式
(2) S8的S原子采用的轨道杂化方式是
(3)气态SeO3分子的空间立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(4)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角
您最近一年使用:0次
名校
解题方法
6 . 磷、硫、氯是重要的非金属元素。回答下列问题:
(1)基态氯原子的核外电子排布式为_______ ;第三周期中第一电离能均大于同周期相邻元素的是_______ (填元素符号)
(2)氮和磷氢化物性质的比较:热稳定性:
_______  (填“>”或“<”)。沸点:
(填“>”或“<”)。沸点:
_______ 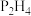 (填“>”或“<”),其沸点大小的判断依据是
(填“>”或“<”),其沸点大小的判断依据是_______ 。
(3)分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),已知
),已知 分子中共含有5对孤电子对,则
分子中共含有5对孤电子对,则 中的大
中的大 键应表示为
键应表示为_______ 。 分子中键角
分子中键角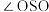
_______  分子中键角
分子中键角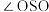 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(1)基态氯原子的核外电子排布式为
(2)氮和磷氢化物性质的比较:热稳定性:

 (填“>”或“<”)。沸点:
(填“>”或“<”)。沸点:
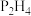 (填“>”或“<”),其沸点大小的判断依据是
(填“>”或“<”),其沸点大小的判断依据是(3)分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 ),已知
),已知 分子中共含有5对孤电子对,则
分子中共含有5对孤电子对,则 中的大
中的大 键应表示为
键应表示为 分子中键角
分子中键角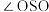
 分子中键角
分子中键角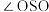 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
您最近一年使用:0次
2023-02-09更新
|
315次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高二上学期期末考试化学试题
名校
7 . 锂 磷酸氧铜电池正极的活性物质是
磷酸氧铜电池正极的活性物质是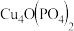 ,可通过下列反应制备:
,可通过下列反应制备: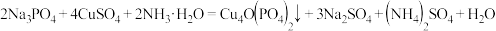
回答下列问题:
(1)上述化学方程式中涉及的 、O、P元素的电负性由小到大的顺序是
、O、P元素的电负性由小到大的顺序是_______ 。
(2)基态 原子的价电子排布式为
原子的价电子排布式为_______ 。
(3) 中含有化学键的类型为
中含有化学键的类型为_______ 。
(4) 空间结构名称为
空间结构名称为_______ ;键角大小比较:NH3_______ H2O (填“大于”或“小于”)
(5)氰气的化学式为 ,结构式为
,结构式为 ,分子中
,分子中 键与
键与 键的个数之比为
键的个数之比为_______ 。
 磷酸氧铜电池正极的活性物质是
磷酸氧铜电池正极的活性物质是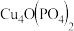 ,可通过下列反应制备:
,可通过下列反应制备: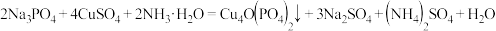
回答下列问题:
(1)上述化学方程式中涉及的
 、O、P元素的电负性由小到大的顺序是
、O、P元素的电负性由小到大的顺序是(2)基态
 原子的价电子排布式为
原子的价电子排布式为(3)
 中含有化学键的类型为
中含有化学键的类型为(4)
 空间结构名称为
空间结构名称为(5)氰气的化学式为
 ,结构式为
,结构式为 ,分子中
,分子中 键与
键与 键的个数之比为
键的个数之比为
您最近一年使用:0次
名校
解题方法
8 . 黄铜矿(CuFeS2)是炼铜的最主要矿物,火法炼铜时发生反应:
(1)Fe在周期表中的位置为____ ;Fe、S、O原子的第一电离能由大到小的顺序是_____ 。
(2)Cu元素的基态原子的电子排布式为_______ ,有_______ 个未成对电子。
(3)SO2分子的立体构型为_______ ,SO2可氧化生成SO3,SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中S原子的杂化轨道类型是_______ 。


(1)Fe在周期表中的位置为
(2)Cu元素的基态原子的电子排布式为
(3)SO2分子的立体构型为

您最近一年使用:0次
解题方法
9 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族,颗粒约2~30微米,伴生矿物有钛铁矿等。回答下列问题:
(1)基态钛原子价电子排布式为_______ 。
(2)Fe的配合物有多种。 、
、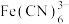 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是_______ (写元素符号,下同);第一电离能由大到小的顺序为_______ 。
(3)磷酸为磷的最高价含氧酸,其空间结构如图:
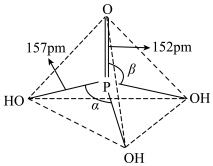
①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
② 的立体构型为
的立体构型为_______ ,中心原子的杂化类型是_______ 。
(4)反型钙钛矿电池无须使用具有光催化活性的 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
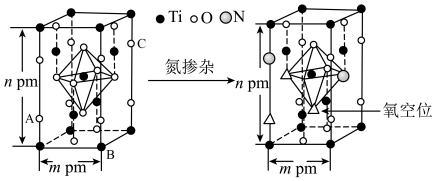
 晶体中
晶体中
_______ ;已知原子A、B的分数坐标分别为 和
和 ,则原子C的坐标为
,则原子C的坐标为_______ ,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为_______ g·cm 。
。
(1)基态钛原子价电子排布式为
(2)Fe的配合物有多种。
 、
、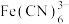 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是(3)磷酸为磷的最高价含氧酸,其空间结构如图:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②
 的立体构型为
的立体构型为(4)反型钙钛矿电池无须使用具有光催化活性的
 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
 晶体中
晶体中
 和
和 ,则原子C的坐标为
,则原子C的坐标为 ,
, 的密度为
的密度为 。
。
您最近一年使用:0次
2023-01-02更新
|
391次组卷
|
3卷引用:吉林省部分学校2022-2023学年高三上学期12月联考化学试题
名校
解题方法
10 . 根据已学物质结构与性质的有关知识,回答下列问题:
(1)请写出第三周期元素中p轨道上有3个未成对电子的元素符号:___________ ,某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是 ,该元素的名称是
,该元素的名称是___________ 。
(2)根据价层电子对互斥理论推测下列离子或分子的空间立体构型:
___________ ,
___________ 。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关反应的离子方程式___________ 、___________ 。
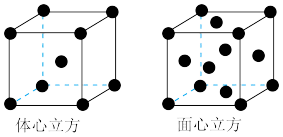
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为___________ ;若两种晶体中最邻近的铁原子间距离相同,则体心立方晶胞和面心立方晶胞的密度之比为___________ 。
(1)请写出第三周期元素中p轨道上有3个未成对电子的元素符号:
 ,该元素的名称是
,该元素的名称是(2)根据价层电子对互斥理论推测下列离子或分子的空间立体构型:


(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关反应的离子方程式
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次



