1 . 下列元素或化合物的性质变化顺序不正确的是
A.第一电离能: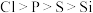 |
B.电负性: |
C.价层电子对互斥理论中, 键电子对数计入中心原子的价层电子对数 键电子对数计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近半年使用:0次
名校
2 . 将X与BeCl2按物质的量比1:1溶于环己烷(溶剂)中得白色沉淀化合物Y,化学式为Be2Cl4I4S4,Y结构如下,下列说法正确的是
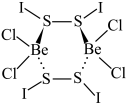
A.X的Lewis结构式为: |
| B.该白色沉淀溶于水会析出游离出S2I2.因为О亲核性强于硫 |
| C.从酸碱反应的角度看X与BeCl2反应,X是酸 |
| D.Y中各元素化学环境相同,其中Be原子的杂化方式与BeCl2一样,都为sp2 |
您最近半年使用:0次
解题方法
3 . 从微粒结构角度分析,下列说法正确的是
A.三氧化硫有单分子气体和三聚分子固体(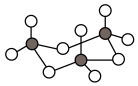 )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
B. 中Al原子采用 中Al原子采用 杂化, 杂化, 离子的空间构型为平面正方形 离子的空间构型为平面正方形 |
C.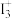 的空间结构为V形,中心原子的杂化方式为 的空间结构为V形,中心原子的杂化方式为 |
D. ( (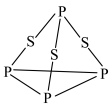 )中S和P原子最外层均满足8电子稳定结构 )中S和P原子最外层均满足8电子稳定结构 |
您最近半年使用:0次
名校
解题方法
4 . 尿素CO(NH2)2是一种高效化肥和化工原料。反应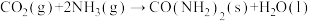 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是
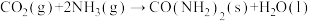 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是| A.CO2分子为极性分子 | B.NH3分子的空间结构为平面三角形 |
C.H2O分子的空间填充模型 | D.尿素分子σ键和π键的数目之比为7:1 |
您最近半年使用:0次
名校
5 . 含元素R的微粒可发生如下反应: 下列说法错误的是
下列说法错误的是
 下列说法错误的是
下列说法错误的是| A.R元素的最高化合价为+7 | B.RO 的空间结构为三角锥形 的空间结构为三角锥形 |
| C.R2在常温常压下一定是气体 | D.R元素位于周期表中的s区 |
您最近半年使用:0次
名校
6 . 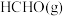 与
与 在催化剂羟基磷灰石(简写为
在催化剂羟基磷灰石(简写为 )表面催化生成
)表面催化生成 和
和 的历程示意图如下。下列说法错误的是
的历程示意图如下。下列说法错误的是

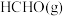 与
与 在催化剂羟基磷灰石(简写为
在催化剂羟基磷灰石(简写为 )表面催化生成
)表面催化生成 和
和 的历程示意图如下。下列说法错误的是
的历程示意图如下。下列说法错误的是
A. 和 和 分子的 分子的 模型都是四面体形 模型都是四面体形 |
| B.羟基磷灰石(HAP)的作用是加快反应速率 |
C. 与 与 分子中的中心原子的杂化轨道类型相同 分子中的中心原子的杂化轨道类型相同 |
| D.该反应过程既有极性共价键的断裂,也有非极性共价键的断裂 |
您最近半年使用:0次
名校
7 . A、B是短周期元素,基态原子最外层电子排布式分别为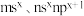 (m>n)。A与B形成的离子化合物加蒸馏水溶解后,观察到白色沉淀,同时有气体逸出,所得溶液和气体均可使酚酞试液变红,下列说法正确的是
(m>n)。A与B形成的离子化合物加蒸馏水溶解后,观察到白色沉淀,同时有气体逸出,所得溶液和气体均可使酚酞试液变红,下列说法正确的是
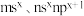 (m>n)。A与B形成的离子化合物加蒸馏水溶解后,观察到白色沉淀,同时有气体逸出,所得溶液和气体均可使酚酞试液变红,下列说法正确的是
(m>n)。A与B形成的离子化合物加蒸馏水溶解后,观察到白色沉淀,同时有气体逸出,所得溶液和气体均可使酚酞试液变红,下列说法正确的是| A.逸出的气体分子的空间构型为三角锥形 |
| B.x为1或者2 |
C.A与B形成的这种离子化合物的摩尔质量为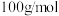 |
D.A元素基态的简单离子核外电子排布式为 |
您最近半年使用:0次
名校
解题方法
8 . 下列有关物质结构与性质说法正确的是
A.酸性: |
B.沸点: |
C.键角: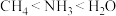 |
D.熔点:对硝基苯酚>邻硝基苯酚(硝基为 ) ) |
您最近半年使用:0次
2023-11-17更新
|
266次组卷
|
2卷引用:上海市行知中学2023-2024学年高三上学期第二次质量监测化学试题
名校
解题方法
9 . 二氟化氧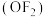 的键角为
的键角为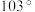 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。
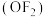 的键角为
的键角为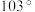 ,是一种无色的剧毒气体,能发生反应:
,是一种无色的剧毒气体,能发生反应: ,下列有关说法正确的是。
,下列有关说法正确的是。A. 难溶于 难溶于 | B. 的键角大于 的键角大于 |
C. 分子中O与F之间存在的是氢键 分子中O与F之间存在的是氢键 | D. 的VSEPR模型名称为正四面体形 的VSEPR模型名称为正四面体形 |
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
10 . 短周期元素X、Y、Z的原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的核外p电子数比s电子数少1个,Z的一种超原子Z 具有40个价层电子。下列说法错误的是
具有40个价层电子。下列说法错误的是
 具有40个价层电子。下列说法错误的是
具有40个价层电子。下列说法错误的是A.XO 的空间结构为平面三角形 的空间结构为平面三角形 |
| B.简单离子半径:Y<Z |
C.YO 的中心原子的杂化方式为sp3杂化 的中心原子的杂化方式为sp3杂化 |
| D.化合物ZY的结构与X的某种单质的结构相似 |
您最近半年使用:0次



