1 . 下列分子中,中心原子不符合“八隅体规则”的是
| A.OF2 | B.SF4 | C.PF5 | D.SiF4 |
您最近一年使用:0次
名校
解题方法
2 . 用价层电子对互斥理论可以预测空间构型,也可以推测键角大小,下列判断正确的是
| A.SO2、CS2、BeCl2都是直线形的分子 |
| B.BF3键角为120°,NF3键角小于120° |
| C.CH2O、BF3、SO3都是平面三角形的分子 |
| D.NH3、PCl3、SF6都是三角锥形的分子 |
您最近一年使用:0次
解题方法
3 . 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.BF3的键角为120° | B.NH3是三角锥形分子 |
| C.SO2是直线形分子 | D.PC13是平面三角形分子 |
您最近一年使用:0次
名校
解题方法
4 . 下列对分子性质的解释中,不正确的是( )
| A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
| B.NF3和BF3的杂化方式不同,前者是sp2后者是sp3 |
| C.HCHO、CH3—、SO3的分子空间构型相同 |
D.由图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子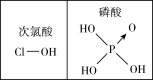 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确的是( )
| A.苯分子中每个碳原子的sp2杂化轨道中的其中一个形成大π键 |
| B.Na3N与NaH均为离子化合物,都能与水反应放出气体,且与水反应所得溶液均能使酚酞溶液变红 |
| C.配离子[Cu(En)2]2+(En是乙二胺的简写)中的配位原子是C原子,配位数为4 |
| D.H2O中的孤对电子数比H3O+的多,故H2O的键角比H3O+的键角小 |
您最近一年使用:0次
名校
6 . 下列描述中正确的是
A.SiF4和 CO 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
B.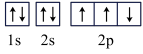 此图错误,违背了泡利原理 此图错误,违背了泡利原理 |
| C.凡中心原子采取sp3 杂化的分子,其 VSEPR 模型都是四面体 |
| D.SO2为 V 形的极性分子 |
您最近一年使用:0次
名校
解题方法
7 . 通常把原子总数和价电子总数相同的分子或离子称为等电子体。人们发现等电子体的空间结构相同,则下列有关说法中正确的是
| A.CH4和NH4+是等电子体,键角均为60° |
| B.H3O+和PCl3是等电子体,均为三角锥形结构 |
| C.NO3﹣和CO32﹣是等电子体,都是平面三角形结构 |
| D.B3N3H6和苯是等电子体,B3N3H6分子中也存在“肩并肩”式重叠的轨道 |
您最近一年使用:0次
名校
解题方法
8 . 工业上用合成气(CO和H2)制取乙醇的反应为2CO+4H2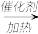 CH3CH2OH+H2O;以CO、O2、NH3为原料,可合成尿素[CO(NH2)2]。下列叙述
CH3CH2OH+H2O;以CO、O2、NH3为原料,可合成尿素[CO(NH2)2]。下列叙述错误 的是
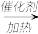 CH3CH2OH+H2O;以CO、O2、NH3为原料,可合成尿素[CO(NH2)2]。下列叙述
CH3CH2OH+H2O;以CO、O2、NH3为原料,可合成尿素[CO(NH2)2]。下列叙述| A.H2O分子VSEPR模型为V形 |
| B.CH3CH2OH分子中亚甲基(-CH2-)上的C原子的杂化形式为sp3 |
| C.在上述涉及的4种物质中,沸点从低到高的顺序为H2<CO< H2O<CH3CH2OH |
| D.CO(NH2)2分子中含有的σ键与π键的数目之比为7:1 |
您最近一年使用:0次
2020-04-16更新
|
177次组卷
|
4卷引用:广东省揭阳市2020届高三下学期线上教学摸底测试化学(理)试题
名校
解题方法
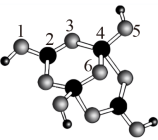
9 . 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法正确的是( )

| A.m=2 |
| B.在Xm-中,硼原子轨道的杂化类型相同 |
| C.1、2原子间和4、5原子间的化学键可能是配位键 |
| D.若382g硼砂晶体中含2molNa+,则硼砂的化学式为Na2B4O7•10H2O |
您最近一年使用:0次
2020-03-07更新
|
209次组卷
|
2卷引用:山东省烟台市2019-2020学年高二上学期期末考试化学试题
2016高二·全国·课时练习
10 . 以下分子或离子的立体构型不是三角锥形的是
| A.NF3 | B.CO32- | C.CO2 | D.H3O+ |
您最近一年使用:0次



